
Ғ@FOLFIRIӮЁӮжӮСFOLFOXӮЖӮМcetuximab•№—p—Г–@ӮНҒA“]ҲЪҗ«‘е’°ҠаӮМҺЎ—ГӮЙ—LҢшӮЕӮ ӮйҒBҚЎүсӮН“]ҲЪҗ«‘е’°ҠаӮМ1st-lineӮЖӮөӮДҒAFOLFIRIӮ ӮйӮўӮНFOLFOXӮМ5-FUӮрҢoҢыFUҚЬӮЕӮ ӮйcapecitabineӮЙ’uӮ«Ҡ·ӮҰӮҪXELIRIҒAXELOXӮЖcetuximabӮМ•№—p—Г–@ӮЙ‘ОӮ·Ӯй–іҚмҲЧү»”дҠr‘жII‘ҠҺҺҢұӮрҚsӮБӮҪҒB
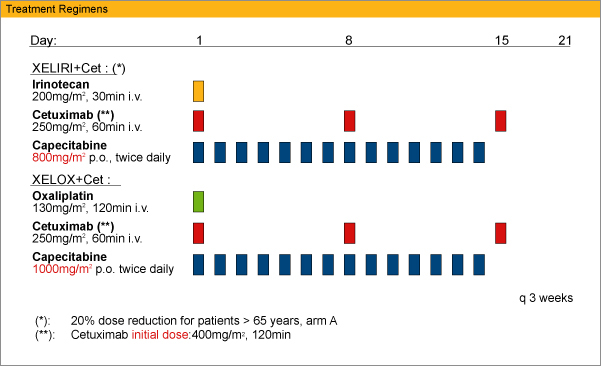
Ғ@“]ҲЪҗ«‘е’°ҠаҠіҺТ185—бӮЙҒAXELIRI (irinotecan (CPT-11) 200mg/m2 day1+capecitabine 800mg/m2ҒA1“ъ2үсҒAday1-14ҒA3ҸT–Ҳ; 65ҚОҲИҸгӮН20%Ңё—К) +cetuximab (400mg/m2 day1ҒAӮ»ӮМҢг–ҲҸT250mg/m2) ӮЬӮҪӮНXELOX (oxaliplatin (L-OHP) 130mg/m2 day1+capecitabin 1,000mg/m2ҒA1“ъ2үсҒAday1-14ҒA3ҸT–Ҳ) +cetuximabӮр“Ҡ—^ӮөӮҪҒB
| ҲкҺҹғGғ“ғhғ|ғCғ“ғgҒF | objective response rate (ORR) |
| “сҺҹғGғ“ғhғ|ғCғ“ғgҒF | time to progression (TTP)ҒAdisease control rate (CR+PR+SD)ҒA”E—eҗ«ҒAgrade 3/4 ӮМ—LҠQҺ–ҸЫ |
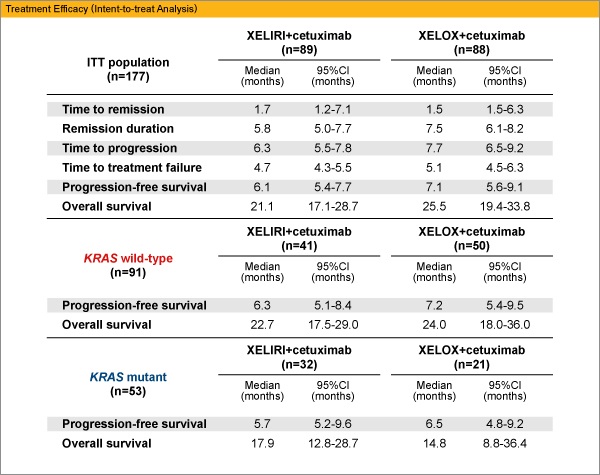
Ғ@Intension-to-treatment үрҗНӮМ‘ОҸЫӮЖӮИӮБӮҪӮМӮН177—б (XELIRI+cetuximabҢQ89—бҒAXELOX+cetuximab ҢQ88—б) ӮЕӮ ӮйҒBORRӮНcetuximab+XELIRIҢQӮӘ46.1%ҒAXELOX+cetuximab ҢQӮӘ47.7%ӮЕӮ ӮиҒAdisease control rate ӮНӮ»ӮкӮјӮк74.2%ӮЖ77.3%ӮЕӮ ӮБӮҪҒBPFS’Ҷүӣ’lӮНӮ»ӮкӮјӮкҒA6.1ғ•ҢҺӮЖ7.1ғ•ҢҺҒAOSӮН21.1ғ•ҢҺӮЖ25.5ғ•ҢҺӮЕӮ ӮБӮҪҒB
Ғ@81.3%ӮМҠіҺТӮЕKRAS ”ӯҢ»Ҹу‘ФӮМүрҗНӮӘүВ”\ӮЕӮ ӮиҒA–мҗ¶Ң^ӮӘ63.2%ҒA•ПҲЩҢ^ӮӘ36.8%ӮЕӮ ӮБӮҪҒBKRAS ”ӯҢ»Ҹу‘ФӮНORRӮЙӮНүeӢҝӮ№ӮёҒAprogression-free survival (PFS) ӮЁӮжӮСoverall survival (OS) ӮНKRAS •ПҲЩҢ^ӮЙ”дӮЧӮД–мҗ¶Ң^ӮЕү„’·Ӯ·ӮйҢXҢьӮӘӮЭӮзӮкӮҪҒB
Ғ@Grade 3/4ӮМ—LҠQҺ–ҸЫӮНҒAүә—ҹӮӘӮ»ӮкӮјӮк15.7%ӮЖ19.3% (p<0.56)ҒA”зҗ]ӮӘ12.4%ӮЖ20.5% (p<0.16)ҒAҗ_Ңo“Еҗ«ӮӘ1.1%ӮЖ14.8% (p<0.01) ӮЕӮ ӮБӮҪҒB
Ғ@“]ҲЪҗ«‘е’°ҠаӮЙ‘ОӮ·Ӯй1st-lineӮЙӮЁӮҜӮйXELIRI+cetuximab—Г–@ҒAӮЁӮжӮСXELOX+cetuximab—Г–@ӮМҢшүКӮЁӮжӮС”E—eҗ«ӮӘҠmӮ©ӮЯӮзӮкӮҪҒB—јғҢғWғҒғ“ӮН“Еҗ«ӮМғvғҚғtғ@ғCғӢӮӘҲЩӮИӮйӮӘҒA—LҢшҗ«ӮЙҚ·ӮНӮИӮ©ӮБӮҪҒBӮөӮ©ӮөҒAcapecitabineӮЖcetuximabӮМ‘gӮЭҚҮӮнӮ№ӮӘ—қ‘z“IӮЕӮ ӮйӮ©ӮНүЫ‘иӮЕӮ ӮйҒB
Ғ@–{–MӮЕӮНҒAӮ·ӮЕӮЙXELOX+bevasizmab—Г–@Ӯ ӮйӮўӮНXELOX+bevasizmab—Г–@ӮӘҲк”Кҗf—ГӮМ’ҶӮЕ•p—pӮіӮкӮДӮўӮйҒBcetuximabӮЖӮМ•№—pӮЙӮВӮўӮДӮа’Қ–ЪӮіӮкӮйӮЖӮұӮлӮЕӮНӮ ӮйӮӘҒACOINҺҺҢұӮЕXELOX—Г–@ӮЖcetuximabӮЖӮМ‘Ҡҗ«ӮМ–в‘иӮӘ’сӢNӮіӮкӮДӮўӮйҒBӮЬӮҪҒAXELIRI—Г–@ӮЙӮВӮўӮДӮНҒACPT-11ӮМҸі”F—p—КӮр’ҙӮҰӮй“Ҡ—^—КӮвcapecitabineӮМҢё—К“Ҡ—^“ҷӮӘӮ ӮиҒAӮ·Ӯ®ӮЙ–{–MӮЕӮМҲк”Кҗf—ГӮЦӮМүһ—pү»ӮН“пӮөӮўӮЖҚlӮҰӮйҒB
(ғҢғ|Ғ[ғgҒFҸјҚг —@Ғ@ғRғҒғ“ғgҒFҚІ“Ў ү·)