
膵癌にはDR5(death receptor 5) およびIGF-1R(insulin-like growth factor 1 receptor)、IGF-1、IGF-2が過剰発現している。
ConatumumabはDR5に対する完全ヒト型モノクローナル抗体で、DR5に結合することでアポトーシスを誘導する。また、AMG479はIGF-1Rに対する完全ヒト型モノクローナル抗体でIGF-1、IGF-2がIGF-1Rに結合するのを阻害することにより、下流へのシグナル伝達を抑制し、細胞増殖を抑える。
これまで、膵癌モデルを用いた前臨床試験で、それぞれの単剤およびgemcitabine(GEM) との併用による抗腫瘍効果が確認され、膵癌または固形癌に対するGEM併用療法の第I相試験が終了している。そこで今回、多施設共同無作為化第II相比較試験を行った。
遠隔転移を有する膵癌(腺癌) の初回治療例を対象に、conatumumab+GEM(CG) 療法群、AMG479+GEM(AG) 療法群、placebo+GEM(PG) 療法群に無作為に割付けた。
・エンドポイント
一次エンドポイント:6ヵ月生存率
二次エンドポイント:奏効率、progression free survival (PFS)、有害事象など
・投与方法
・CG療法:conatumumab 10mg/kg、day1、15、GEM 1000mg/m2、day1、8、15、4週毎
・AG療法:AMG479 12mg/kg、day1、15、GEM 1000mg/m2、day1、8、15、4週毎
・PG療法:placebo day1、15、GEM 1000mg/m2、day1、8、15、4週毎
CG療法群に41例、AG療法群に42例、PG療法群に42例、計125例が登録された。患者背景は3群間に大きな差はなかった。
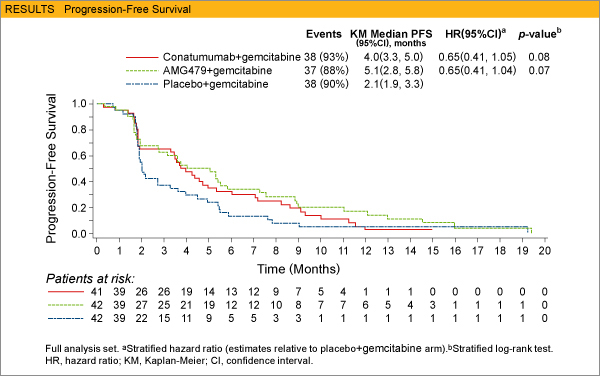
6ヵ月生存率 (CG、AG、PG) は各々59%、57%、50%、progression free survival (PFS) 中央値は4.0ヵ月、5.1ヵ月、2.1ヵ月 (CG vs. PG; HR 0.65、95%CI:0.41-1.05、p=0.08、AG vs. PG; HR 0.65、95%CI:0.41-1.04、p=0.07) とCG療法群およびAG療法群で良好な傾向がみられた。
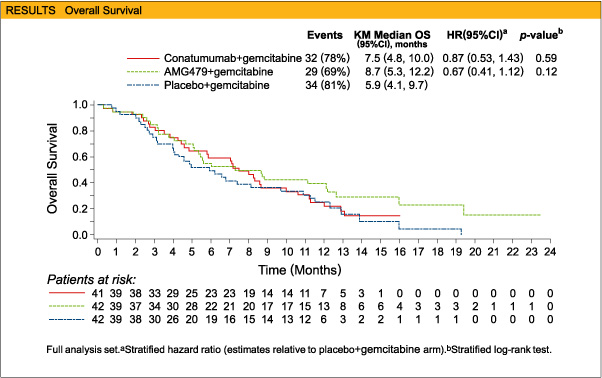
1年生存率(CG、AG、PG) はそれぞれ20%、39%、23%、OS中央値は7.5ヵ月、8.7ヵ月、5.9ヵ月(CG vs. PG; HR 0.87、95%CI:0.53-1.43、p=0.59、AG vs PG; HR 0.67、95%CI:0.41-1.12、p=0.12) とAG群でより良好な傾向であった 。奏効率は各々3%、10%、3%であった。
Grade 3-5の有害事象(CG、AG、PG) は、好中球減少が各々22%、18%、13%、血小板減少 が17%、15%、8%とCG療法群およびAG療法群で高く、高血糖は2%、18%、3%とAG群で高かった。
CG療法およびAG療法は忍容可能であり、遠隔転移を有する膵癌に対する抗腫瘍効果が認められた。本試験の結果より、進行膵癌に対するAG療法のさらなる検証が必要と考えられた。
遠隔転移を有する膵癌において、DR5(TRAILのレセプター) に対する完全ヒト型モノクローナル抗体であるconatumumabと、IGF-1Rに対する完全ヒト型モノクローナル抗体であるAMG479のGEM単独に対する上乗せ効果を検証したplacebo controlの無作為化第II相試験である。
発表者はAMG479の有用性をさらに臨床試験で検証するとしているが、一次エンドポイントである6ヵ月 PFSではconatumumab併用群、AMG479併用群で大きな差を認めなかった。また、IGF-1Rはインシュリンレセプターのkinase domainと84%のhomologyを有するため、IGF-1Rを標的とした薬剤では高血糖は不可避である。
難治癌である膵癌に対しては有効性の確認された治療法が少ないため、より大規模な臨床試験によって、両薬剤の有用性を検証していくべきであると思われる。
(レポート:山崎 健太郎 コメント・監修:寺島 雅典)