背景
ACTS-GC試験は病理学的stage II/IIIの術後胃癌症例を対象とした試験(n=1,059) であり、手術単独群に対して、S-1による術後補助化学療法 (1年) を実施することで、生存期間の有意な延長を示すことが報告されている[5年OS (overall survival): S-1: 71.7% vs. 手術単独:61.1%, HR=0.669, 95%CI: 0.540-0.828: 図1]1)。今回、ACTS-GC試験登録患者の検体を用い、有効性と関連性のある因子を同定するために探索的なバイオマーカー解析を実施した。
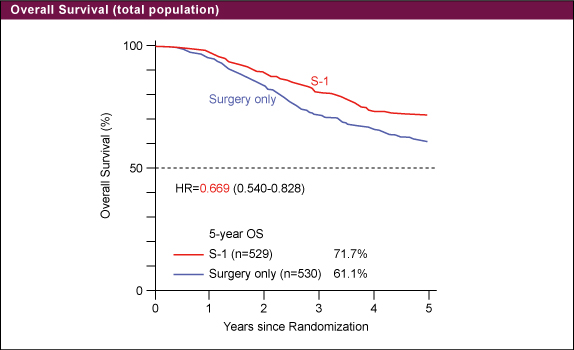 図1
図1対象と方法
ACTS-GC試験に登録された患者1,059例のうち、ホルマリン固定パラフィン包埋切片された検体829例 (78.3%) がレトロスペクティブなバイオマーカー解析の対象となった。ピリミジン代謝経路、成長因子伝達経路、アポトーシス、DNA修復などを含む63の遺伝子がTaqManによる増幅後にRT-PCR法にて定量的に解析され、遺伝子発現レベルに関してはGAPDH、ACTB、RPLP0の幾何学的な平均により標準化され、基準遺伝子として用いられた。それぞれの遺伝子発現に関しては中央値を境に低発現と高発現に分類した。遺伝子発現による生存への影響に関しては、ACTS-GC試験の5年OSを用いて解析された。
結果
検索した63の遺伝子のうち、IGF1RとAREGがOSと強く相関していた (図2)。OSはIGF1R高発現の症例では低発現の症例より有意に不良であったが(5年OS: 61.5% vs. 74.1%、HR=1.638, 95%CI: 1.277-2.101, p<0.0001)、逆にAREGでは高発現の症例で低発現の症例よりも有意に良好な結果だった(5年OS: 73.2% vs. 62.3%, HR=0.640, 95%CI: 0.500-0.820, p=0.0004)。
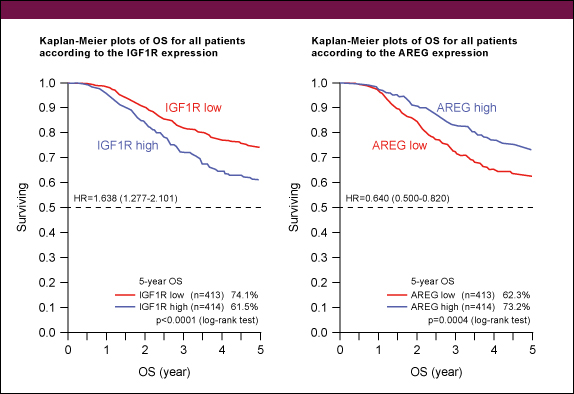 図2
図2S-1群と手術単独群の5年OSを比較してみると、IGF1R低発現群 (78.0% vs. 70.4%. HR=0.716, 95%CI: 0.485-1.058, p=0.092) ではIGF1R高発現群 (69.6% vs. 52.8%, HR=0.552, 95%CI: 0.401-0.762, p=0.0002) よりもハザード比が低く (図3)、一方、AREG低発現群 (70.4% vs. 54.8%, HR=0.570, 95%CI: 0.410-0.792, p=0.0007) ではAREG高発現群 (76.6% vs. 69.6%, HR=0.740, 95%CI: 0.506-1.082, p=0.119) よりハザード比が低かった (図4)。相互作用に関しては有意差を認めなかった。
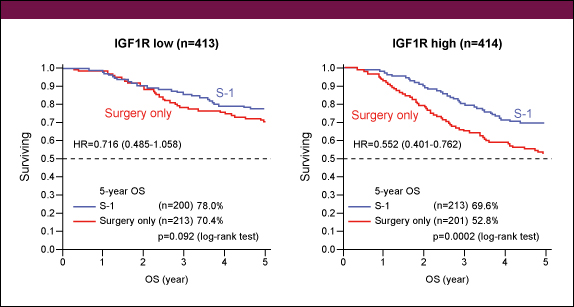 図3
図3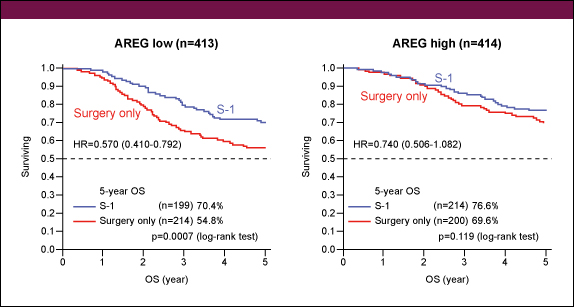 図4
図4結論
IGF1R 遺伝子発現は、病理学的stage II/IIIの根治切除後胃癌症例に対して予後不良と関連性を示したが、AREG 遺伝子発現は良好な生存と関連性を示した。生存期間に対する相互作用は、S-1とこれらの各種遺伝子発現との間に存在しなかった。
コメント
これまで2011年 米国臨床腫瘍学会年次集会2)、2012年 消化器癌シンポジウム3, 4)と2回にわたって発表してきたACTS-GCバイオマーカー研究の3回目の報告である。Low density arrayを用いて63の遺伝子の発現について解析した。その結果、生存転帰と関連が認められたものは、AREGとIGF1Rのみであった。IGF1R高発現例の転帰が不良であることは、胃癌のみならず肺癌や大腸癌など他の癌種でも認められており、今回の結果もそれを支持するものと思われた。胃癌においても今後IGF1Rを標的とした薬剤の開発に期待がかかる。
一方、AREGは、EREGと共にEGFRのリガンドであり、大腸癌などでは高発現例で転帰が不良であることが知られているが、本結果では、AREG高発現例で転帰が良好であったので、これまでの報告と一致しない結果であった。リガンドの発現については、2012年の米国臨床腫瘍学会年次集会でも、EREG発現例の転帰が良好であったとする報告 (#3516)5)もあり、positiveに作用する場合とnegativeに作用する場合とがあるようである。大腸癌ではAREG、EREG発現例で抗EGFR抗体の効果が高いことが知られており、胃癌においてもAREG発現例は抗EGFR抗体治療の良い適応になるものと思われた。ただし、こういったRT-PCRの解析ではcut-off値の設定によって大きく結果が異なるため、臨床に応用するには至適なcut-off値の設定を含めたvalidationが必要である。今後、prognosticおよびpredictiveなマーカーとなる gene setsの同定について解析が加えられる予定である。日本発のGastroPrintの出現に大いに期待したい。
(レポート:結城 敏志 監修・コメント:寺島 雅典)
- Reference
-
- 1) Sasako M, et al.: ESMO2010: abst #709PD [ESMO 2010レポート]
- 2) Terashima M, et al.: 2011 Annual Meeting of the American Society of Clinical Oncology® abst #4013 [学会レポート]
- 3) Sasako M, et al.: 2012 Gastrointestinal Cancers Symposium: abst #52
- 4) Kitada K, et al.: 2012 Gastrointestinal Cancers Symposium: abst #53
- 5) Adams RA, et al.: 2012 Annual Meeting of the American Society of Clinical Oncology®: abst #3516 [学会レポート]

