皮膚障害と治療効果
吉野: 続いて、抗EGFR抗体薬による皮膚障害と治療効果の関連についてディスカッションを深めたいと思います。市川先生、よろしくお願いします。
市川: CetuximabやPanitumumabの治療に伴う皮膚障害の程度は、KRAS exon 2変異型の患者においても治療効果と強く相関することが知られています。また、2010年の米国臨床腫瘍学会年次集会で発表された、PRIME試験のKRAS exon 2野生型における皮膚障害の影響に関する報告では、皮膚障害がgrade 2以上の患者はgrade 0/1の患者に比べて、奏効率、PFS、OSのいずれも有意に良好でした。そこで我々は、The New England Journal of Medicine誌に掲載されたDouillard 先生のPRIME試験におけるRAS 解析についての論文に対して以下の質問を寄せた結果、誌面上でcorrespondenceとして掲載されました10)。
質問は、Panitumumabの有効性と皮膚障害の強さとの関連性はRAS 野生型でもみられるのか、また、RAS 変異型でも皮膚障害と有効性の間に関連性はみられるのか、です。
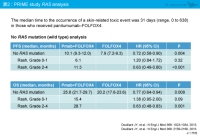
Douillard: 結論から言えば、RAS 野生型においてもKRAS exon 2野生型と同様に、皮膚障害がgrade 2以上の患者は、PFS (HR=0.63, 95% CI: 0.49-0.80, p<0.001)、OS (HR=0.63, 95% CI: 0.48-0.83, p=0.001) いずれもベネフィットを認め、grade 0/1の患者は予後不良でした (表2)。また、興味深いことにKRAS 変異型でも同様の傾向が認められています。ただ、RAS 変異型におけるFOLFOX4 + Panitumumab群では、皮膚障害がgrade 2以上の患者は、grade 0/1の患者よりもPFS (7.5 vs. 5.7ヵ月)、OS (17.6 vs. 9.9ヵ月) いずれも良好ですが、それでもFOLFOX4群 (PFS: 8.7ヵ月、OS: 18.7ヵ月) のほうが優っています (表3)。つまり、皮膚障害と治療効果に直接的な関連があるわけではなく、皮膚障害を発現する患者は恐らく免疫反応あるいは炎症反応などが持続しているため、良好な成績が得られるのだと考えられます。
なお、CPT-11 + Cetuximabの投与22日後に皮膚障害がgrade 0/1であった症例を対象に、Cetuximabを標準量投与する群と、grade 2の皮膚障害が発現するまで増量し続ける群とを比較したEVEREST試験では、KRAS (exon 2) 野生型においては増量群で奏効率が良好だったものの、KRAS 変異型では差を認めませんでした11)。しかし、症例数が少なかったため、現在、1st-lineにおけるFOLFIRI + Cetuximabにおいて、同様に標準量群と増量群を比較した第II相試験であるEVEREST2試験が進行中です12)。ただ、EVEREST2試験の対象はKRAS exon 2野生型なので、RAS 解析による結果が望まれます。
市川: 皮膚障害の重症度は、薬物動態の代理マーカーになり得るのでしょうか。
Douillard: それはまだわかりませんが、治療効果の臨床的指標にはなると思います。RAS 野生型のFOLFOX4 + Panitumumab群における皮膚障害がgrade 0/1の症例では、FOLFOX4単独群のほうがPFSとOSともに優っていました。
吉野: PRIME試験は対照群がFOLFOXと強力な化学療法であったため、BSCと比較した20020408試験でRAS 変異型における皮膚障害についての解析が行われれば、皮膚障害の程度が効果予測因子になるのか予後因子なのか、ある程度の答えは出るかもしれません。
RAS 変異型における抗EGFR抗体薬のメカニズム
吉野: 他に質問はありますか。
谷口: RAS 変異型に対するPanitumumabの投与は、効果がみられないだけでなく、むしろ不良です。どういったメカニズムなのでしょうか。
Douillard: FIRE-3試験のRAS 変異型では、FOLFIRI + Cetuximab群はFOLFIRI + Bevacizumab群に対してOSは少し下回るものの有意差はありません。一方、PRIME試験のRAS 変異型では、FOLFOX4 + Panitumumab群はFOLFOX4群に対して有意に不良です。なぜFOLFIRIではなく、FOLFOXとの併用で悪影響がみられるのでしょうか。いくつか仮説が考えられますが、FOLFOXと抗EGFR抗体薬との間の薬物相互作用が挙げられます。肺癌においても、プラチナ製剤 + EGFRチロシンキナーゼ阻害剤の併用療法は有効性を認めていません13, 14)。恐らくプラチナ製剤によるDNA損傷が修復機構に影響を与えるのだと思われます。
吉野: Scott Kopetz先生は、プラチナ製剤であるL-OHPおよび抗EGFR抗体薬の耐性と、非受容体型チロシンキナーゼSrcの活性化との関連について報告しています15)。
Douillard: 可能性はあると思います。メカニズムは明確ではありませんが、細胞株レベルにおいてはDNA修復機構レベルでの薬物相互作用を示すデータがあります。
市川: Jordan Berlin先生は、The New England Journal of Medicine誌のeditorialで、変異型のRAS アイソフォームと野生型のRAS アイソフォームとの相互作用について指摘されていますね16)。
Douillard: 仮説の1つですが、検証は非常に困難です。腫瘍にはRAS 変異のある細胞も変異のない細胞もありheterogeneityです。
RAS の次の新たなバイオマーカー
吉野: RAS 検査の臨床的意義は確立しましたが、RAS 以外に抗EGFR抗体薬における新しいバイオマーカーは考えられますか。
Douillard: PRIME試験における他のバイオマーカー解析について討議していますが、私はPI3Kを検討したいと思っています。ただ問題は、腫瘍組織が足りなくなってきていることです。
吉野: DNAのストックは非常に重要ですね。MD Anderson Cancer Centerの報告では、PIK3CA exon 20、特にH1047R変異乳癌がPI3K/AKT/mTOR阻害剤により劇的な反応を示しています17)。したがって、PIK3CA 変異を有する大腸癌患者において抗EGFR抗体薬の効果が認められない場合は、PI3K/AKT/mTOR阻害剤が期待されます。
Douillard: PIK3CA 変異型に対しては、アスピリンの効果も報告されています18)。アスピリンは安価ですし、非常に印象的です。
吉野: COX-2阻害剤は有効性が認められていませんが、なぜアスピリンに効果があるのでしょうか。
Douillard: アスピリンはCOX-2阻害だけでなく、もっと幅広い作用があるからではないでしょうか。まだアスピリンの作用は全て明らかになっていません。
吉野: 現在、結腸癌に対する術後補助化学療法におけるFOLFOX/XELOXの6ヵ月投与と3ヵ月投与を比較するIDEA研究が、日本を含めた国際メタ解析プロジェクトとして実施中ですが、米国のCALGB80702試験は、COX-2阻害剤Celecoxibの有無を加えた2×2 factorial designになっています19)。CALGB80702試験の結果が、COX-2阻害剤あるいはアスピリンの有用性を検討する例証になるかもしれません。
本日は、KRAS exon 2からRAS 検査へのパラダイムシフトについて議論してきました。PRIME試験やFIRE-3試験などのRAS 解析により、RAS 検査の臨床的意義が確立されました。そして、今年の米国臨床腫瘍学会年次集会で報告されるCALGB80405試験が、PEAK試験やFIRE-3試験と同様の傾向を示せば、切除不能進行・再発大腸癌患者の約半数であるRAS 野生型に対しては、抗EGFR抗体薬が1st-lineで使用されるようになるでしょう。
また、皮膚障害の程度は、Panitumumab投与の臨床的指標になりますが、RAS 変異型では皮膚障害の程度にかかわらずFOLFOX単独が上回っていました。皮膚障害の程度が予後因子なのか、効果予測因子なのかについては、BSCと比較した20020408試験で同様の解析を行うことで示されると考えられます。
Douillard先生、市川先生、谷口先生、本日はありがとうございました。
