The European Cancer Congress 2013 - ESMO


丂FIRE-3帋尡偼丄僪僀僣偺AIO僌儖乕僾偑峴偭偨丄悽奅弶偺Cetuximab偲Bevacizumab傪捈愙斾妑偟偨戞III憡帋尡偱偁傞丅崱擭偺暷崙椪彴庮釃妛夛偱KRAS codon12, 13栰惗宆偵偍偄偰FOLFIRI + Cetuximab孮偑FOLFIRI + Bevacizumab孮偵懳偟偰OS (overall survival) 偺拞墰抣偱3.7儠寧偺嵎傪弌偟偰桳堄側墑挿傪帵偟偨丅
丂峈EGFR峈懱栻偼KRAS 堚揱巕偵曄堎偑偁傞偲岠壥偑側偄偽偐傝偐丄暪梡偡傞峈娻嵻偺岠壥尭庛傪棃偟偰偟傑偄丄摿偵L-OHP儀乕僗偺峈娻嵻偲偺暪梡偱傛傝尭庛偡傞偙偲偑巜揈偝傟偰偄偨丅偦偺偨傔丄條乆側僶僀僆儅乕僇乕偺尋媶偑峴傢傟丄傛傝岠壥傪敪婗偱偒傞徢椺偺峣傝崬傒偑柾嶕偝傟偰偄偨丅偙偺側偐偱偼丄峈EGFR峈懱栻偱偁傞Panitumumab偵偍偄偰KRAS 偺codon12, 13埲奜偺曄堎傗丄摨偠RAS 僼傽儈儕乕偱偁傞NRAS 偺曄堎傪彍偔偙偲 (RAS 栰惗宆) 偱丄傛傝岠壥偑婜懸偱偒傞懳徾孮偑峣傝崬傔傞偙偲偑丄崱擭偺暷崙椪彴庮釃妛夛偱曬崘偝傟偨 (PEAK帋尡丄PRIME帋尡丄20020408帋尡) 丅崱夞偺曬崘偱偼丄摨條偺孹岦偑Cetuximab偱傕擣傔傜傟傞偐偲偄偆揰丄CPT-11儀乕僗偺峈娻嵻暪梡偵傛傝偳傟偩偗塭嬁偑弌傞偐偑拲栚偝傟偰偄偨丅
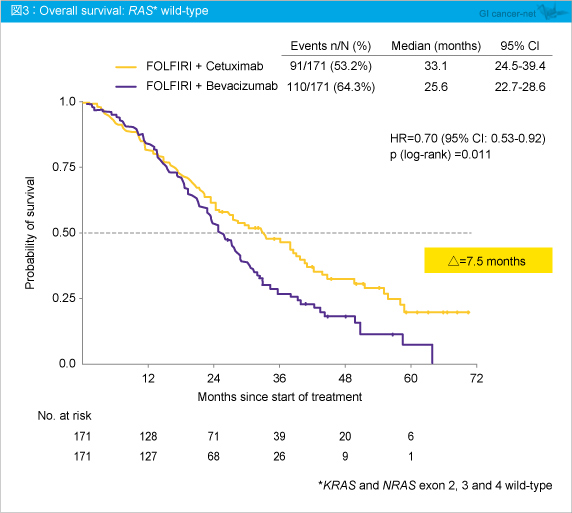
丂寢壥偼丄RAS 栰惗宆偵偍偄偰FOLFIRI + Cetuximab孮偑FOLFIRI + Bevacizumab孮偵懳偟OS偺僴僓乕僪斾0.7丄拞墰抣偱7.5儠寧偺嵎傪弌偟丄OS偺夵慞傪帵偡寢壥偲側偭偨丅
丂尩奿偵尵偆偲CALGB/SWOG 80405帋尡偺寢壥傪懸偮昁梫偑偁傞偲巚傢傟傞偑丄崱屻偼RAS 栰惗宆偺1st-line偼峈EGFR峈懱栻傪壛偊偨帯椕丄RAS 曄堎宆偺1st-line偼Bevacizumab傪壛偊偨帯椕傊偲丄柧妋側惐傒暘偗偑恑傓偙偲偑梊憐偝傟傞丅
丂傑偨丄偙傟傜偺寢壥傪椪彴偵梡偄傞偨傔偵丄慡偰偺RAS 堚揱巕偺曄堎偵懳偡傞専嵏宯偺妋棫偑媫柋偱偁傞丅
丂FIRE-3帋尡 (AIO丄KRK-0306) 偼丄KRAS 栰惗宆愗彍晄擻恑峴丒嵞敪戝挵娻偺1st-line偵偍偄偰丄FOLFIRI + Cetuximab (Cetuximab孮) 偲FOLFIRI + Bevacizumab (Bevacizumab孮) 偺桳梡惈傪斾妑偡傞柍嶌堊壔戞III憡帋尡偱偁傞丅杮擭偺暷崙椪彴庮釃妛夛偱丄Cetuximab孮偼Bevacizumab孮偵懳偟偰憈岠棪 (62 vs. 58%, p=0.183) 丄PFS (progression-free survival) (10.0 vs. 10.3儠寧, p=0.547) 偵偼嵎傪擣傔側偐偭偨傕偺偺丄OS偵偍偄偰桳堄側墑挿岠壥傪帵偟偨 (28.7 vs. 25.0儠寧, HR=0.77, p=0.017) 丅崱夞丄帠慜偵寁夋偝傟偨僶僀僆儅乕僇乕夝愅傪峴偭偨偺偱丄偦偺寢壥傪曬崘偡傞丅
丂KRAS exon 2 (codon 12, 13) 栰惗宆偺愗彍晄擻恑峴丒嵞敪戝挵娻姵幰偵偍偄偰丄KRAS exon 3 (codon 61) 丄exon 4 (codon 146) 丄NRAS exon 2 (codon 12, 13) 丄exon 3 (codon 59, 61) 丄exon 4 (117, 146) 偍傛傃BRAF exon 11丄exon 15 (codon 600) 偺曄堎偑憈岠棪丄PFS丄OS偵媦傏偡塭嬁偵偮偄偰夝愅傪峴偭偨丅
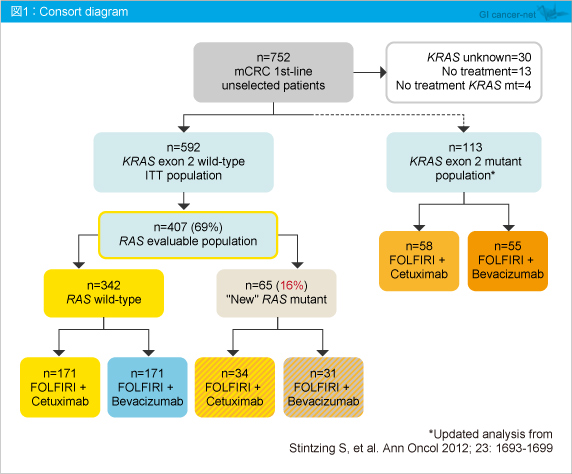
丂奺堚揱巕偺曄堎椺偼丄KRAS exon 3: 4.3%丄exon 4: 4.9%丄NRAS exon 2: 3.8%丄exon 3: 2亾丄exon 4: 0%丄BRAF exon 11: 0%丄exon 15: 10%偱偁傝丄RAS 夝愅偑壜擻偱偁偭偨407椺偺偆偪丄342椺偑慡偰RAS 栰惗宆偱丄65椺 (16%) 偵壗傜偐偺RAS 曄堎傪擣傔偨 (RAS 曄堎宆) (恾1) 丅
丂姵幰攚宨偼丄ITT夝愅 (KRAS exon 2栰惗宆) 椺偲RAS 夝愅椺偲偺娫偱僶儔儞僗偑偲傟偰偄偨丅側偍丄RAS 夝愅椺偵偍偗傞2nd-line帯椕偼丄Cetuximab孮偱L-OHP: 62.0%丄Bevacizumab: 46.0%丄峈EGFR峈懱栻17.5%偱偁傝丄Bevacizumab孮偱L-OHP: 63.1%丄Bevacizumab: 15.4%丄峈EGFR峈懱栻43.8%偱偁偭偨丅
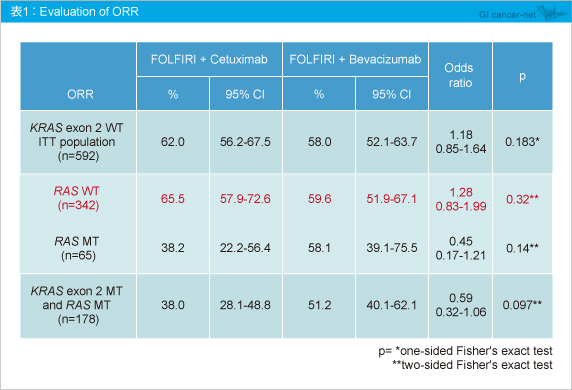
丂FIRE-3帋尡偺庡梫昡壙崁栚偱偁傞憈岠棪偼丄RAS 栰惗宆偱Cetuximab孮65.5%丄Bevacizumab孮59.6%偲丄ITT夝愅傛傝傕嵎偑峀偑偭偨傕偺偺丄桳堄嵎偼擣傔傜傟側偐偭偨 (昞1) 丅堦曽丄RAS 曄堎宆偱偼偦傟偧傟38.2%丄58.1%偲Cetuximab孮偱晄椙側孹岦偵偁偭偨丅
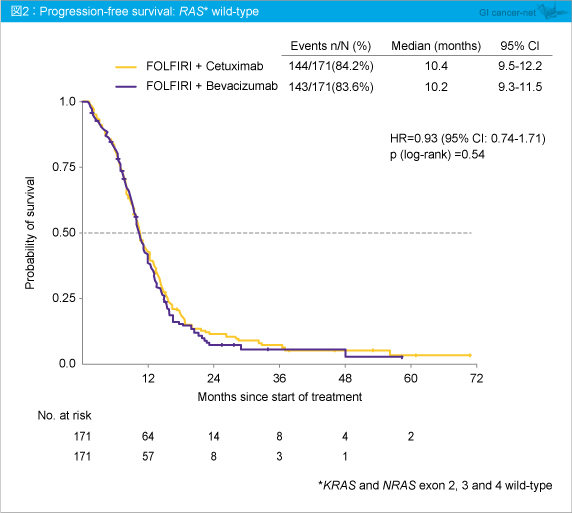
丂FIRE-3帋尡偵偍偗傞RAS 夝愅偱偼丄RAS 栰惗宆偵偍偄偰憈岠棪丄PFS偱偼桳堄嵎傪擣傔側偐偭偨傕偺偺丄OS偼Cetuximab孮偑Bevacizumab孮偵懳偟偰拞墰抣偱7.5儠寧偺墑挿傪傒偣丄僴僓乕僪斾偼0.70偱偁偭偨丅堦曽丄壗傜偐偺RAS 曄堎傪擣傔偨徢椺偱偼Cetuximab孮偼Bevacizumab孮偵懳偟偰儀僱僼傿僢僩偼傒傜傟側偐偭偨丅 偟偨偑偭偰丄愗彍晄擻恑峴丒嵞敪戝挵娻偵懳偟偰偼丄RAS (KRAS 丄NRAS ) 曄堎偺専嵏偑嫮偔悇彠偝傟傞丅慡偰偺RAS 偑栰惗宆偵偍偗傞1st-line帯椕偱偼丄Cetuximab傪娷傓儗僕儊儞偑椪彴揑儀僱僼傿僢僩傪傕偨傜偡偲峫偊傜傟傞丅