背景と目的
標準治療後の切除不能進行・再発大腸癌に対する3rd-lineとしてのPanitumumab単剤療法の有効性を検証した無作為化比較第III相試験 (20020408試験) の探索的なバイオマーカー解析により、KRAS exon2 (codon 12, 13) 変異以外のKRAS、NRAS 変異の有無もPanitumumabの効果予測因子となる可能性が示されている1)。
今回、1st-lineとしてPanitumumab + FOLFOX療法とFOLFOX療法の比較第III相試験 (PRIME試験) の登録例の腫瘍組織を用いて、KRAS (exon 2を除く)、NRAS、BRAF 遺伝子まで拡大して追加解析を行った。
対象と方法
PRIME試験に登録され、保存された腫瘍組織検体がTherascreen® KRAS Mutation KitでKRAS exon 2野生型と判定された患者を対象に、サンガー法によるDNAシークエンシングならびにWAVE-based SURVEYOR® Scan Kitを用いてKRAS exon 3 (codon 61)、4 (codon 117, 146)、NRAS exon 2 (codon 12, 13)、3 (codon 61)、4 (117, 146)、BRAF exon 15 (codon 600) の遺伝子変異の有無を測定し、これらの変異が、PRIME試験においてPFS (progression-free survival)、OS (overall survival) にどのような影響を与えるかについて解析した。
結果
PRIME試験で無作為化された患者1,183例のうち、1,060例 (90%) でRAS 変異の評価が可能であった。
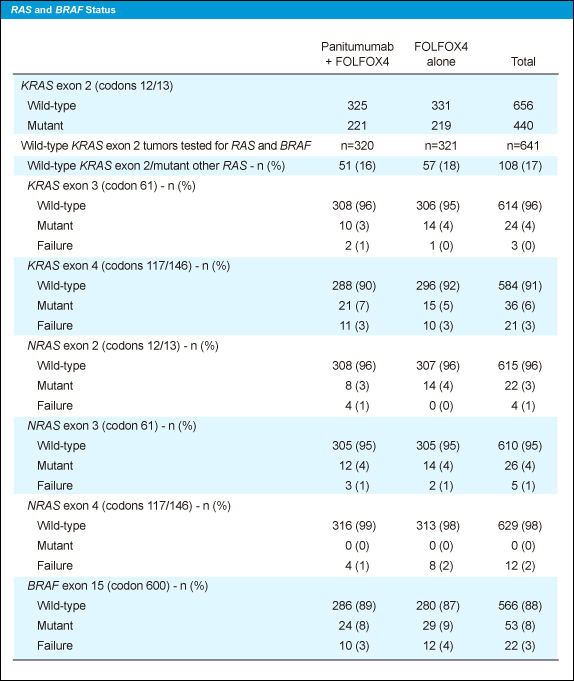
KRAS exon 2野生型患者641例中108例 (17%) に変異が認められ、その内訳はKRAS exon 3変異が24例 (4%)、KRAS exon 4変異が36例 (6%)、NRAS exon 2変異が22例 (3%)、NRAS exon 3変異が26例 (4%)、NRAS exon 4変異は0例 (0%)であった。また、BRAF exon 15 変異は53例 (8%) に認められた (表1)。
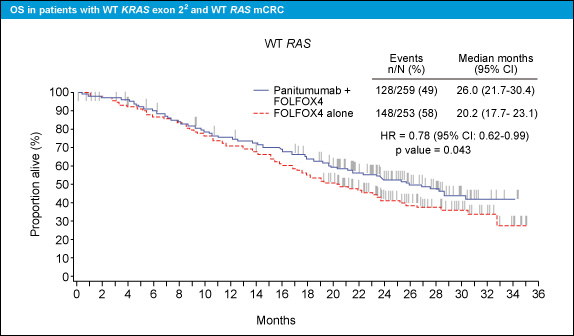
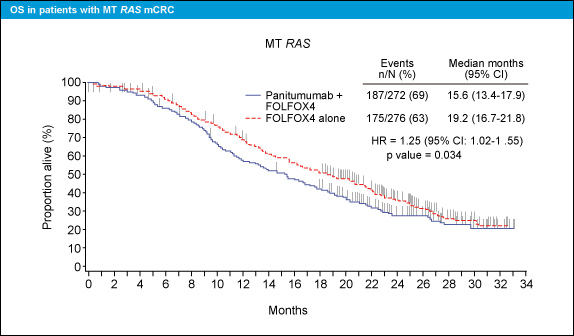
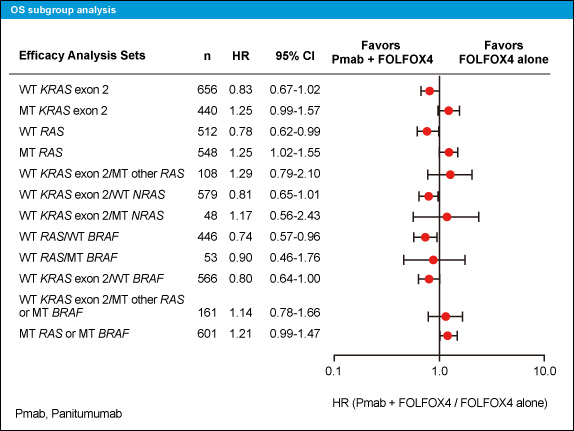
RAS 野生型 (KRAS、NRAS すべて野生型) においてOSを比較したところ、Panitumumab + FOLFOX群はOS中央値が26.0ヵ月であり、FOLFOX群の20.2ヵ月と比較して5.8ヵ月の有意な延長を認めた (HR=0.78, 95% CI: 0.62-0.99, p=0.043) (図1)。一方、RAS 変異型 (KRAS、NRAS変異型) では、OS中央値はそれぞれ15.6ヵ月、19.2ヵ月であり、Panitumumab + FOLFOX群が有意に不良であった (HR=1.25, 95% CI: 1.02-1.55, p=0.034) (図2)。
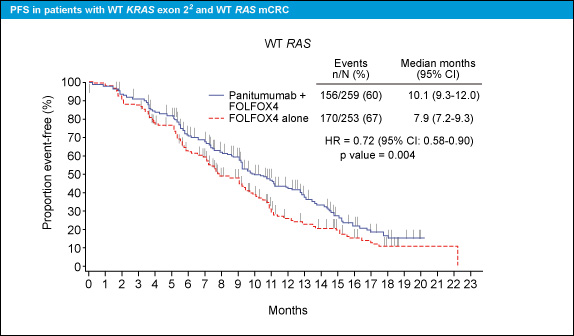
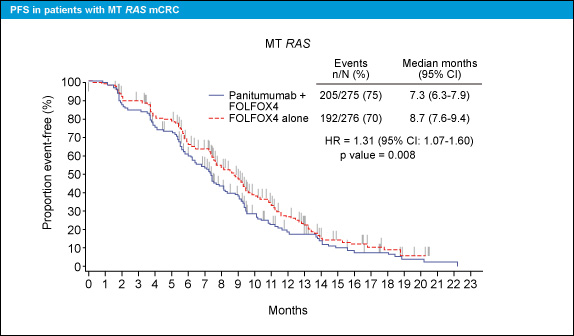
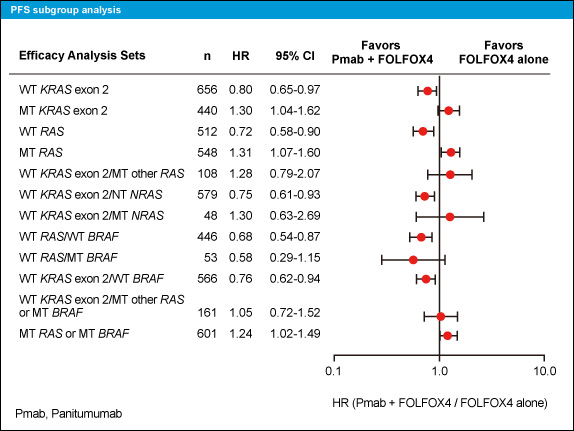
PFSについても、RAS 野生型ではPanitumumab併用群で有意に良好であったが (中央値10.1ヵ月 vs. 7.9ヵ月、HR=0.72, 95% CI: 0.58-0.90, p=0.004) (図3)、RAS 変異型では不良であった (中央値7.3ヵ月 vs. 8.7ヵ月、HR=1.31, 95% CI: 1.07-1.60, p=0.008) (図4)。
なお、RAS 野生型でのPanitumumab併用によるOS、PFSへの上乗せ効果は、RAS codon 59変異症例7例を除外すると、さらに顕著になった (PFS: HR=0.71, p=0.002、OS: HR=0.77, p=0.032)。
一方、BRAF 変異型ではFOLFOXに対するPanitumumab + FOLFOXのOS、PFSのHRはそれぞれ0.90、0.58であり、Panitumumab併用の効果が示唆される傾向にあった (図5、6)。
結論
PRIME試験での無作為化患者のうち、90%の症例で追加のRAS 変異が評価でき、exon 2野生型の17%でRAS 変異が確認された。RAS 野生型の患者に対するPanitumumab + FOLFOXは、FOLFOXと比較して5.8ヵ月のOS中央値の延長が認められた。また、BRAF 変異の有無はPanitumumabの効果予測因子とはならなかった。
コメント
本研究は、PRIME試験の登録症例中、90%に追加解析がなされRAS の評価ができた素晴らしい研究である。抗EGFR抗体薬の使用は、KRAS 野生型であることが必須であったわけであるが、今回の研究により、従来KRAS 野生型とされていた中にさらに他の遺伝子変異が潜んでいることが判明した。すべてのRAS 変異を除いた野生型ではOS がPanitumumab併用群で26.0ヵ月と従来の報告をさらに伸ばし、FOLFOX単独群に比し5.8ヵ月の延長を認めた。一方、変異型ではPanitumumab併用群で3.6ヵ月短縮していた。個別の詳細を見てもNRAS 野生型ではHRは0.81なのに対し変異型では1.17であるため、Panitumumab投与で不利な傾向にありそうだが、結論付けるためにも今後の検討を待ちたい。BRAF に関しては変異の有無で、両群で特に差は見られず効果予測因子ではなく、予後因子であることが考えられ、変異群でPanitumumab上乗せは若干良い傾向であった。
本研究結果により、将来的には事前に無効群を調整し、無駄な副作用を受ける患者を減らすことができるようになるかもしれない。上述の如く、すべて野生群でのPanitumumab併用群のOSは明らかに改善しており、これらの検査法がシステムも含めて各施設で完備されれば、バイオマーカーによる個別化治療がさらに効率よく進められることになろう。
(レポート:谷口 浩也 監修・コメント:小松 嘉人)
- Reference
-
- 1) Peeters M, et al.: Clin Cancer Res. 19(7): 1902-1912, 2013 [PubMed]