グループ2に対する早期腫瘍縮小
既にお話があったように、ESMOガイドラインでは患者を4つのグループに分類しており、グループ1では「最大限」の腫瘍縮小が求められ、グループ2では「早期」の縮小効果が求められます。
今年の米国臨床腫瘍学会で発表されたPEAK試験、FIRE-3試験の奏効率は、いずれも抗EGFR抗体薬併用群において良好な傾向がみられています。また、CRYSTAL試験、OPUS試験においては治療後8週以内に20%以上腫瘍が縮小した早期腫瘍縮小 (ETS) 症例は、Cetuximab併用群が化学療法単独群に比べて、CRYSTAL試験で13%、OPUS試験で23%多くみられ、ETSは症状の改善につながっていることも報告されています6)。
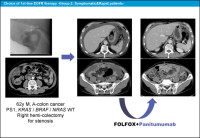
ここで、グループ2の症例を紹介します。図10は62歳の男性で、KRAS /BRAF /NRAS 野生型の上行結腸癌です。結腸狭窄のために結腸右半切除術を受けました。術後2週以内に腹水の増大、腹膜転移が見られたためFOLFOX + Panitumumab療法が行われ、症状の改善を得ることができました。
グループ3に対するOSの延長
次はグループ3に対する治療です。グループ3では生存期間の延長とQOLの向上が求められます。
PEAK試験とFIRE-3試験の結果は、KRAS 野生型大腸癌において、Bevよりも抗EGFR抗体薬による治療が重要であることを示唆しています。しかし、PFSは同等である一方でOSで延長が認められた原因はまだ明らかではなく、後治療についても考える必要があります。
非小細胞肺癌(NSCLC)において標準化学療法とGefitinibとを比較したNEJ002試験では、Gefitinib群がPFS中央値を2倍延長し、OSも良好でした7)。しかし、90%を超えるクロスオーバー率のもと検討した結果、OSはほぼ同様になりました8)。この結果から、完全にクロスオーバーして薬剤を投与すればOSは同様になる可能性があり、治療順序による影響は少ないと考えられます。
一方、PEAK試験でBev群が2nd-lineで抗EGFR抗体薬を使用した症例は31%であり、FIRE-3試験では42.9%です (表3)。つまりBev群では多くの症例が抗EGFR抗体薬を投与する機会を逸しており、これが非常に重要なポイントになっています。
最後に、私に継続した癌治療の重要性を教えてくれた症例を紹介したいと思います。36歳の女性で、KRAS 野生型のS状結腸癌です。肝臓や卵巣への転移を認め、腹部膨満をきたしたグループ2の症例です。FOLFOX + Cetuximabを6サイクル施行したところ良好な腫瘍縮小が得られたので、原発巣と卵巣転移を切除し、患者の希望によりストーマの閉鎖を行いました。その後、FOLFOX + Cetuximabを再導入しましたが多数の切除不能な肝転移や肺転移を認め、患者と話し合いながら、L-OHPの再導入を含むBev併用療法、Cetuximabの再導入とCPT-IIの使用等、適宜治療を変更し、最終的には診断から3年後に亡くなりました。
この症例は、抗EGFR抗体薬などの効果的な初期治療を行うことでグループ2がグループ3になる可能性があること、そして継続した治療のなかで有効である薬剤を使い切ることの重要性を教えてくれました。PEAK試験やFIRE-3試験の結果は、KRAS 野生型の患者に対して抗EGFR抗体薬を1st-lineとして使用する強力なエビデンスであり、当該患者に対して使用する機会を逃してはいけないと考えています。