背景と目的
ミスマッチ修復機構の欠損 (deficient mismatch repair: dMMR) を有する癌は、大腸癌をはじめとする固形癌でしばしば認められ、マイクロサテライト不安定性を引き起こすことから、多くのneoantigenを有することが知られている。そのため、dMMRを有する癌に対し免疫チェックポイント阻害剤の効果が期待できるのではないかという仮説のもと本試験を行った。
対象と方法
dMMRを有する大腸癌 (コホートA)、MMR欠損のない (proficient mismatch repair: pMMR) 大腸癌 (コホートB)、dMMRを有する大腸癌以外の固形癌 (コホートC) の3群に分けて患者が登録され、抗PD-1抗体薬Pembrolizumab (10mg/kg, 2週毎) による治療が行われた。なお、MMRの判定には標準的なPCR-basedのマイクロサテライト不安定性検査が用いられた。
主要評価項目はimmune-related response criteria (irRC) に基づく奏効率、ならびに20週時点でのPFSであった。
結果
コホートA (13例)、コホートB (25例)、コホートC (10例) のほとんどが2レジメン以上の前治療歴を有していた。また、コホートAの85%がリンチ症候群であり、コホートCは胆道癌 (4例)、子宮内膜癌 (2例)、小腸癌 (2例)、前立腺癌 (1例)、胃癌 (1例) であった。
奏効率はコホートA 62%、コホートB 0%、コホートC 60%であり、コホートAとコホートCで主要評価項目を達成した。また、病勢コントロール率はコホートA 92%、コホートB 16%、コホートC 70%であった。
図1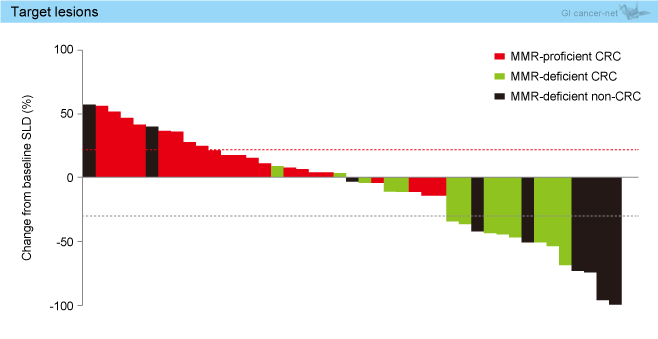
図2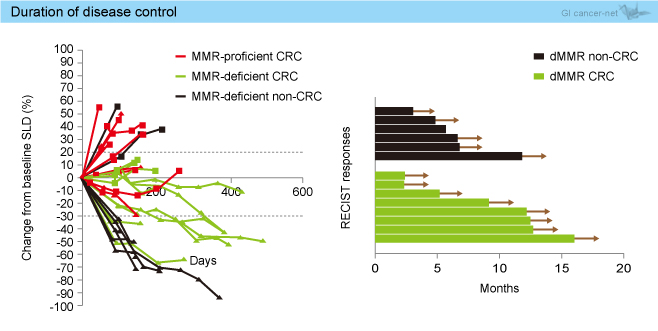
PFS中央値は、コホートA未到達、コホートB 2.3ヵ月であった (図3)。
図3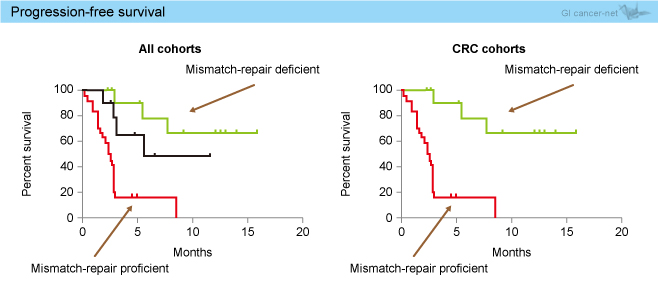
全コホートにおける有害事象は、膵炎 (15%)、内分泌障害 (12%)、皮疹 (17%) などを認めた。
なお、病理組織学的評価において、dMMRはpMMRと比較してinvasive frontでのCD8陽性T細胞数やPD-L1発現が高い傾向にあった。また、全エクソン解析において、dMMRの体細胞遺伝子変異数は、pMMRと比較して有意に多かった (p=0.007)。
結論
dMMRを有する固形癌に対するPembrolizumabの有効性が示唆された。なお、その臨床効果を確認するため、MSI陽性大腸癌を対象としたPembrolizumabの国際共同第II相試験 (KEYNOTE-164) が計画中である。
コメント
抗PD-1抗体薬Pembrolizumabは、PD-1とそのリガンドであるPD-L1、PD-L2との結合を阻害するヒト化モノクローナル抗体薬である。本報告結果は、PD-1経路が介在する抗腫瘍免疫応答の阻害の解除が癌増殖を阻止抑制することを臨床的に明らかにし、免疫治療戦略が現実的に期待できるものとなった。今後実臨床導入への開発展開が急速に進むであろう。確かに恩恵を受ける大腸癌患者は限られたものであるが、分子生物学から発展した現在の薬剤開発コンセプトが正しい方向であることを裏付け、今後の開発進歩を勇気付ける内容であった。
本剤は、昨年10月に米国FDAにより、EGFR 遺伝子変異陰性およびALK 融合遺伝子変異陰性で、プラチナ製剤ベースの化学療法を施行中または施行後に進行した非小細胞肺癌 (NSCLC) に対して画期的治療薬に指定された。Pembrolizumabの画期的治療薬の指定はメラノーマに続き2件目であり、その分本報告の注目度は高かった。加えて、LBAとしてabstractは前日まで公表されず、さらに同日にNew England Journal of Medicine誌公開という取り扱いであった。今年の米国臨床腫瘍学会年次集会における実質的な初日の第1演題報告は、拍手喝采で受け入れられていた。
(レポート:谷口 浩也 監修・コメント:佐藤 温)


