|
|
BRiTEは米国49の州で行われた巨大な前向きコホート研究で、2004年2月〜2005年6月の間に一次治療としてBevacizumabを含む治療を受け、インフォームドコンセントが得られた切除不能進行・再発大腸癌患者1,953例を対象とした (表2)。これら一次治療を受けた登録患者のうち、臨床的もしくは画像にてPD (progressive disease) と医師によって診断された1,445例が、PDが確認された後にBevacizumabを含む治療を受けた群 (BBP)、Bevacizumabを含まない治療群 (no BBP)、および無治療群の3群に分けられ、比較がなされた。BRiTEの結果はASCO 2007で報告され3)、翌2008年のJournal of Clinical Oncologyに掲載された (Grothey A, et al.: J Clin Oncol. 26(33): 5326-5334, 2008) 4)。
 BBP (Bevacizumab beyond progression)
BBP (Bevacizumab beyond progression)
BRiTEは観察研究であるため、二次治療としては「Bevacizumabを含む治療が行われたか否か、無治療であるかどうか」のみについて調査がなされ、後治療のレジメンの規定はされていない。主要評価項目としては、最初にPDが確認された時点から死亡までのsurvival beyond progression (SBP) が用いられている。追跡期間中央値が19.6ヵ月となった2007年1月における調査では、二次治療がなされなかった無治療群が253例、no BBP群が531例、BBP群が642例であった。BBP群とno BBP群の間には背景要因の差はほとんど認められなかったが、ECOG PSが1以上の症例が BBP群においてやや少ない傾向が認められている (PD後無治療群=54.6%、no BBP群=51.6%、BBP群=42.5%)。
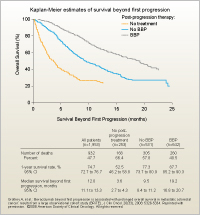
Kaplan-Meier曲線によるSBPの比較では、1年生存率で無治療群52.5%、no BBP群77.3%、BBP群87.7%であり、SBPの中央値でみても無治療群3.6ヵ月、no BBP群9.5ヵ月、BBP群19.2ヵ月と、いずれもPD後のさらなるBevacizumabによる治療が予後の改善に寄与することが示された (図2)。
また、immortal time biasの影響を考慮した解析では、2ヵ月以内にPD後治療が開始された症例に絞り込んで、no BBP群447例とBBP群477例の両群間で比較が行われている。このSBP中央値の比較検証の結果でも、no BBP群9.2ヵ月 (95% CI: 8.3-11.2ヵ月)、BBP群16.8ヵ月 (95% CI: 14.7-19.6ヵ月) と、BBPが生存延長をもたらしていることが明らかにされた。
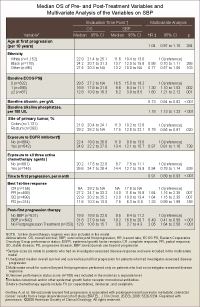
さらにこれらのデータについて多変量解析を行った結果でも、no BBPのハザードを1とした場合のBBPのハザード比は0.49 (95% CI: 0.41-0.58, p<0.001) と、PD後にもBevacizumab治療を行うことが効果をもたらすことが示されている (表3)。
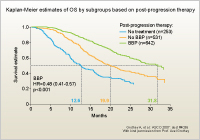
乳癌などの一部の癌種を除き、通常の抗癌治療においては、PDが確認された後には一次治療で用いられた治療法は適用されないことが臨床腫瘍学の常識となっているが、今回のBRiTEの結果は、たとえ一次治療でBevacizumabを含むレジメンの効果がなくなりPDとなった後でも、次のレジメンにさらにBevacizumabを加えることが予後を改善する可能性を示唆したものであり、画期的な知見であるといえる。ただし、2007年のASCOで最初に発表されたBBP群のOSが31.8ヵ月という衝撃的な予後の改善であったため、本論文には掲載されていないこのASCOでのKaplan-Meier曲線 (図3) が独り歩きし3)、過剰な期待とコンセンサスを形成してしまったという点については、試験全体をしっかりと理解したうえで正しい評価をすべきであろう。
 BRiTEを読み解くうえで注意すべき点
BRiTEを読み解くうえで注意すべき点
観察研究がエビデンスレベルの観点からみてRCTに比べて信頼性がやや落ちることは、当然のこととされている。BRiTEにおいては、この問題に対する批判に答えるために、多変量解析、sensitivity analysisなどの生物統計学的手法を駆使して、背景要因の相違によるバイアスを調整したり、腫瘍部位による特定の傾向を検証したり、Bevacizumabと化学療法の治療パターンの多様性がBBPの生存に及ぼす効果なども評価したりしている。BRiTEにおいては、これら全ての考えうる限りの観察研究の問題点について統計学的解析や検討を行ったうえで、BBPがno BBPに対して優れた予後改善効果があると結論づけているわけである。したがって、観察研究としては、prospectiveであることも含め、最も洗練された試験であるといえよう。
ただし、これらのmodel based analysisに関する多大な配慮が払われているにもかかわらず、観察研究自体のもっている限界を超えた新しい次元の解析と解釈が得られているとはいい難い。明らかな問題点をあげるとすれば、いわゆる“Confounding by indication (適応による交絡)” と呼ばれるバイアスが入ってしまっていることである。すなわち、PD後の治療方針が各現場の医師達に任されているため、Bevacizumabによる治療ができるという患者群とBevacizumabによる治療が不可能と判断された患者群の間には、担当医しか評価できない患者背景の差があると考えるべきである。
先にBBPの項で述べたように、ベースライン (2007年1月時点) の患者背景でBBP群においてPSが良好な症例が多いことから、前治療の効果が各群間で異なっている可能性が高い。さらにbest first responseもBBP群が良好であることから推測するに、BBP群は治療が効きやすい集団であるということができる。このBBP群が何らかの条件で選択される可能性が高いものであるならば、このBRiTEの結果からは、PD後に使用されたBevacizumabのおかげで予後がよいのか、医師が予後良好と思われる患者群を選択してBBP群になっているのかの区別はつかない。BRiTEで不十分な部分は、一次治療から二次治療に移行する時点での因子で充分な調整が行われていない可能性が高い。したがって今回の解析では、本来はできる限りBevacizumabを選択する理由となった因子で調整すべきであったといえる。もちろん、このBRiTEではさまざまな解析を付加することによって、この問題についても対策がなされているとは思われるが、RCTに代表される検証的なdesign based analysisに対して、探索的なmodel based analysisにはある程度の限界があることを熟知しておかなければならない。
過去の例をあげると、エストロゲン仮説に基づいて、高用量のエストロゲンを投与することによって心筋梗塞のリスクを低下させうるhormone replacement therapy (HRT) の可能性について検討した16年にもわたる大規模コホート観察研究であるNurses’ Health Studyでは、HRTが心筋梗塞リスクを下げる5)との結論が示されたにもかかわらず、その後実施されたWomen’s Health Initiativeの大規模RCTにおいて、HRTは心筋梗塞リスクを高めるという逆の結果が示されている6)。この違いは、ランダム化がなされていない研究では、社会的な背景の差や治療に対するアドヒアランス (コンプライアンス) の差によるバイアスを除くことが難しいこと、さらには「より心血管リスクの少ない患者にHRTを行う」という医師の裁量の差によるバイアスの可能性など、観察研究の弱点を示したものとしてよく知られている。
BRiTEがきわめて洗練された観察研究であることについての異論はないが、Journal of Clinical OncologyのようなQuality Journalに掲載されたからといって、無批判にその結果を盲信したり、即ガイドラインへの記載を検討したりすることは誤りである。これはこのBBPの再現性をみたARIESの結果7)についても同様のcriticalな視点をもつことが必要であり、きっちりとした介入研究 (大規模RCT) の結果とは一線を画した判断をおくべきであることを忘れてはいけない。現在、AIO0504 (ML18147) 試験8)によりBBPに関する検証を目的としたRCTが進められており、この臨床比較対照試験によって、BBPの真の意義と位置づけが明らかになるものと期待されている。
 |