Abstract #660
RAS 野生型切除不能進行・再発大腸癌に対する1st-lineとしてのmFOLFOX6 + PanitumumabまたはBevacizumab:RECISTを越えた腫瘍縮小効果
First-line Treatment with Modified FOLFOX6 (mFOLFOX6) + Panitumumab or Bevacizumab in Wild-type RAS Metastatic Colorectal Carcinoma: Tumor Response Outcomes Beyond RECIST
Fernando Rivera, et al.
1st-lineにおける抗EGFR抗体薬とBevacizumabの比較に答えは?
PEAK試験の対象症例を
RAS 野生型に絞ってDpR (deepness of response)、ETS (early tumor shrinkage) に関して解析した結果である。臨床試験における抗腫瘍効果を判定する指標であるRECISTでは奏効率において両群間に有意差はないものの、“真のエンドポイント”であるOSにおいてPanitumumab群はBevacizumab群に対して有意な延長を認めた。一般的に進行・再発大腸癌に対する1st-lineにおいてPFSがOSをサロゲートするとされているが、本試験と同様にBevacizumabと抗EGFR抗体薬を比較した
FIRE-3試験ではCetuximab群でOSのみの延長がみられている。Bevacizumab vs. 抗EGFR抗体薬の1st-lineにおける抗EGFR抗体薬の優越性を検証した試験として、
FIRE-3試験、
PEAK試験、CALGB 80405試験 (主要評価項目はOS) の3試験が行われたが、いずれにおいても主要評価項目では優越性は証明されていない。
PEAK試験、
FIRE-3試験においてはOSで抗EGFR抗体薬の優越性が認められており、その理由についてETS、DpRの指標が挙げられ、より早く、より縮小することがOSの延長につながるという意見もあるが、これら3つの試験においては2nd-line以降の治療が規定されていない。したがって、現時点では、
RAS 野生型の1st-lineにおける分子標的薬をBevacizumabあるいは抗EGFR抗体薬にするかは、各症例に応じて決定していくことが必要である。
背景と目的
切除不能進行・再発大腸癌に対する1st-lineとしてのmFOLFOX6 + Panitumumab (Panitumumab群) とmFOLFOX6 + Bevacizumab (Bevacizumab群) を比較した
PEAK試験では、
RAS 野生型 (
KRAS /
NRAS exon 2、3、4に変異なし) 症例において、Panitumumab群はBevacizumab群に比べPFSおよびOSを有意に延長することが報告されているが、RECISTに基づく奏効率は両群に差はみられなかった
1) 。一方で、近年の報告では1st-lineの長期予後には奏効の深さと期間などが影響を与えていることが示唆され
2, 3) 、早期で、深く、維持期間の長い腫瘍縮小は、症状緩和や切除機会の改善などの臨床的ベネフィットをもたらすと考えられている。
本研究ではPEAK試験の探索的解析として、ETS (early tumor shrinkage)、DpR (deepness of response)、腫瘍量などの腫瘍動態や、CEA値の変化ついて評価した。
対象と方法
PEAK試験の対象は、前治療を行っていない
KRAS exon 2野生型の切除不能進行・再発大腸癌であり、本解析では
RAS 野生型170例を解析対象とし、奏効率 (治験担当医師評価)、DoR (depth and duration of response、初回奏効から病勢進行もしくは死亡までの期間)、TTR (time to response、無作為化から初回奏効までの期間)、DpR (腫瘍縮小を認めた場合は最縮小時、認めなかった場合はPD時におけるベースラインからの腫瘍縮小率)、CEA値 (ベースラインからの変化率)、ETS (8週時点での腫瘍縮小率が20%以上もしくは30%以上) などについて評価した。
結果
対象の患者背景は両群でほぼ同等であったが、標的病変の最長径和平均値はPanitumumab群129.0mm、Bevacizumab群108.6mm、CEA中央値はそれぞれ12.8μg/L、14.7μg/Lであった。
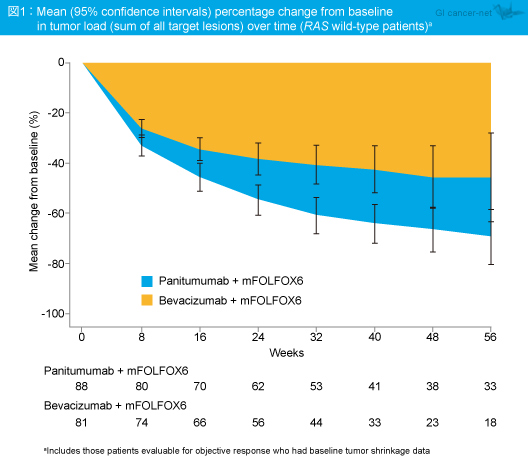
抗腫瘍効果の検討では、CRをPanitumumab群3例 (3.4%)、Bevacizumab群1例 (1.2%) で認め、奏効率はそれぞれ57%、50%であった。TTR中央値はPanitumumab群2.3ヵ月、Bevacizumab群3.8ヵ月とPanitumumab群で短い傾向がみられ (HR=0.85, 95% CI: 0.58-1.25, p=0.4090)、DoR中央値はそれぞれ11.4ヵ月、8.5ヵ月とPanitumumab群で有意に長く (p=0.0159)、DpR中央値もそれぞれ65%、46%とPanitumumab群で有意に良好であった (p=0.0007)。なお、腫瘍量 (標的病変の最長径和) の経時的な変化率は図1の通りであり、いずれの時点においてもPanitumumab群で良好であった。
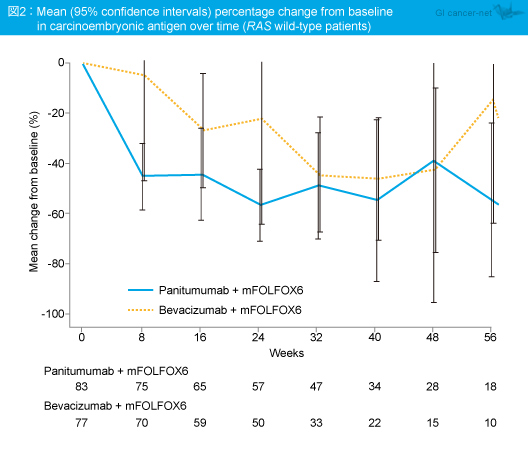
CEA値の変化率は測定時点のほとんどにおいてPanitumumab群で良好であり、75%以上の低下を認めた患者はPanitumumab群55.6%、Bevacizumab群46.6%であった (OR=0.70, 95% CI: 0.35-1.38) (図2)。
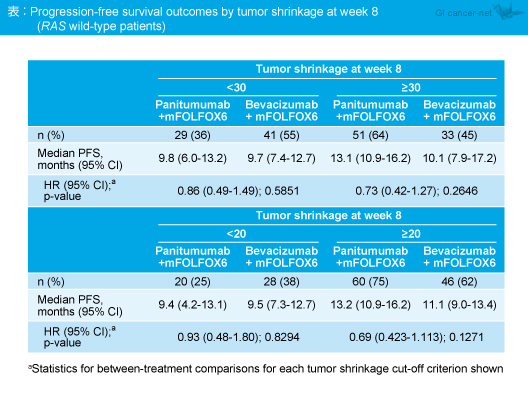
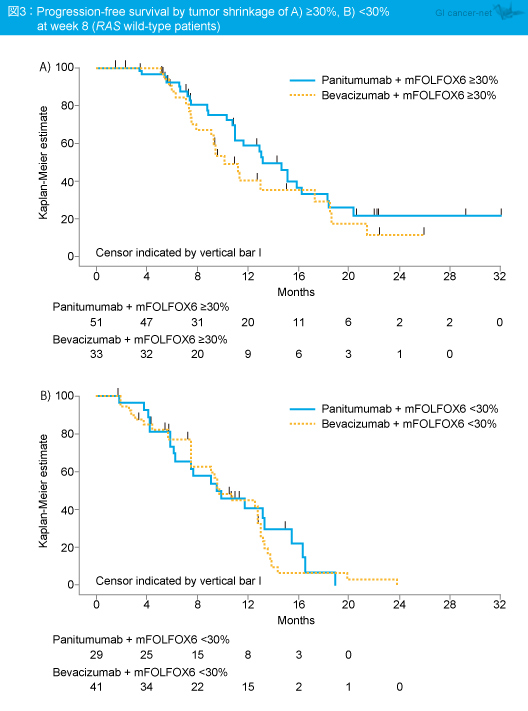
ETSを達成した症例は、ETSのカットオフ値30%以上ではPanitumumab群で有意に多く (OR=0.46, 95% CI: 0.23-0.92, p=0.0259)、ETSのカットオフ値20%以上においてもPanitumumab群で多い傾向がみられた (OR=0.55, 95% CI: 0.26-1.15, p=0.1223) 。ETS達成の有無別にPFSを比較した結果、カットオフ値30%以上 (HR=0.73, 95% CI: 0.42-1.27, p=0.2646)、20%以上 (HR=0.69, 95% CI: 0.423-1.113, p=0.1271) のいずれもPanitumumab群はBevacizumab群に比べてETS達成例におけるPFSが良好な傾向がみられた (表、図3)。
なお、治療群を統合してETS 達成別にPFSを比較すると、ETS30%以上の症例12.8ヵ月、ETS30%未満の症例9.7ヵ月 (HR=0.54、95% CI: 0.36-0.80, p=0.0019)、ETS20%以上の症例12.9ヵ月、ETS20%未満の症例9.4ヵ月 (HR=0.50, 95% CI: 0.34-0.75, p=0.0008) と、いずれもETSを達成した症例が有意に良好であった。
切除率はPanitumumab群13%、Bevacizumab群11%、完全切除率は両群とも9%、切除までの期間中央値はそれぞれ4.9ヵ月、4.4ヵ月であり、差はみられなかった。なお、6ヵ月PFSは切除例でPanitumumab群82%、Bevacizumab群67%、非切除例でそれぞれ73%、68%であった。
結論
Panitumumab群はBevacizumab群に比べ、早期かつ長期に、より深い奏効が得られることが明らかとなった。これらの結果は臨床的ベネフィットをもたらすと考えられ、PEAK試験におけるPFSおよびOSの結果を理解する上で重要であると考えられる。また、同様に1st-lineにおける抗EGFR抗体薬とBevacizumabを比較したFIRE-3試験3, 4) の結果と一貫していた。
Reference
1) Schwartzberg LS, et al. J Clin Oncol. 32(21) : 2240-2247, 2014[
PubMed]
2) Mansmann UR, et al.: 2013 Gastrointestinal Cancers Symposium: abst #427
3) Heinemann V, et al.: 2014 WCGC: abst #O-0030
4) Stintzing S, et al.: 2014 Gastrointestinal Cancers Symposium: abst #445[
学会レポート]