|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。
|

PEAK試験:KRAS 野生型の切除不能進行・再発大腸癌患者に対する1st-lineにおけるmFOLFOX6 + PanitumumabとmFOLFOX6 + Bevacizumabの無作為化比較第II相試験
PEAK (Study 20070509) : A Randomized Phase 2 Study of mFOLFOX6 With Either Panitumumab or Bevacizumab as 1st-line Treatment in Patients With Unresectable Wild-Type (WT) KRAS Metastatic Colorectal Cancer (mCRC)
Lee S. Schwartzberg, et al.

1st-lineにおける至適な分子標的治療薬とは?
〜PEAK試験から垣間見えるもの〜
〜PEAK試験から垣間見えるもの〜

結果、PFS、OS (overall survival) 、奏効率はいずれもPanitumumab群が若干良好な結果ではあるものの、Bevacizumab群との間に明らかな相違は認められなかった。安全性に関しては、皮疹、下痢、粘膜炎、低マグネシウム血症はPanitumumab群に、高血圧はBevacizumab群に多い傾向を認めたが、致死的有害事象に差はなかった。
本試験は、もとより無作為化第II相試験であり、検証的な結論は導き出せない。また、OSの結果は、後半のKaplan-Meier曲線の開きとHR=0.72だけ見るとPanitumumab群が良好な結果のように見えるが、明らかに観察期間が短いimmatureなdataであり、慎重に解釈する必要がある。それでも、フルに治療した場合、3rd-lineまで可能なBevacizumab群と2nd-lineまでしかないPanitumumab群では有効性に差がないこと、また、サブグループ解析ではLDH高値や転移臓器個数の多い対象でPanitumumab群が良好なPFS、OSを示し、75歳以上の高齢者ではBevacizumab群が良好であった結果などは、今後の実地臨床への応用に役立つものと考える。いずれにせよ、検証的な試験としてCALGB80405試験やFIRE-3試験 (いずれも2013年 米国臨床腫瘍学会年次集会 で公表予定) の結果が待望される。
Panitumumab (Pmab) は1st-lineとしてPmab + FOLFOX4療法とFOLFOX4単独療法とを比較する第III相試験 (PRIME試験) において、KRAS 野生型の切除不能進行・再発大腸癌患者のPFSを有意に改善することが示されている。今回、未治療のKRAS 野生型の切除不能進行・再発大腸癌を対象としたPmab + mFOLFOX6とBev + mFOLFOX6を比較した、多施設共同無作為化比較第II相試験PEAKの結果を紹介する。
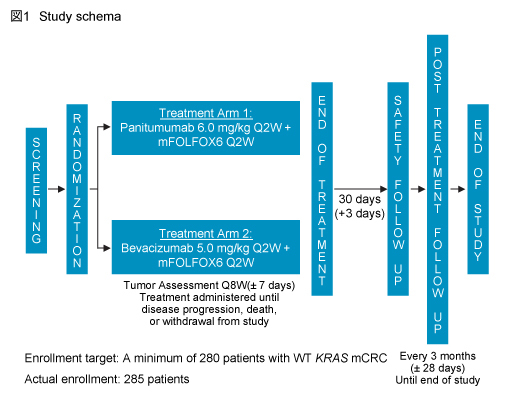
患者をPmab (6.0mg/kg) + mFOLFOX6を2週毎投与 (Pmab群) とBev (5.0mg/kg) + mFOLFOX6を2週毎投与 (Bev群) とに1:1の割合で無作為に割り付けた (図1) 。患者の適格基準は、KRAS 野生型、ECOG PS ≦1で、化学療法、抗VEGF抗体薬、抗EGFR抗体薬による治療を行っていない切除不能進行・再発大腸癌患者である。
主要評価項目はPFS、副次評価項目はOS、奏効率、安全性であった。
主要評価項目はPFS、副次評価項目はOS、奏効率、安全性であった。
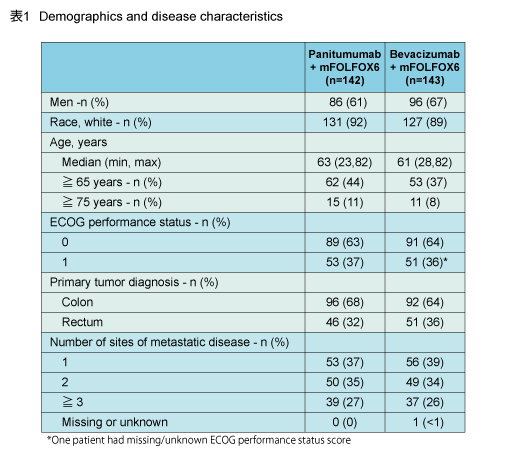
KRAS 野生型の切除不能進行・再発大腸癌患者285例のうち、治療が施行された278例が割り付けられた。両群間の患者背景に差はなかった (表1) 。
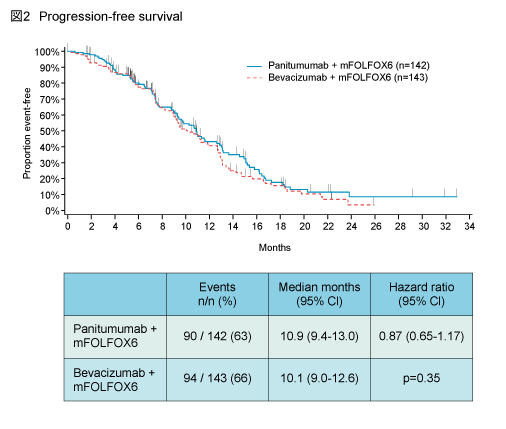
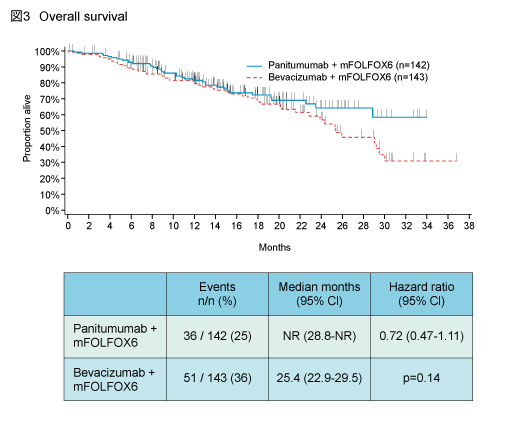
主要評価項目であるPFS中央値は、Pmab群10.9ヵ月 (95% CI: 9.4-13.0) 、Bev群10.1ヵ月 (95% CI: 9.0-12.6) であった (HR=0.87, 95% CI: 0.65-1.17, p=0.35) (図2) 。副次評価項目であるOS中央値は、Pmab群未到達 (95% CI: 28.8-NR) 、Bev群25.4ヵ月 (95% CI: 22.9-29.5) であった (HR=0.72, 95% CI: 0.47-1.11, p=0.14) (図3) 。また、奏効率はPmab群58%、Bev群54%であった。
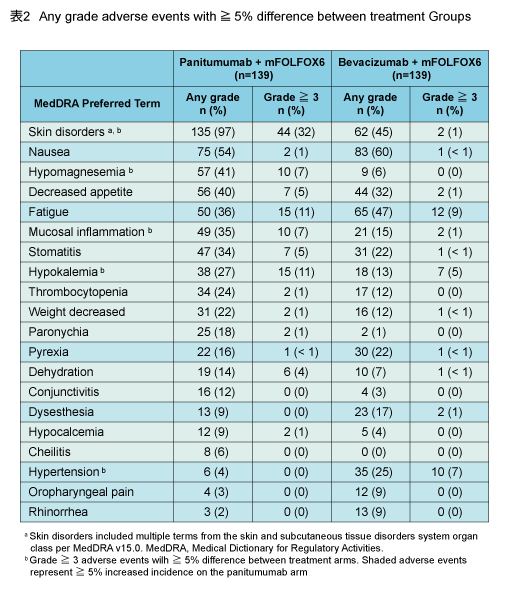
Grade 3/4の有害事象の発現頻度はPmab群86%、Bev群76%であった。Grade 5 (死亡) の発現頻度はPmab群5%、Bev群6%であった。Grade 3以上で両群間に5%以上の差がみられた有害事象は表2の通りである。いずれかの有害事象により治療を中断した症例は、Pmab群24%、Bev群27%であった。
未治療のKRAS 野生型の切除不能進行・再発大腸癌に対する今回の試験において、PFS (HR=0.87) 、OS (HR=0.72) 、奏効率 (58% vs. 54%) は、いずれもPmab群が良好な傾向にあったものの、有意差は認められなかった。また、継続治療は比較的バランスがとれていた。
Pmab群の安全性プロファイルは、抗EGFR抗体薬のclass effectとして知られているものであり、Pmab群において発現率の高いgrade 3/4および重篤な有害事象は、抗EGFR抗体薬のclass effectとして知られているものであった。また、有害事象による治療中断率は両群で同等で、新たな安全性の徴候は確認されなかった。
Pmab群の安全性プロファイルは、抗EGFR抗体薬のclass effectとして知られているものであり、Pmab群において発現率の高いgrade 3/4および重篤な有害事象は、抗EGFR抗体薬のclass effectとして知られているものであった。また、有害事象による治療中断率は両群で同等で、新たな安全性の徴候は確認されなかった。
