|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。
|

切除不能進行・再発大腸癌におけるPanitumumabの有効性と安全性に関するレトロスペクティブ・コホート試験: HGCSG 1002試験 〜臨床におけるPanitumumab投与早期の効果予測因子に関する解析結果〜
Retrospective Cohort Study on the Safety and Efficacy of Panitumumab for Metastatic Colorectal Cancer Patients: HGCSG1002 -Analysis of Clinical Early Predictor for the Efficacy-
Susumu Sogabe, et al.

日常臨床におけるPanitumumab投与に関して詳細検討の結果報告 -
3rd-lineにおいてCEAは治療早期の効果予測因子になり得るか?
3rd-lineにおいてCEAは治療早期の効果予測因子になり得るか?

Sogabeらは3rd-line以降にPmabを使用した症例 (n=67) を対象に、Pmabの早期効果予測因子の探索を行い、報告した。抗EGFR抗体薬投与後の効果予測因子としては皮膚障害1) が代表的であるが、Cetuximabに関しては早期の血清マグネシウム値の低下が効果予測因子として期待されるとの報告もなされている2)。
今回の報告では血清マグネシウム値に加え、CEA、CA19-9、血清アルブミン値、血清カルシウム値に関して効果予測因子としての有効性を評価しているが、早期 (治療開始4週) の効果予測因子として有望なのはCEAのみであった。しかし、残念ながら腫瘍マーカーの測定は保険収載上、月1回となるため、実臨床においてさらに早期の評価は困難である。
やはり治療開始前に評価可能な有望な効果予測因子が必要である。現在はKRAS 遺伝子変異検索が唯一の効果予測因子であるが、KRAS 野生型の症例においても無効例は少なからず存在しており、今後はKRAS 遺伝子以外の明確なバイオマーカーの出現が望まれる。現在、網羅的遺伝子解析手法を用いたバイオマーカー検討 (BREAC試験) なども行われており、有望な効果予測因子の出現を期待したい。
EGFR経路の阻害は大腸癌治療において重要な要素であるが、抗EGFR抗体薬を投与した際に効果を示す患者群は限られている1, 3, 4)。これまで、抗EGFR抗体薬の投与早期における臨床的効果予測因子に関する研究がいくつか報告されていることから2)、今回、Pmab治療開始早期におけるMg2+、Ca2+、アルブミン (Alb) 、 CEA、CA19-9の血清濃度の低下が、OS (overall survival) やPFS (progression-free survival) を予測する因子になるかを探索した。
HGCSG 1002試験では、2010年6月〜2011年10月に20施設で治療された症例のうち、20歳以上で病理学的検査においてKRAS 野生型大腸癌と確認され、Pmabを含む化学療法を実施した200例を対象とし、Mg2+、Ca2+、Alb、CEA、CA19-9の血清濃度をもとに解析を行った。
なお、腫瘍効果はRECIST ver.1.1、PFS / OSはKaplan-Meier method用いて評価し、奏効率 / 病勢コントロール率はFisher's exact test、PFS / OSはlog-rank testを用いて統計解析を実施した。
なお、腫瘍効果はRECIST ver.1.1、PFS / OSはKaplan-Meier method用いて評価し、奏効率 / 病勢コントロール率はFisher's exact test、PFS / OSはlog-rank testを用いて統計解析を実施した。
HGCSG 1002試験に登録された200例のうち5-FU / CPT-11 / L-OHP不応となった症例は142例であり、そのうち抗EGFR抗体薬未治療患者67例を解析した。
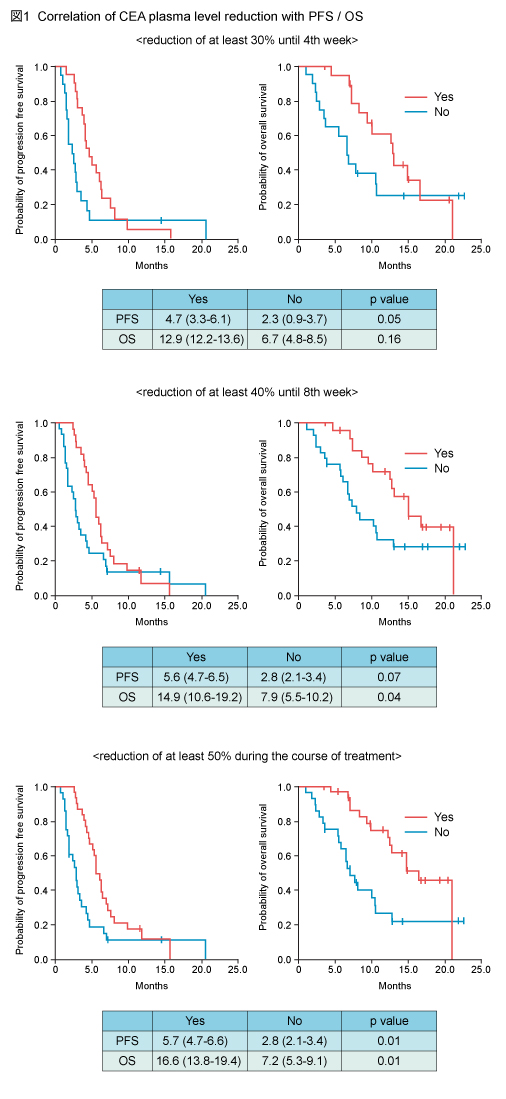
Pmab治療開始後4週目までに血清CEA値低下≧30%例ではPFS中央値が4.7ヵ月と、<30%例 (2.3ヵ月) に比べて有意に高く (p=0.05) 、OS中央値もそれぞれ12.9ヵ月、6.7ヵ月と (p=0.16) 、血清CEA値低下例で延長する傾向を認めた (図1上) 。治療開始後8週目までの血清CEA値低下≧40%例でも同様の傾向がみられ (図1中) 、治療期間中の血清CEA値低下≧50%の有無により、PFS中央値は5.7ヵ月 vs. 2.8ヵ月 (p=0.01) 、OS中央値は16.6ヵ月 vs. 7.2ヵ月 (p=0.01) と、ともに有意差が認められた (図1下) 。
Pmab治療開始後4週目までに血清CEA値低下≧30%例ではPFS中央値が4.7ヵ月と、<30%例 (2.3ヵ月) に比べて有意に高く (p=0.05) 、OS中央値もそれぞれ12.9ヵ月、6.7ヵ月と (p=0.16) 、血清CEA値低下例で延長する傾向を認めた (図1上) 。治療開始後8週目までの血清CEA値低下≧40%例でも同様の傾向がみられ (図1中) 、治療期間中の血清CEA値低下≧50%の有無により、PFS中央値は5.7ヵ月 vs. 2.8ヵ月 (p=0.01) 、OS中央値は16.6ヵ月 vs. 7.2ヵ月 (p=0.01) と、ともに有意差が認められた (図1下) 。
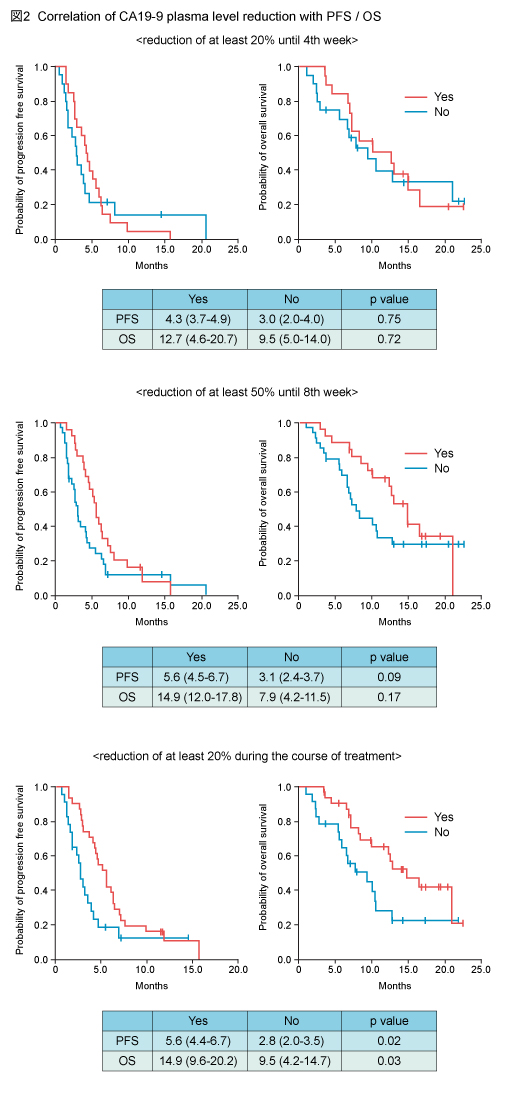
また、血清CA19-9値は、治療開始後4週目までの≧20%低下例、および8週目までの≧50%低下例において良好な傾向がみられ、治療期間中の≧20%低下例では、<20%低下例に対してPFS (p=0.02) 、OS (p=0.03) ともに有意な延長が認められた (図2) 。
一方、治療開始早期のMg2+、Ca2+、Albの血清濃度低下については、PFS、OSとの関連性は認められなかった。
切除不能進行・再発大腸癌患者に対するPmab治療開始早期の血清CEA値≧30%低下は、PFSとOSにおける効果予測因子となることが示唆された。一方、Ca2+、Albにおいては、PFSやOSとの関連性はみられなかった。
なお、Pmab投与期間中の低マグネシウム血症とPFS / OSとの関連性がこれまで報告されているが、本研究においてPmab治療開始早期の血清Mg2+濃度低下はPFS/OSの予測因子とならなかった。
なお、Pmab投与期間中の低マグネシウム血症とPFS / OSとの関連性がこれまで報告されているが、本研究においてPmab治療開始早期の血清Mg2+濃度低下はPFS/OSの予測因子とならなかった。
Reference
1) van Cutsem E, et al.: J Clin Oncol. 25(13): 1658-1664, 2007 [PubMed]
2) Vincenzi B, et al.: Ann Oncol. 22(5): 1141-1146, 2011 [PubMed]
3) Cunningham D, et al.: N Engl J Med. 351(4): 337-345, 2004 [PubMed]
4) Peeters M, et al.: J Clin Oncol. 28(31): 4706-4713, 2010 [PubMed]
1) van Cutsem E, et al.: J Clin Oncol. 25(13): 1658-1664, 2007 [PubMed]
2) Vincenzi B, et al.: Ann Oncol. 22(5): 1141-1146, 2011 [PubMed]
3) Cunningham D, et al.: N Engl J Med. 351(4): 337-345, 2004 [PubMed]
4) Peeters M, et al.: J Clin Oncol. 28(31): 4706-4713, 2010 [PubMed]
関連リンク
・GI pedia 第3回「大腸癌のバイオマーカー」
・2013年 消化器癌シンポジウム abst #541 「切除不能進行・再発大腸癌におけるPanitumumabの有効性と安全性に関するレトロスペクティブ・コホート試験: HGCSG 1002試験 〜Cetuximab不応患者に対するPanitumumabの有効性と安全性の解析結果〜」
・2013年 消化器癌シンポジウム abst #554 「切除不能進行・再発大腸癌におけるPanitumumabの有効性と安全性に関するレトロスペクティブ・コホート試験: HGCSG 1002試験 〜Panitumumabの有害事象に関する解析結果〜」
・GI pedia 第3回「大腸癌のバイオマーカー」
・2013年 消化器癌シンポジウム abst #541 「切除不能進行・再発大腸癌におけるPanitumumabの有効性と安全性に関するレトロスペクティブ・コホート試験: HGCSG 1002試験 〜Cetuximab不応患者に対するPanitumumabの有効性と安全性の解析結果〜」
・2013年 消化器癌シンポジウム abst #554 「切除不能進行・再発大腸癌におけるPanitumumabの有効性と安全性に関するレトロスペクティブ・コホート試験: HGCSG 1002試験 〜Panitumumabの有害事象に関する解析結果〜」
