|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。
|

切除不能進行・再発大腸癌におけるBevacizumab beyond progressionによる効果予測因子としての循環血管増殖因子: 第III相試験BEBYP試験からのtranslational analyses
Circulating Angiogenic Factors as Predictors of Benefit from Bevacizumab (bev) beyond Progression in Metastatic Colorectal Cancer (mCRC): Translational Analyses from the Phase III BEBYP trial.
Chiara Cremolini, et al.

血漿sVEGFR-2およびPlGF濃度は、BBP療法の効果予測因子である可能性が示唆された

本報告ではBBPの治療効果を示唆したBEBYP試験における血漿中バイオマーカー検索の結果として、1) 可溶性VEGFR-2 (sVEGFR-2) 高値の症例はBBPの治療効果がより高い、2) PlGF高値の症例はBBPの治療効果が高い、3) sVEGFR-2高値かつPlGF高値の症例はBBPの治療効果が最も高い (HR=0.25, p=0.0043)、ことを示している。
本報告のlimitationは、a) 59症例という少数例の報告である、b) 測定値のカットオフラインを中央値としているためか群間の症例数に偏りがある (sVEGFR-2高値例における化学療法群は18例だが化学療法 + Bev群は12例、PlGF低値例における化学療法群は20例だが化学療法 + Bev群は9例など) であり、また検索したその他のバイオマーカーについての報告がなされていない。しかし、今まで明らかになっていないBev併用療法のバイオマーカー「候補」が示された点で注目すべき報告である。
第III相試験であるML18147試験およびBEBYP試験は、切除不能進行・再発大腸癌における初回増悪後のBev継続投与の有効性を示した。また、化学療法 + Bevによる1st-line治療により、血管新生関連因子の血漿濃度に動的な変動が起こることが下記のように報告されている。
なお、演者らの研究グループにより、in vitroの試験によって血管新生阻害薬に対する耐性獲得は、PIGF、VEGFR-2、PDGF、Tie-2 などの血管新生関連遺伝子の発現の上昇に関連しており、マウスモデルにおけるin vivoデータによって、疾患増悪時と奏効時で同様の因子の組織や血漿濃度が増加していることが示されている。
| ・ | FOLFIRI + Bevにより治療された患者コホートにおいて、疾患の増悪が画像により評価される前にbFGF、HGFレベルが上昇することが示された1)。 |
| ・ | FOLFOXIRI + Bevにより治療された患者コホートにおいて、疾患増悪時にsVEGFR-2レベルが大きく変動することが観察された2)。 |
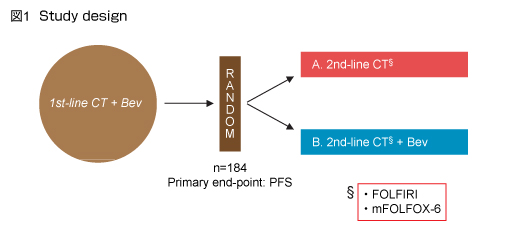
BEBYP試験 (Bevを含んだ1st-line治療で増悪した患者について、2nd-line治療として化学療法 ± Bevの有効性を比較した第III相試験:図1) に登録された59例において、初回増悪時点 (ベースライン時) および治療中に血漿を採取し、前臨床における知見を基にsVEGFR-2、PlGF、PDGF-C、bFGF、Ang-2、sTie-2などをELISA法により測定した。血漿レベルはカットオフ値として中央値を用い、高値、低値を定義した。
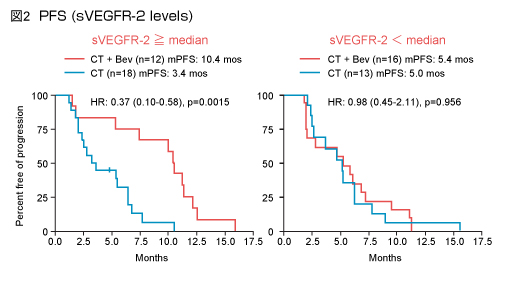
sVEGFR-2レベルが高値の症例におけるPFS中央値は化学療法 + Bev群10.4ヵ月、化学療法群3.4ヵ月とBevの継続投与による有意な延長を示したが (HR=0.37, 95% CI: 0.10-0.58, p=0.0015) 、sVEGFR-2レベル低値の症例においてはそれぞれ、5.4 ヵ月、5.0ヵ月であり、関連は認められなかった (HR=0.98, 95% CI: 0.45-2.11, p=0.956) (図2) 。また、治療アームとベースラインにおけるsVEGFR-2レベルとの間に有意な相関が確認された (p=0.036) 。
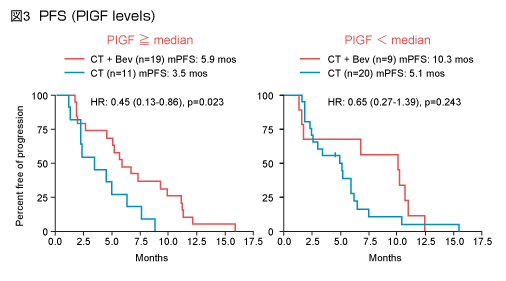
PlGFレベルが高値の症例においても、PFS中央値は化学療法 + Bev群5.9ヵ月、化学療法群3.5ヵ月と、Bevによる延長を示した (HR=0.45, 95% CI: 0.13-0.86, p=0.023) (図3) 。しかし、治療アームとベースラインにおけるPlGFレベルとの間に相関は認められなかった (p=0.210) 。
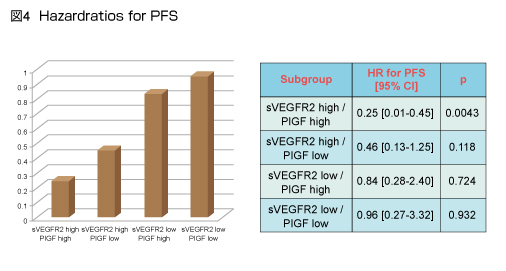
さらに、sVEGFR-2とPlGFとの統合解析により、増悪後のBev継続による治療効果が異なる4つのサブグループが確認され、sVEGFR-2およびPlGFレベルがともに高値の群ではBev継続投与により有意なbenefitを得られることが示された (HR=0.25, 95% CI: 0.01-0.45, p=0.0043) (図4) 。
初回増悪時点の血漿sVEGFR-2レベルはBevの継続投与による効果予測因子となることが期待される。また、sVEGFR-2とPlGFの統合解析は、増悪後におけるBevの継続投与によるbenefitを、より享受できるサブグループを確認するために有用な可能性がある。今回報告したサブグループ解析は、独立したコホートにおいて前向きに検証されることが望まれる。
