|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。
|

膵癌切除後の術後補助化学療法としてのGemcitabine vs. S-1の無作為化第III相試験: JASPAC-01試験
Randomized Phase III Trial of Adjuvant Chemotherapy with Gemcitabine vs. S-1 for Resected Pancreatic Cancer Patients (JASPAC-01 study)
Katsuhiko Uesaka, et al.

S-1は膵癌においても本邦の術後補助化学療法の標準に

膵癌の術後補助化学療法はCONKO-001試験のエビデンスに基づきGemcitabine (GEM) が標準であった。このCONKO-001試験におけるGEM群の3年DFS (disease-free survival) は23.5%であり、当試験でのGEM群もほぼ同様の成績を示しているが、そこからのHRが0.56と改善していることは驚嘆に値する結果である。また、膵癌手術は膵頭十二指腸切除と侵襲の大きい術式がとられるが、S-1群の65%がこの術式で切除を受けているなかで、毒性中止は21%と、むしろGEM群の25%より低く忍容性も担保されている。まさに、速やかに臨床導入をすべきといえるデータである。
S-1の良好な成績が報告されると、必ずと言っていいほどdiscussantから白人での忍容性を検証すべきという言葉が上がる。しかし本邦ではさらなる治療成績の向上のために、S-1 + αの補助化学療法の開発を目指すことが期待される。
膵癌切除後のGEMの術後補助化学療法によってDFSが有意に延長することがCONKO-001試験において示されており1)、このエビデンスに基づき、GEMは膵癌の術後補助化学療法の標準治療とされている。一方、本邦で行われたGEST試験では、切除不能進行膵癌の治療においてフッ化ピリミジン系経口薬であるS-1がGEMに対し非劣性であることが確認され2)、この知見により、S-1は日本における進行膵癌の標準治療の1つとなっている。
そこで、術後補助化学療法におけるGEMに対するS-1の非劣性を検証する多施設共同オープンラベル無作為化第III相試験 (JASPAC-01試験) が実施され、今回、中間解析の結果が報告された。
そこで、術後補助化学療法におけるGEMに対するS-1の非劣性を検証する多施設共同オープンラベル無作為化第III相試験 (JASPAC-01試験) が実施され、今回、中間解析の結果が報告された。
対象は、組織学的に浸潤性膵管腺癌であることが確認され、stage II以下および腹腔動脈合併切除されたstage IIIの膵癌患者であり、R0またはR1切除され、過去3年以内に化学療法や放射線療法を受けていないECOG PS 0/1の症例を、GEM 1,000mg/m2 (day1, 8, 15を4週毎) を6サイクル投与する群 (GEM群) と、S-1 40〜60/mg (bid, day1〜28を6週毎) を4サイクル投与する群 (S-1群) とに無作為に割り付けた (図) 。
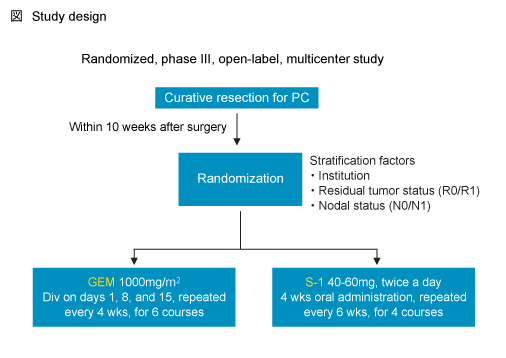
主要評価項目はOS (overall survival) とし、副次評価項目はRFS (relapse-free survival) 、有害事象、健康関連QOLであった。また、GEM群の3年OSを36%、S-1のHR期待値を0.87と仮定し、HRの非劣性マージンは1.25と設定した。必要なサンプルサイズは360例、検出力80%、有意水準は両側検定0.05であった。なお、180例が死亡した時点で中間解析を行うよう計画された。
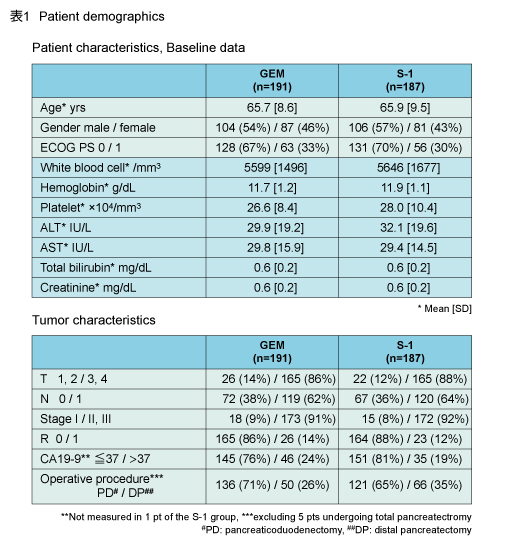
2007年4月〜2010年6月までに日本の33施設から登録された385例のうち、解析の対象となったのは378例であり、GEM群は191例、S-1群は187例であった。ベースライン時の患者背景は両群でよくバランスがとれていた (表1) 。なお、2012年7月までに得られた生存データの中間解析に基づき、独立データ監視委員会は速やかな結果の公表を勧告した。
主要評価項目であるOSの HRは0.56 (99.8% CI: 0.36-0.87, p<0.0001) と非劣性基準を満たすとともに、S-1群のGEM群に対する優越性も確認された (p<0.0001) 。なお、GEM群のOS中央値は25.5ヵ月と、CONKO-001試験の成績 (GEM群22.1ヵ月) と比べても遜色なく1)、2年OSはGEM群53%、S-1群70%であった。
また、RFS中央値はGEM群11.2ヵ月に対しS-1群23.2ヵ月であり、S-1群で有意な延長を認め (HR=0.56, 95% CI: 0.43-0.71, p<0.0001) 、2年RFSはそれぞれ29%、49%であった。
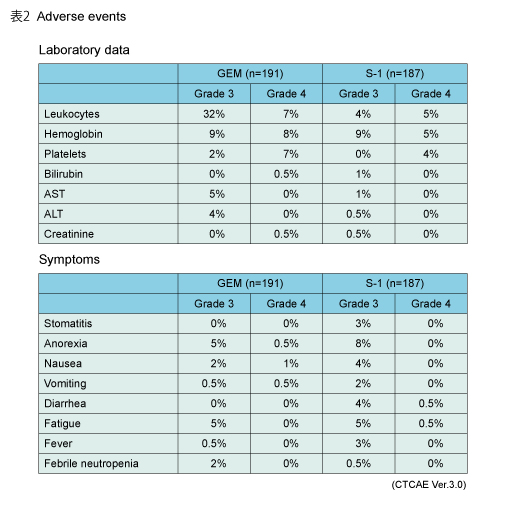
治療完遂率はGEM群58%、S-1群72%であった。治療中止理由は、再発がGEM群26例 (14%) 、S-1群9例 (5%) 、毒性がそれぞれ48例 (25%) 、40例 (21%) 、患者拒否が5例、3例、その他は2例、0例であった。Grade 3/4の有害事象は、白血球減少や血小板数減少がGEM群で多く、口内炎や下痢がS-1で多い傾向がみられたが、全般的に両群とも良好な安全性プロファイルを示した (表2) 。
また、RFS中央値はGEM群11.2ヵ月に対しS-1群23.2ヵ月であり、S-1群で有意な延長を認め (HR=0.56, 95% CI: 0.43-0.71, p<0.0001) 、2年RFSはそれぞれ29%、49%であった。
治療完遂率はGEM群58%、S-1群72%であった。治療中止理由は、再発がGEM群26例 (14%) 、S-1群9例 (5%) 、毒性がそれぞれ48例 (25%) 、40例 (21%) 、患者拒否が5例、3例、その他は2例、0例であった。Grade 3/4の有害事象は、白血球減少や血小板数減少がGEM群で多く、口内炎や下痢がS-1で多い傾向がみられたが、全般的に両群とも良好な安全性プロファイルを示した (表2) 。
S-1群はGEM群に対する非劣性基準のみならず優越性基準をも満たした。また、RFSもS-1群がGEM群よりも有意に優れており、忍容性は両群とも良好であった。
以上より、膵癌切除後の術後補助化学療法としてS-1はGEMに対して優越性を示したことから、S-1は膵癌切除後の患者に対する新たな標準治療となる可能性がある。
以上より、膵癌切除後の術後補助化学療法としてS-1はGEMに対して優越性を示したことから、S-1は膵癌切除後の患者に対する新たな標準治療となる可能性がある。
