|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。
|

Abstract #387
切除不能進行・再発大腸癌2nd-line治療例に対するPanitumumab + FOLFIRI療法とFOLFIRI療法の無作為化比較第III相試験 (20050181試験) :最終報告
Final results from study 181: Randomized phase III study of FOLFIRI with or without panitumumab (pmab) for the treatment of second-line metastatic colorectal cancer (mCRC).
Alberto F. Sobrero, et al.

2nd-line FOLFIRI + Panitumumab療法は標準治療の1つであることが再確認された

また、今回報告された探索的な検討として、FOLFIRI + Panitumumab療法によりgrade 2-4の皮膚毒性がみられた患者では、FOLFIRI療法を受けた患者に比べ、PFSおよびOSの有意な延長が認められ、既報と同様に皮膚毒性はKRAS 遺伝子変異とは独立した治療効果予測因子であることが本試験でも確認された。しかしながら、皮膚毒性はあくまで有害事象であり、願わくはPanitumumab投与前に事前に皮膚毒性の程度を予測する方法の開発が望まれる。
20050181試験では、KRAS 野生型の切除不能進行・再発大腸癌の2nd-line治療例に対するFOLFIRI療法へのPanitumumabの上乗せにより、PFSの有意な延長とOSの延長傾向が認められた1)。今回は予定されていた最終症例登録から30ヵ月時点での有効性の最終解析結果、ならびにKRAS 野生型における皮膚毒性の程度と抗腫瘍効果について報告する。
対象と方法は既報の通りである。皮膚毒性の程度と抗腫瘍効果については、バイアスを最小化するためにランドマーク解析を行った。50%超の患者で最高gradeの皮膚毒性が認められる治療開始28日目をランドマークとし、その時点で腫瘍の増悪が認められない患者を解析対象とした。
全1,186例中、KRAS statusが判明したのは1,083例 (91%) であった。KRAS 野生型は597例 (55%) であり、Panitumumab + FOLFIRI群で303例、FOLFIRI群では294例であった。各群の患者背景に偏りはみられなかった。Oxaliplatin既投与例はKRAS 野生型のPanitumumab併用群で67%、FOLFIRI群では65%、Bevacizumab既投与例は各々18%、20%、肝臓を含む複数の転移を有する症例は68%、65%であった。
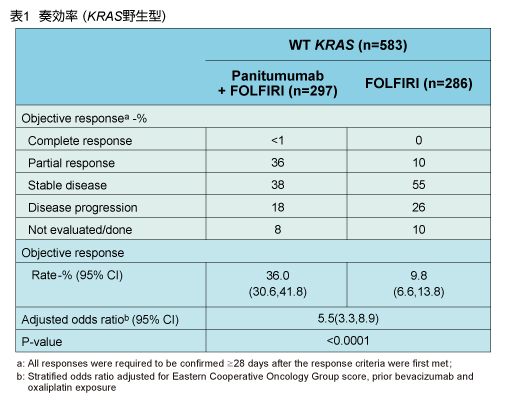
奏効率はPanitumumab併用群で36.0%、FOLFIRI群では9.8%であり、Panitumumabの併用による有意な改善が得られた (Adjusted OR=5.5, 95% CI: 3.3-8.9, p<0.0001) (表1)。
奏効率はPanitumumab併用群で36.0%、FOLFIRI群では9.8%であり、Panitumumabの併用による有意な改善が得られた (Adjusted OR=5.5, 95% CI: 3.3-8.9, p<0.0001) (表1)。
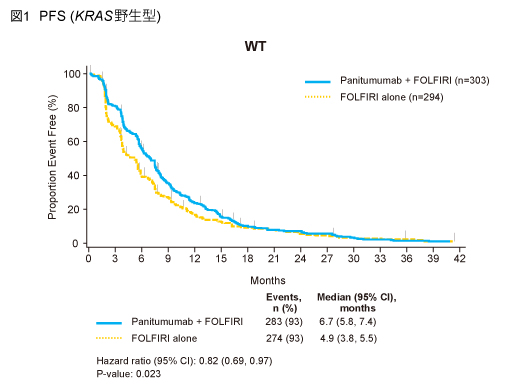
KRAS 野生型患者におけるPFS中央値は、Panitumumab併用群で6.7ヵ月、FOLFIRI群では4.9ヵ月であり、Panitumumab併用による有意な延長が認められた (HR=0.82, 95% CI: 0.69-0.97, p=0.023) (図1)。
一方、OS中央値は各々14.5ヵ月、12.5ヵ月であり、Panitumumab併用による延長傾向がみられたものの、有意差は得られなかった (HR=0.92, 95% CI: 0.78-1.10, p=0.37)。試験治療後に抗EGFR抗体薬が投与された患者はPanitumumab併用群で12%、FOLFIRI群では34%であり、FOLFIRI群のOSへの影響が考えられた。
一方、OS中央値は各々14.5ヵ月、12.5ヵ月であり、Panitumumab併用による延長傾向がみられたものの、有意差は得られなかった (HR=0.92, 95% CI: 0.78-1.10, p=0.37)。試験治療後に抗EGFR抗体薬が投与された患者はPanitumumab併用群で12%、FOLFIRI群では34%であり、FOLFIRI群のOSへの影響が考えられた。
有害事象は初回解析とほぼ同様であった。
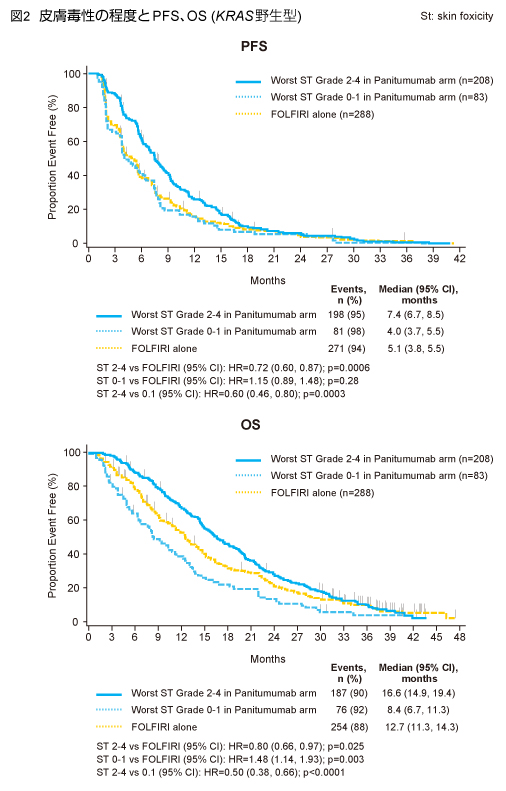
皮膚毒性の最高grade別のPFS中央値は、KRAS 野生型のPanitumumab併用群のgrade 2-4で7.4ヵ月、FOLFIRI群では5.1ヵ月 (HR=0.72, 95% CI: 0.60-0.87, p=0.0006)、OS中央値は各々16.6ヵ月、12.7ヵ月であり (HR=0.80, 95% CI: 0.66-0.97, p=0.025)、FOLFIRI群と比較してgrade 2-4で有意に良好であった (図2)。
一方、grade 0/1ではFOLFIRI群との比較においてもPFS中央値 (Grade 0/1 vs. FOLFIRI群=4.0ヵ月 vs. 5.1ヵ月)、OS中央値 (8.4ヵ月 vs. 12.7ヵ月) ともに不良であり、PRIME試験最終解析における皮膚毒性と抗腫瘍効果の結果と同様であった2)。
皮膚毒性の最高grade別のPFS中央値は、KRAS 野生型のPanitumumab併用群のgrade 2-4で7.4ヵ月、FOLFIRI群では5.1ヵ月 (HR=0.72, 95% CI: 0.60-0.87, p=0.0006)、OS中央値は各々16.6ヵ月、12.7ヵ月であり (HR=0.80, 95% CI: 0.66-0.97, p=0.025)、FOLFIRI群と比較してgrade 2-4で有意に良好であった (図2)。
一方、grade 0/1ではFOLFIRI群との比較においてもPFS中央値 (Grade 0/1 vs. FOLFIRI群=4.0ヵ月 vs. 5.1ヵ月)、OS中央値 (8.4ヵ月 vs. 12.7ヵ月) ともに不良であり、PRIME試験最終解析における皮膚毒性と抗腫瘍効果の結果と同様であった2)。
本最終解析結果では、初回解析1)と同じくFOLFIRIとPanitumumabの併用による奏効率およびPFSの有意な延長ならびにOSの延長傾向が認められた。試験治療終了後、FOLFIRI群の34%に抗EGFR抗体薬が投与されており、OSに影響を与えた可能性が考えられた。有害事象のプロファイルは初回解析とほぼ同様であった。また、FOLFIRI + Panitumumab療法によりgrade 2-4の皮膚毒性がみられたKRAS 野生型の患者では、FOLFIRI療法を受けた患者に比べ、PFSおよびOSの有意な延長が認められた。
Reference
1) Peeters M, et al.: J Clin Oncol. 28(31): 4706-4713, 2010 [PubMed]
2) Douillard JY, et al.: 2012 Gastrointestinal Cancers Symposium: abst #531 [学会レポート]
1) Peeters M, et al.: J Clin Oncol. 28(31): 4706-4713, 2010 [PubMed]
2) Douillard JY, et al.: 2012 Gastrointestinal Cancers Symposium: abst #531 [学会レポート]
関連リンク
2012年 消化器癌シンポジウム #531
皮膚毒性の程度と抗腫瘍効果、患者によるQOL評価 (PRO) の最終報告:切除不能進行・再発大腸癌初回治療例に対するPanitumumab±FOLFOX4療法の無作為化比較第III相試験 (PRIME試験) 2010年 米国臨床腫瘍学会年次集会 #3529
切除不能進行・再発大腸癌二次治療例に対するFOLFIRI+panitumumab療法とFOLFIRI療法の無作為化比較第III相試験 (20050181試験) における皮膚毒性と抗腫瘍効果に関する検討 2011年 米国臨床腫瘍学会年次集会 #3574
切除不能進行・再発大腸癌2nd-line治療例に対するPanitumumab + FOLFIRI療法とFOLFIRI療法無作為化比較第III相試験 (20050181試験) のサブグループ解析 ESMO 2011 #6132
Oxaliplatin ± Bevacizumab治療歴を有するKRAS 遺伝子野生型の切除不能進行・再発大腸癌患者に対するPanitumumab + FOLFIRI療法とFOLFIRI療法の有効性の比較: 20050181試験の結果から
2012年 消化器癌シンポジウム #531
皮膚毒性の程度と抗腫瘍効果、患者によるQOL評価 (PRO) の最終報告:切除不能進行・再発大腸癌初回治療例に対するPanitumumab±FOLFOX4療法の無作為化比較第III相試験 (PRIME試験) 2010年 米国臨床腫瘍学会年次集会 #3529
切除不能進行・再発大腸癌二次治療例に対するFOLFIRI+panitumumab療法とFOLFIRI療法の無作為化比較第III相試験 (20050181試験) における皮膚毒性と抗腫瘍効果に関する検討 2011年 米国臨床腫瘍学会年次集会 #3574
切除不能進行・再発大腸癌2nd-line治療例に対するPanitumumab + FOLFIRI療法とFOLFIRI療法無作為化比較第III相試験 (20050181試験) のサブグループ解析 ESMO 2011 #6132
Oxaliplatin ± Bevacizumab治療歴を有するKRAS 遺伝子野生型の切除不能進行・再発大腸癌患者に対するPanitumumab + FOLFIRI療法とFOLFIRI療法の有効性の比較: 20050181試験の結果から
