|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。
|

Abstract #531
皮膚毒性の程度と抗腫瘍効果、患者によるQOL評価 (PRO) の最終報告:切除不能進行・再発大腸癌初回治療例に対するPanitumumab±FOLFOX4療法の無作為化比較第III相試験 (PRIME試験)
Final skin toxicity and patient-reported outcomes results from PRIME: A randomized phase 3 study of panitumumab + FOLFOX4 for 1st-line metastatic colorectal cancer
Jean-Yves Douillard, et al.

抗EGFR抗体薬の治療効果予測マーカーとしての皮膚毒性の程度の意義は?

今回は、大腸癌初回化学療法FOLFOX4へのPanitumumabの上乗せ効果を検証するPRIME試験1) における皮膚毒性の程度と抗腫瘍効果、患者によるQOL評価 (PRO: Patient Reported Outcomes) が検討されている。すでに報告された内容2) ではあるが、PRIME試験の最終解析結果3) におけるKRAS 野生型症例を対象に絞って検討したものである。その結果、今までの多くの報告と同様に、KRAS 野生型のgrade 2-4を認めた症例ではgrade 0-1の症例と比較して、奏効率、progression-free survival (PFS)、overall survival (OS) の延長に有意差を認めたとの結果であった。
抗EGFR抗体薬の臨床効果と皮膚毒性の程度の相関で重要なことは、皮膚障害の程度が少ない症例では効果が十分に得られないことであると思われる。
Cetuximabにおいては、皮膚反応が陰性もしくは軽度の症例における用量増量試験 (EVEREST) が行われ、Cetuximabを増量することにより奏効率が改善することが報告されたが、PFSの延長効果は0.9ヵ月であり、十分とは言えない結果であった4)。
また、皮膚毒性の程度の評価は臨床医の判断であり、皮膚毒性に対する予防的な支持療法介入によっても毒性の程度が変わり得るものであることなどもあり、現在のところは、皮膚毒性の程度をマーカーとして個々の患者さんの治療戦略を立てていくことは困難であると言わざるを得ない。
皮膚毒性は宿主の反応でもあることから、今後、宿主側の遺伝子の解析等により治療前に予測できるバイオマーカーの検討がなされることを期待したい。
PRIME試験の最終解析より、KRAS 野生型の切除不能進行・再発大腸癌患者の1st-line治療において、Panitumumab + FOLFOX4群はFOLFOX4単独群と比較し、有意にPFSおよび奏効率を改善することが示された3)。今回は皮膚毒性の程度と抗腫瘍効果、患者によるQOL評価 (PRO) の最終解析結果から、KRAS 野生型の患者について報告する。
本試験の対象と評価項目は既報の通りである。皮膚毒性およびPROの解析は、最後の症例登録から30ヵ月時点での最終解析のデータをもとに行った。
PROはEuroQol 5項目法 (EQ-5D) のHealth State Index (HSI) およびOverall Health Rating (OHR) を用いて評価した。皮膚毒性の程度と抗腫瘍効果については、バイアスを最小化するためにランドマーク解析を行った。50%超の患者で最高gradeの皮膚毒性が認められる治療開始28日目をランドマークとし、その時点で腫瘍の増悪が認められない患者を解析対象とした。
PROはEuroQol 5項目法 (EQ-5D) のHealth State Index (HSI) およびOverall Health Rating (OHR) を用いて評価した。皮膚毒性の程度と抗腫瘍効果については、バイアスを最小化するためにランドマーク解析を行った。50%超の患者で最高gradeの皮膚毒性が認められる治療開始28日目をランドマークとし、その時点で腫瘍の増悪が認められない患者を解析対象とした。
PRIME試験登録患者1,183例のうち、皮膚毒性解析の対象となったのはKRAS 野生型および変異型患者1,057例であった。KRAS 野生型患者の内訳は、Panitumumab併用群の皮膚毒性の最高grade 2-4が250例、同grade 0-1が64例、FOLFOX4群は320例であった。
最終解析時のKRAS 野生型患者のPFSおよびOS中央値、奏効率は既報の通りである。
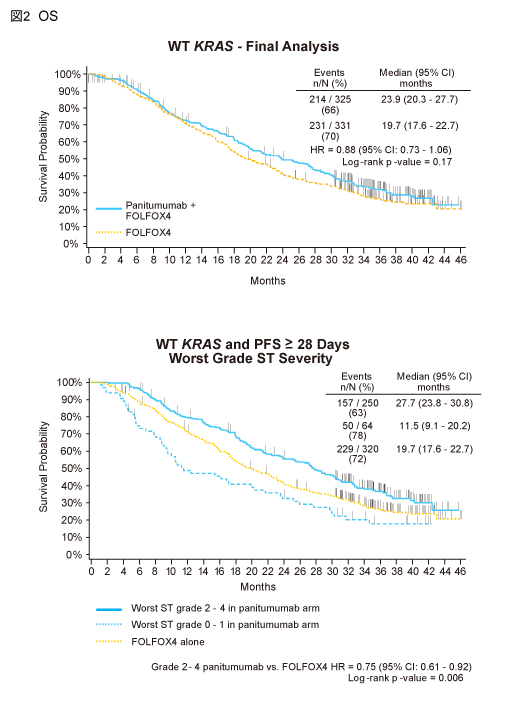
皮膚毒性の最高grade別のPFS中央値は、Panitumumab併用群のgrade 2-4で11.3ヵ月、grade 0-1で6.1ヵ月、FOLFOX4群では8.7ヵ月であり、grade 2-4においてFOLFOX4群と比較してPFSの有意な延長が認められた (HR=0.71, 95% CI: 0.59-0.85, p=0.0002) (図1)。また、OS中央値は各々27.7ヵ月、11.5ヵ月、19.7ヵ月であり、PFSと同様、grade 2-4においてFOLFOX4群と比較してOSの有意な延長が認められた (HR=0.75, 95% CI: 0.61-0.92, p=0.006) (図2)。
最終解析時のKRAS 野生型患者のPFSおよびOS中央値、奏効率は既報の通りである。
皮膚毒性の最高grade別のPFS中央値は、Panitumumab併用群のgrade 2-4で11.3ヵ月、grade 0-1で6.1ヵ月、FOLFOX4群では8.7ヵ月であり、grade 2-4においてFOLFOX4群と比較してPFSの有意な延長が認められた (HR=0.71, 95% CI: 0.59-0.85, p=0.0002) (図1)。また、OS中央値は各々27.7ヵ月、11.5ヵ月、19.7ヵ月であり、PFSと同様、grade 2-4においてFOLFOX4群と比較してOSの有意な延長が認められた (HR=0.75, 95% CI: 0.61-0.92, p=0.006) (図2)。
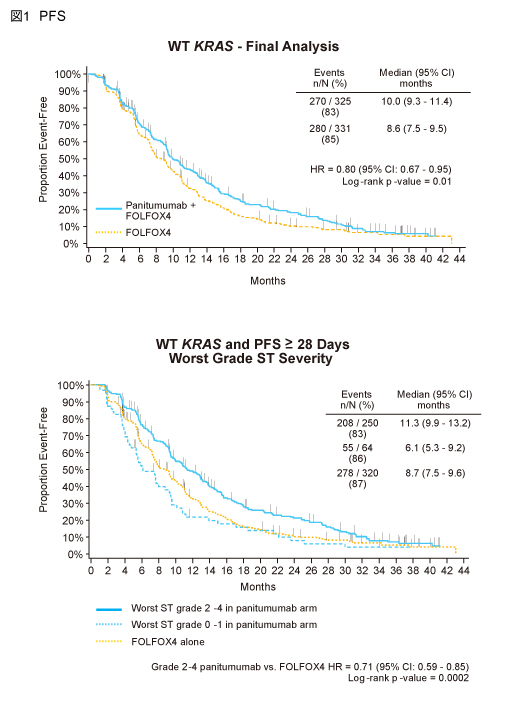
奏効率はPanitumumab併用群のgrade 2-4で63% (95% CI: 57-69%)、grade 0-1で41% (29-54%)、FOLFOX4群では49% (44-55%) であった。
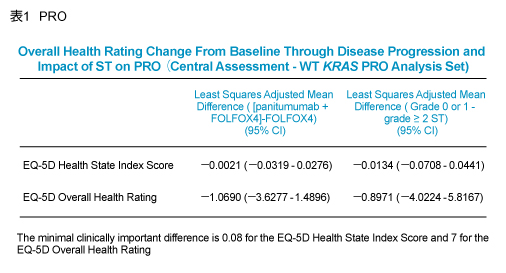
PROについては、Panitumumab併用群とFOLFOX4群の間に臨床上意義のある差は認められず、また皮膚毒性grade 2-4とgrade 0-1の症例においても差はみられなかった (表1)。全体の有害事象のプロファイルは、grade 2-4/0-1群とFOLFOX4群とで概ね同程度であった。
PROについては、Panitumumab併用群とFOLFOX4群の間に臨床上意義のある差は認められず、また皮膚毒性grade 2-4とgrade 0-1の症例においても差はみられなかった (表1)。全体の有害事象のプロファイルは、grade 2-4/0-1群とFOLFOX4群とで概ね同程度であった。
KRAS 野生型で1st-line治療としてPanitumumab + FOLFOX4療法を受けた患者のうち、皮膚毒性の最高grade 2-4の患者では、FOLFOX4群と比べてPFSおよびOSの有意な延長が認められた。また、皮膚毒性の最高grade 2-4とgrade 0-1の患者でPROに有意な差異はみられなかった。有害事象のプロファイルは、抗EGFR治療で予想される範囲のものであった。
Reference
1) Douillard JY, et al.: J Clin Oncol. 28(31): 4697-4705, 2010 [PubMed][論文紹介]
2) Douillard JY, et al.: 2010 Annual Meeting of the American Society of Clinical Oncology®: abst #3528 [学会レポート]
3) Douillard JY, et al.: 2011 Annual Meeting of the American Society of Clinical Oncology®: abst #3510 [学会レポート]
4) Tejpar S, et al.: 2007 Annual Meeting of the American Society of Clinical Oncology®: abst #4037
1) Douillard JY, et al.: J Clin Oncol. 28(31): 4697-4705, 2010 [PubMed][論文紹介]
2) Douillard JY, et al.: 2010 Annual Meeting of the American Society of Clinical Oncology®: abst #3528 [学会レポート]
3) Douillard JY, et al.: 2011 Annual Meeting of the American Society of Clinical Oncology®: abst #3510 [学会レポート]
4) Tejpar S, et al.: 2007 Annual Meeting of the American Society of Clinical Oncology®: abst #4037
関連リンク
2011年 米国臨床腫瘍学会年次集会 #3510
切除不能進行・再発大腸癌初回治療例に対するPanitumumab + FOLFOX4療法とFOLFOX4療法の無作為化比較第III相試験 (PRIME試験): 最終報告
2010年 米国臨床腫瘍学会年次集会 #3528
切除不能進行・再発大腸癌初回治療例に対するFOLFOX4+panitumumab療法とFOLFOX4療法の無作為化比較第III相試験 (PRIME試験) における皮膚毒性と抗腫瘍効果に関する検討
論文紹介
未治療の転移を有する大腸癌患者に対する1st-line治療としてのpanitumumab + infusional 5-FU/LV/oxaliplatin (FOLFOX4) 併用とFOLFOX4単独の比較:第III相無作為化試験 (PRIME) の結果 (Douillard JY, et al.: J Clin Oncol. 2010)
2011年 米国臨床腫瘍学会年次集会 #3510
切除不能進行・再発大腸癌初回治療例に対するPanitumumab + FOLFOX4療法とFOLFOX4療法の無作為化比較第III相試験 (PRIME試験): 最終報告
2010年 米国臨床腫瘍学会年次集会 #3528
切除不能進行・再発大腸癌初回治療例に対するFOLFOX4+panitumumab療法とFOLFOX4療法の無作為化比較第III相試験 (PRIME試験) における皮膚毒性と抗腫瘍効果に関する検討
論文紹介
未治療の転移を有する大腸癌患者に対する1st-line治療としてのpanitumumab + infusional 5-FU/LV/oxaliplatin (FOLFOX4) 併用とFOLFOX4単独の比較:第III相無作為化試験 (PRIME) の結果 (Douillard JY, et al.: J Clin Oncol. 2010)
