|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。
|

Abstract #384
Stage II結腸癌患者の遺伝子発現プロファイルに基づく予後予測分類 (ColoPrint) の臨床的および技術的validation
Clinical and technical validation of a genomic classifier (ColoPrint) for predicting outcome of stage II colon cancer patients
Josep Tabernero, et al.

ColoPrint: stage II結腸癌治癒切除例の再発リスクを予測する画期的な多重遺伝子診断法

大腸癌領域でも、Oncotype DX ColonやColoPrintなどの多重遺伝子診断法の開発が進んでいる。特にstage II結腸癌治癒切除例の再発リスク層別化の研究が盛んに行われており、本研究からColoPrintは再発リスクの高いstage II結腸癌を正確に選別できる可能性が示唆された。特記すべきことは、単変量解析で米国臨床腫瘍学会年次集会1) やNCCNガイドライン2) で提唱されるhigh risk featureと比較して、3年recurrence-free survival (RFS) に対しColoPrintはハザード比2.9と凌駕する成績を示したこと、MSI (マイクロサテライト不安定性)*のハザード比をも超える点である。
さらにT3-MSS症例に限定した検討は、Oncotype DX Colonとの比較可能性を意識した内容といえる。3年RFSに対しColoPrintはハザード比3.04であり、Oncotype DX Colonのハザード比1.6より良好である。ColoPrintは再発リスクの高いstage II患者の識別にきわめて有用であり、臨床病理的パラメータを補足的に用いることでよりよい治療決定が可能になると考えられる。
Oncotype DX Colonはホルマリン固定パラフィン包埋切片で解析が可能である一方、 ColoPrintは新鮮標本が必要という不利な一面もあるが、技術革新によってこの点が解決されることを期待する。
*MSIが低い症例 (MSI-L) およびMSIを示さない症例 (MSS) では再発リスクが高く、MSIが高い症例 (MSI-H) では再発リスクが低いと報告されている (参照:GI - pedia)。
治癒切除後stage II結腸癌患者の25 - 35%で再発がみられることから、stage IIにおいても術後補助化学療法のベネフィットが得られる患者群があると考えられる。ColoPrintは、18遺伝子の発現プロファイルに基づいてstage I-III結腸癌患者の再発リスクを予測する予後分類である。今回は複数のclinical validation studyにおけるstage II症例のプール解析の結果を報告する。
3本のclinical validation studyに登録されたstage II結腸癌320例 (追跡期間中央値70ヵ月) を対象に、単変量および多変量解析を行った。再現性・標準化試験では、再発リスク別 (低・中・高リスク) のサンプルを用いた。
Stage II症例320例のうち、ColoPrintにより209例 (65.3%) が低リスクに、111症例 (34.7%) が高リスクに分類された。患者背景 (低リスク群 vs. 高リスク群) は年齢中央値: 67.3歳 vs. 69.3歳、70歳超: 37.8% vs. 41.4%、男性: 55.5% vs. 63.1%、検索リンパ節12個以下: 19.6% vs. 26.1%、T4: 12.9% vs. 9.0%であり、両群間に有意差はみられなかった。MSIを示さない症例 (MSS) は低リスク群で74.6%、高リスク群では87.4%であり、高リスク群で有意に多かった (p=0.008)。
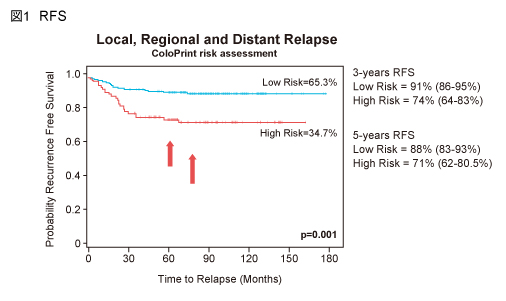
RFSは両群間で有意差がみられた (p=0.001) (図1)。3年RFSは低リスク群で91% (95% CI: 86 - 95%)、高リスク群では74% (64 - 83%) であり、既報のvalidation studyの結果と酷似していた (各々90.9%、73.9%)3)。
RFSは両群間で有意差がみられた (p=0.001) (図1)。3年RFSは低リスク群で91% (95% CI: 86 - 95%)、高リスク群では74% (64 - 83%) であり、既報のvalidation studyの結果と酷似していた (各々90.9%、73.9%)3)。
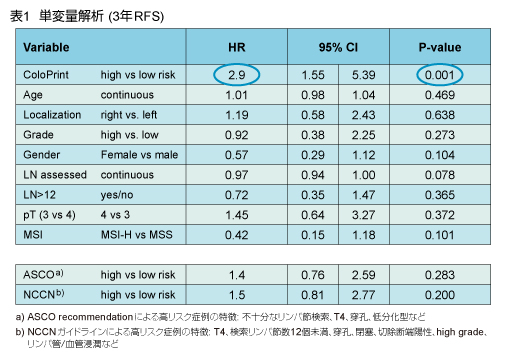
3年RFSの単変量解析では、ColoPrint (高リスク群 vs. 低リスク群) が唯一の有意な独立したパラメータであった (HR=2.9, 95% CI: 1.55-5.39, p=0.001) (表1)。検索リンパ節数、T-stage、MSI、また複数の臨床病理学的因子から成る米国臨床腫瘍学会年次集会 recommendation1) およびNCCNガイドライン2) によるリスク評価は、いずれも有意なパラメータではなかった。
さらに米国臨床腫瘍学会年次集会 (p=0.165)、NCCN (p=0.113)、T-stage (p=0.166)、MSI (p=0.086) に基づき患者を2群に分類しRFSを比較したところ、いずれにおいても有意差は示されなかった。
さらに米国臨床腫瘍学会年次集会 (p=0.165)、NCCN (p=0.113)、T-stage (p=0.166)、MSI (p=0.086) に基づき患者を2群に分類しRFSを比較したところ、いずれにおいても有意差は示されなかった。
T3かつMSSの症例 (T3-MSS) 227例を対象としたサブグループ解析においても、ColoPrintは3年RFSの有意な独立したパラメータであった (HR=3.04, 95% CI: 1.45-6.34, p=0.003)。T3-MSSの3年RFSは低リスク群で91%、高リスク群では73%であり、全体解析と一貫した結果が得られた。
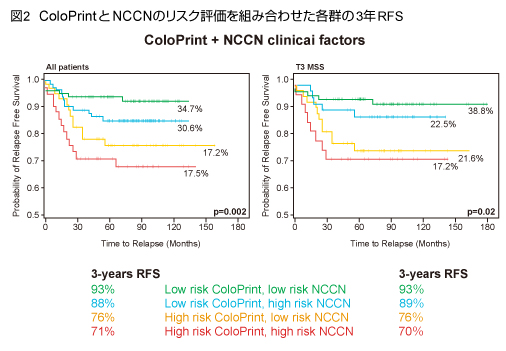
さらに、ColoPrintとNCCNの組み合わせにより患者を4群に分け、3年RFSを比較した (図2)。その結果、ColoPrint / NCCN低リスク群で93%、ColoPrint低 / NCCN高リスク群で88%、ColoPrint高 / NCCN低リスク群で76%、ColoPrint / NCCN高リスク群では71%であった (p=0.002)。T3-MSSにおいてもほぼ同値であり、ColoPrintと臨床病理学的パラメータを組み合わせることで、最良のリスク層別化ができる可能性が示された。
さらに、ColoPrintとNCCNの組み合わせにより患者を4群に分け、3年RFSを比較した (図2)。その結果、ColoPrint / NCCN低リスク群で93%、ColoPrint低 / NCCN高リスク群で88%、ColoPrint高 / NCCN低リスク群で76%、ColoPrint / NCCN高リスク群では71%であった (p=0.002)。T3-MSSにおいてもほぼ同値であり、ColoPrintと臨床病理学的パラメータを組み合わせることで、最良のリスク層別化ができる可能性が示された。
なお、再現性・標準化試験として複数の検者が低・中・高リスクの3種類のサンプルを用い、連続して20日間解析を行った結果、ばらつきがみられたのは5%未満であった。
本解析では、治癒切除後のstage II結腸癌患者の60%以上がColoPrintにより低リスク群 (3年RFS: 91%) に分類された。ColoPrintは再発リスクの高いstage II患者の識別に有用であり、臨床病理的パラメータを補足的に用いることでよりよい治療決定が可能になると考えられる。
現在、stage II/III結腸癌患者を対象とした前向き研究 (PARSC試験) が進行中であり、これまでに11ヵ国32施設からstage II 340例、stage III 300例が登録された4)。同試験ではstage II 575例の登録を目指している。
現在、stage II/III結腸癌患者を対象とした前向き研究 (PARSC試験) が進行中であり、これまでに11ヵ国32施設からstage II 340例、stage III 300例が登録された4)。同試験ではstage II 575例の登録を目指している。
Reference
1) Benson AB 3rd, et al.: J Clin Oncol. 24(1): J Clin Oncol. 22(16): 3408-3419, 2004 [PubMed][論文紹介]
2) NCCN Clinical Practice Guideline in Oncology, Colon Cancer, 2012, version 2
3) Salazar R, et al.: J Clin Oncol. 29(1): 17-24, 2011 [PubMed][論文紹介]
4) Salazar R, et al.: 2012 Gastrointestinal Cancers Symposium: abst #678
1) Benson AB 3rd, et al.: J Clin Oncol. 24(1): J Clin Oncol. 22(16): 3408-3419, 2004 [PubMed][論文紹介]
2) NCCN Clinical Practice Guideline in Oncology, Colon Cancer, 2012, version 2
3) Salazar R, et al.: J Clin Oncol. 29(1): 17-24, 2011 [PubMed][論文紹介]
4) Salazar R, et al.: 2012 Gastrointestinal Cancers Symposium: abst #678
関連リンク
論文紹介
StageIIおよびIIIの大腸癌における予後予測を改善するための遺伝子発現サイン (Salazar R, et al.: J Clin Oncol. 2011) GI-pedia 第3回「大腸癌のバイオマーカー」
2. 術後補助化学療法におけるバイオマーカー 2009年 米国臨床腫瘍学会年次集会 #4000-4002
分子マーカーによる個別化術後補助化学療法
(QUASAR validation study/PETACC-3試験のトランスレーショナルリサーチ) 論文紹介
結腸癌における5-FUベース術後補助化学療法の無効を予測するマーカーとしてのミスマッチ修復欠損 (Sargent DJ, et al.: J Clin Oncol. 2010)
論文紹介
StageIIおよびIIIの大腸癌における予後予測を改善するための遺伝子発現サイン (Salazar R, et al.: J Clin Oncol. 2011) GI-pedia 第3回「大腸癌のバイオマーカー」
2. 術後補助化学療法におけるバイオマーカー 2009年 米国臨床腫瘍学会年次集会 #4000-4002
分子マーカーによる個別化術後補助化学療法
(QUASAR validation study/PETACC-3試験のトランスレーショナルリサーチ) 論文紹介
結腸癌における5-FUベース術後補助化学療法の無効を予測するマーカーとしてのミスマッチ修復欠損 (Sargent DJ, et al.: J Clin Oncol. 2010)
