ESMO 2014 Congress
戝挵娻
Abstract #501O
CALGB/SWOG 80405帋尡丗枹帯椕偺愗彍晄擻恑峴丒嵞敪戝挵態娻姵幰偵懳偡傞FOLFIRI / mFOLFOX6偲Bevacizumab傑偨偼Cetuximab暪梡偺戞III憡帋尡亅奼戝RAS 夝愅
CALGB/SWOG 80405: Phase III Trial of Irinotecan/5-FU/Leucovorin (FOLFIRI) or Oxaliplatin/5-FU/Leucovorin (mFOLFOX6) with Bevacizumab (BV) or Cetuximab (CET) for Patients (Pts) with Untreated Metastatic Adenocarcinoma of the Colon or Rectum (MCRC): Expanded RAS analyses
Heinz-Josef Lenz, et al.

Expert's view

巗愳 搙 愭惗
徍榓戝妛摗偑媢昦堾
庮釃撪壢
丂KRAS exon 2栰惗宆偱怴偟偔RAS 曄堎偑偁傞偲敾掕偝傟偨徢椺偱偼丄Cmab孮偱OS偑椙岲側孹岦傪擣傔偨 (HR=0.74, 95% CI: 0.4-1.1, p=0.21)丅FIRE-3帋尡側偳偺偙傟傑偱偺曬崘偐傜偼梊憐傕偮偐側偄寢壥偱偁傞丅梊憐傕偮偐側偄寢壥傪尒偨偲偒丄椪彴壠偼帋尡偺幙傪傑偢媈栤帇偟丄偦偺寢壥傪庴偗擖傟側偄懺搙傪偲傝偑偪偱偁傞丅偦傕偦傕丄乽RAS 曄堎宆偵峈EGFR峈懱栻偼柍岠乿偺僄價僨儞僗偼丄慜岦偒偵峴傢傟偨椪彴帋尡偺廔椆屻偵屻傠岦偒尋媶偲偟偰峴傢傟傞乬prospective-retrospective design乭偵婎偯偄偨傕偺偱偁傞丅偙偺僨僓僀儞偱偼丄嵞尰惈偺偁傞寢壥偑暋悢偺帋尡偱婛偵摼傜傟偰偄傞埲忋丄崱夞偺CALGB/SWOG 80405帋尡偑堎側偭偨寢壥偱偁偭偰傕丄乽RAS 曄堎宆偵峈EGFR峈懱栻偼柍岠乿偺僄價僨儞僗偼儗儀儖I偺傑傑偱晄曄偱偁傞丅
丂傑偨丄FIRE-3帋尡丄PEAK帋尡偲堎側傝丄CALGB/SWOG 80405帋尡偱偼RAS 栰惗宆偵偍偗傞OS墑挿偑Cmab孮偱擣傔傜傟側偐偭偨丅崱夞偺敪昞偼丄栺60亾偺徢椺傪懳徾偲偟偨乽work in progress乿偺拞娫夝愅偱偁傝丄寢榑偼崱屻偺敪昞傪懸偮傋偒偱偁傠偆丅RAS 栰惗宆傪専摙偟偨崱夞偺栺60亾偺徢椺偼KRAS exon 2傪専摙偟偨徢椺偺姵幰攚宨偲嵎偑側偄偲弎傋傜傟偨丅偟偐偟丄桳堄嵎専掕偼偝傟偰偄側傕偺偺丄RAS 栰惗宆偺Cmab孮偱偼Palliative intent丄Primary in place徢椺偑彮側偔丄Liver metastases only徢椺偑懡偔擣傔傜傟丄拞娫夝愅備偊偵婲偒偨慖戰僶僀傾僗偺壜擻惈傕偁傠偆丅偝傜偵丄RAS 栰惗宆偵偍偗傞FOLFIRI + Cmab偺OS偼FIRE-3帋尡33.1儠寧丄CALGB/SWOG 80405帋尡32.0儠寧偲嵞尰惈偑偁傞偑丄RAS 栰惗宆偵偍偗傞FOLFIRI + Bev偺OS偼FIRE-3帋尡25.6儠寧丄CALGB/SWOG 80405帋尡35.2儠寧偲丄帋尡娫斾妑偱偼偁傞傕偺偺OS偑戝偒偔堎側偭偰偄傞丅傗偼傝丄Lenz愭惗偑弎傋偨傛偆偵丄RAS 栰惗宆偵偍偗傞寢榑偼丄崱屻偺RAS 夝愅傗1st-line偺帯椕嫮搙偲帯椕婜娫丄2nd-line側偳偺徻嵶僨乕僞傕崌傢偣偰峫偊傞傋偒偱偁傠偆丅
丂ESMO偼廔傢偭偰傕丄寢嬊丄CALGB/SWOG 80405帋尡偼 乬Stay tuned乭 (TV僠儍儞僱儖偼偦偺傑傑両) 偱偁傞丅僠儍儞僱儖傪懼偊側偐偭偨傕偺偺丄婥偑偮偄偨傜曻憲拞巭偱乬Never ending story乭偩偭偨偲偄偆帠懺偩偗偼旔偗偰梸偟偄傕偺偱偁傞丅
丂CALGB80405帋尡偱偼丄KRAS exon 2 (codon 12, 13) 栰惗宆偺愗彍晄擻恑峴丒嵞敪戝挵娻偵懳偡傞1st-line偵偍偗傞FOLFIRI傑偨偼mFOLFOX6偲偺暪梡椕朄偲偟偰Bevacizumab (Bev) 偲Cetuximab (Cmab) 傪斾妑専摙偟偨寢壥丄OS偍傛傃PFS偱嵎偑側偄偙偲偑帵偝傟偨丅堦曽丄KRAS 傗NRAS 偺懠偺codon曄堎偺妶惈壔傕丄EGFR慾奞嵻傊偺掞峈惈偵娭楢偡傞偙偲偑曬崘偝傟偰偄傞丅偦偙偱丄RAS 栰惗宆偵偍偗傞帯椕岠壥傪昡壙偡傞偨傔偵扵嶕揑夝愅傪峴偭偨丅
丂RAS 曄堎偺夝愅偵偼BEAMing朄1, 2)傪梡偄丄KRAS exon 2 (codon 12, 13)丄exon 3 (codon 59, 61)丄exon 4 (codon 117, 146)丄NRAS exon 2 (codon 12, 13)丄exon 3 (codon 59, 61)丄exon 4 (codon 117, 146) 偺儈僗僙儞僗曄堎傪僗僋儕乕僯儞僌偟偨丅側偍丄椪彴偵巊梡偝傟傞壜擻惈偺偁傞懠偺専嵏朄偵懃傝丄僇僢僩僆僼抣偼1%偲偟偨丅
丂KRAS exon 2栰惗宆偺1,137椺偺偆偪RAS 偺昡壙偑壜擻偱偁偭偨偺偼670椺 (59%) 偱偁傝丄幚嵺偵夝愅偑峴傢傟偨621椺偺偆偪95椺 (15.3%) 偱怴偨側RAS 曄堎偑摨掕偝傟偨 (恾1)丅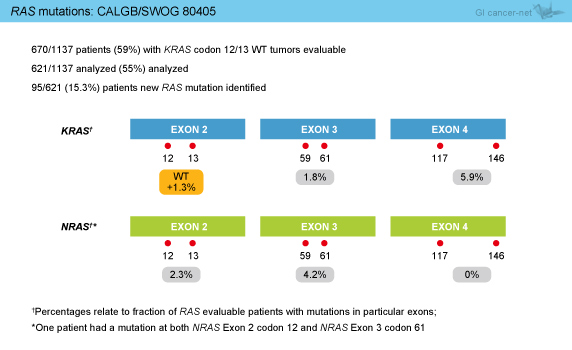
丂KRAS exon 2栰惗宆偺1,137椺偺偆偪RAS 偺昡壙偑壜擻偱偁偭偨偺偼670椺 (59%) 偱偁傝丄幚嵺偵夝愅偑峴傢傟偨621椺偺偆偪95椺 (15.3%) 偱怴偨側RAS 曄堎偑摨掕偝傟偨 (恾1)丅
恾1

丂RAS 昡壙壜擻廤抍偵偍偗傞Bev孮丄Cmab孮偺姵幰攚宨偼丄傎傏摨摍偱偁偭偨丅傑偨丄RAS 昡壙壜擻廤抍偵偍偗傞桳岠惈偼丄KRAS exon 2栰惗宆廤抍偲傎傏摨條偱偁傝丄憈岠棪偼Cmab孮偱桳堄偵椙岲偱偁偭偨傕偺偺 (p<0.01)丄PFS丄OS偱偼桳堄嵎傪擣傔側偐偭偨丅
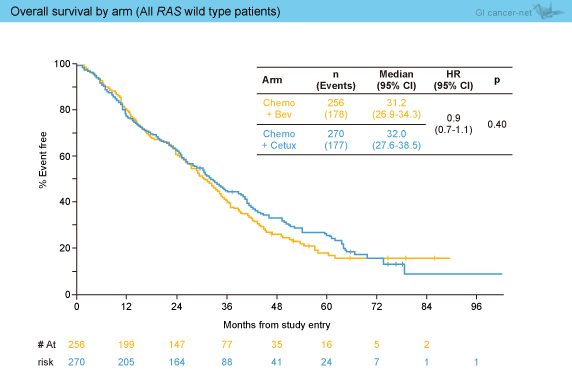
丂RAS 栰惗宆偵偍偗傞夝愅偱偼丄憈岠棪偼Bev孮53.8%丄Cmab孮68.6%偲Cmab孮偱桳堄偵椙岲偱偁偭偨 (p<0.01)丅堦曽丄PFS拞墰抣偼Bev孮11.3儠寧丄Cmab孮11.4儠寧偱偁傝丄桳堄嵎傪擣傔側偐偭偨 (HR=1.1, 95% CI: 0.9-1.3, p=0.31) (恾2)丅摨條偵丄OS拞墰抣偼Bev孮31.2儠寧丄Cmab孮32.0儠寧偲椉孮娫偵桳堄嵎傪擣傔側偐偭偨 (HR=0.9, 95% CI: 0.7-1.1, p=0.40) (恾3)丅側偍丄KRAS exon 2栰惗宆偱懠偺RAS 偺偄偢傟偐偑曄堎宆偺徢椺偱偼丄Bev孮22.3儠寧丄Cmab孮28.7儠寧偲Cmab孮偱椙岲側孹岦偱偁偭偨 (HR=0.74, 95% CI: 0.4-1.1, p=0.21)丅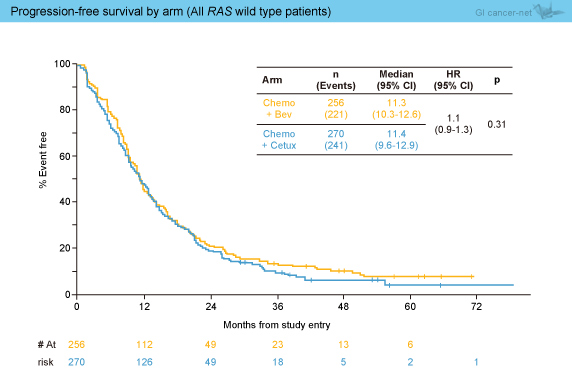
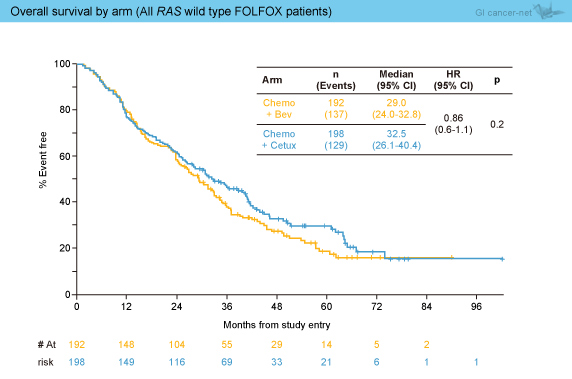
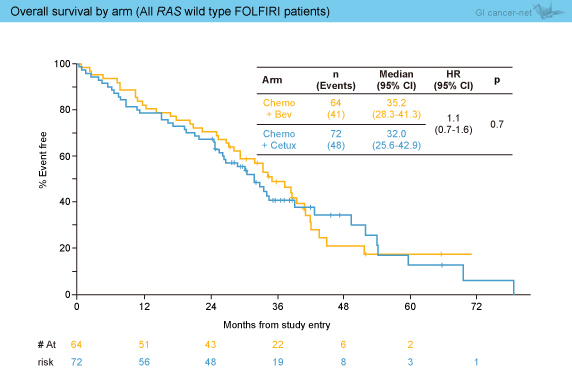
 丂RAS 栰惗宆偵偍偗傞壔妛椕朄暿夝愅偱偼丄mFOLFOX6偱偼OS拞墰抣偑Bev孮29.0儠寧丄Cmab孮32.5儠寧偱偁傝丄Cmab孮偱椙岲側孹岦偱偁傞傕偺偺桳堄嵎偼擣傔側偐偭偨 (HR=0.86, 95% CI: 0.6-1.1, p=0.2) (恾4)丅傑偨丄FOLFIRI偱偼OS拞墰抣偑Bev孮35.2儠寧丄Cmab孮32.0儠寧偱偁傝丄桳堄嵎偼擣傔側偐偭偨 (HR=1.1, 95% CI: 0.7-1.6, p=0.7) (恾5)丅
丂RAS 栰惗宆偵偍偗傞壔妛椕朄暿夝愅偱偼丄mFOLFOX6偱偼OS拞墰抣偑Bev孮29.0儠寧丄Cmab孮32.5儠寧偱偁傝丄Cmab孮偱椙岲側孹岦偱偁傞傕偺偺桳堄嵎偼擣傔側偐偭偨 (HR=0.86, 95% CI: 0.6-1.1, p=0.2) (恾4)丅傑偨丄FOLFIRI偱偼OS拞墰抣偑Bev孮35.2儠寧丄Cmab孮32.0儠寧偱偁傝丄桳堄嵎偼擣傔側偐偭偨 (HR=1.1, 95% CI: 0.7-1.6, p=0.7) (恾5)丅
丂RAS 栰惗宆偵偍偗傞夝愅偱偼丄憈岠棪偼Bev孮53.8%丄Cmab孮68.6%偲Cmab孮偱桳堄偵椙岲偱偁偭偨 (p<0.01)丅堦曽丄PFS拞墰抣偼Bev孮11.3儠寧丄Cmab孮11.4儠寧偱偁傝丄桳堄嵎傪擣傔側偐偭偨 (HR=1.1, 95% CI: 0.9-1.3, p=0.31) (恾2)丅摨條偵丄OS拞墰抣偼Bev孮31.2儠寧丄Cmab孮32.0儠寧偲椉孮娫偵桳堄嵎傪擣傔側偐偭偨 (HR=0.9, 95% CI: 0.7-1.1, p=0.40) (恾3)丅側偍丄KRAS exon 2栰惗宆偱懠偺RAS 偺偄偢傟偐偑曄堎宆偺徢椺偱偼丄Bev孮22.3儠寧丄Cmab孮28.7儠寧偲Cmab孮偱椙岲側孹岦偱偁偭偨 (HR=0.74, 95% CI: 0.4-1.1, p=0.21)丅
恾2

恾3

恾4

恾5

丂愗彍晄擻恑峴丒嵞敪戝挵娻偺怴婯恌抐椺偼偡傋偰RAS 専嵏傪庴偗傞傋偒偱偁傞偲峫偊傜傟傞丅OS偼30儠寧埲忋偑怴偨側昗弨偱偁傝丄1st-line偼暃嶌梡偺壜擻惈傪娷傔帯椕栚昗傪斀塮偡傋偒偱偁傞丅崱屻丄dose intensity丄帯椕婜娫丄庮釃晹埵丄庮釃弅彫丄2nd-line帯椕丄峈EGFR峈懱栻傗峈VEGF峈懱栻偺怴偨側僶僀僆儅乕僇乕側偳偺僨乕僞偑廤愊偝傟傟偽丄FIRE-3帋尡偲杮帋尡偲偺堘偄偵偮偄偰棟夝偑恑傓壜擻惈偑偁傞丅
偙偺僒僀僩偼堛椕娭學幰偺曽乆傪懳徾偵嶌惉偟偰偄傑偡丅昁偢偛棙梡婯栺偵摨堄偺忋丄偛棙梡偔偩偝偄丅婰帠撪梕偱庢傝忋偘偨栻嵻偺岠擻丒岠壥偍傛傃梡朄丒梡検偵偼丄擔杮崙撪偱彸擣偝傟偰偄傞撪梕偲堎側傞傕偺偑丄懡暘偵娷傑傟偰偄傑偡偺偱偛拲堄偔偩偝偄丅

