背景と目的
進行肝細胞癌は、Sorafenibによる延命効果が証明されているものの依然として予後不良な疾患である。HBV感染、HCV感染はPD-1発現を上昇させることが知られており、免疫チェックポイント阻害剤である抗CTLA-4抗体薬Tremelimumabの第II相試験では奏効率15%と良好な効果の一方、grade 3以上のトランスアミナーゼ上昇を45%に認めた1)。今回、免疫チェックポイント阻害剤の抗PD-1抗体薬であるNivolumabの進行肝細胞癌に対する第I/II相試験が行われた。
対象と方法
主な適格基準は、根治切除不能の肝細胞癌、Child-Pughスコア7点以下、少なくとも1レジメン以上の前治療歴を有する (Sorafenibを含む)、AST/ALT値が正常上限の5倍以下、等であった。肝炎ウイルスの有無により非感染 (Uninfected)、HCV、HBVの3群に分けて登録された。各群において用量漸増パートと拡大パートが設定され、Nivolumab 0.1~10mg/kgの隔週投与が行われた。
主要評価項目は用量制限毒性 (DLT) を含む安全性の評価、副次評価項目はRECIST 1.1による抗腫瘍効果、探索的解析としてOS等であった。
結果
2015年3月12日の中間解析時点において47例 (用量漸増パート43例、拡大パート4例) が登録され、各群の内訳はUninfected群21例、HCV群11例、HBV群11例であった (図1)。治療継続中は17例、治療中止は30例あった (CR 2例、PD 26例、副作用 1例)。DLTは1例のみ (肝不全) であり、最大耐用量 (MTD) には到達しなかった。
Uninfected群、HCV群では、3mg/kgの用量が選択され、拡大パートが開始された。HBV群は現在も用量漸増パートを継続中である。
図1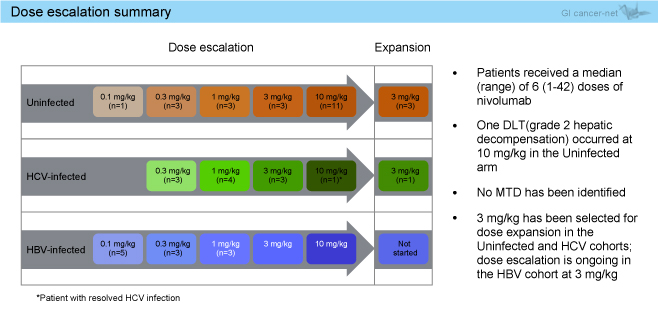
Grade 3以上の有害事象は9例 (19%) に認められ、grade 3のAST/ALT上昇が多くを占めた (表1)。
表1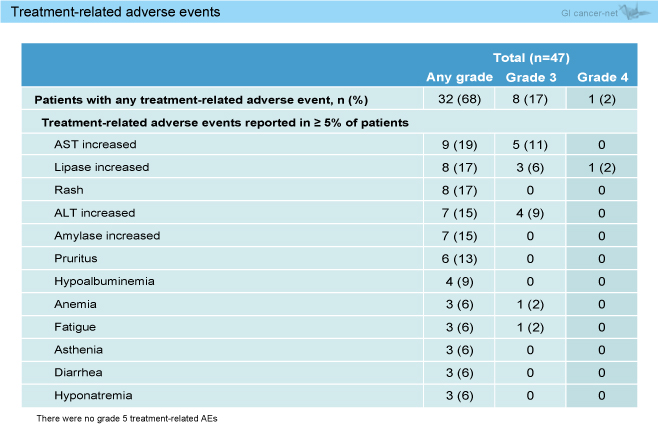
奏効率は全体で19% (CR 2例を含む) であり、Uninfected、HCV、HBVの各群それぞれ14%、36%、10%であった。標的病変の最大変化率を図2、標的病変の変化率を図3に示す。
図2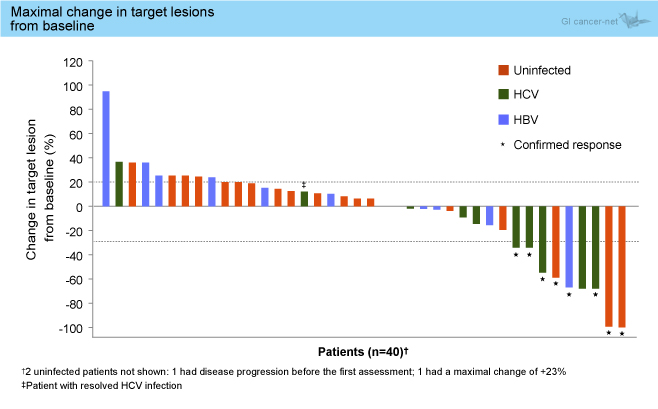
図3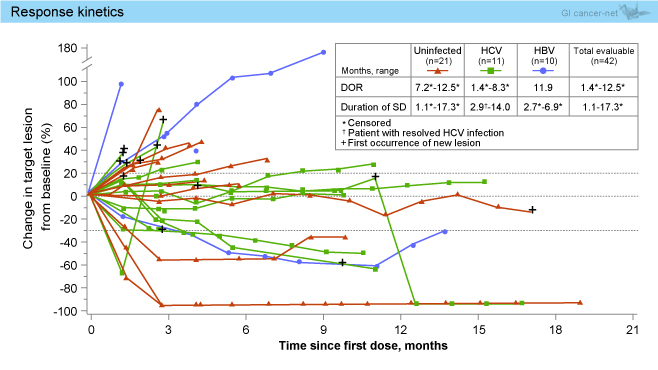
OS解析はpreliminaryであるが、9ヵ月、12ヵ月時点での生存率は、それぞれ70% (95% CI: 52-82)、62% (95% CI: 42-76) であった。
結論
Nivolumabは、良好な安全性プロファイルを有し、HBV・HCV感染を含む肝細胞癌に対する有効性が示唆された。すべての用量、コホートで抗腫瘍効果を認めたことから、現在3mg/kgの用量での拡大パートが進行中である。
コメント
ヒト型抗ヒトPD-1モノクローナル抗体薬Nivolumabは、PD-1とそのリガンドであるPD-L1およびPD-L2との結合を阻害し、癌抗原特異的なT細胞の増殖、活性化および細胞傷害活性の増強等により、腫瘍増殖を抑制する。本邦では2014年7月にメラノーマに対して製造販売承認、米国FDAでは、メラノーマに加え、2015年3月にプラチナ製剤併用化学療法中または治療後に増悪した進行肺扁平上皮癌に対し適応拡大を承認している。さらに、本発表の次演題 (LBA109) でCheckMate 057試験結果が報告された1)。対象が肺癌なので、本サイトでは報告されない内容ではあるが、重要な結果なので簡単に紹介する。CheckMate 057試験は非扁平上皮癌の非小細胞肺癌 (NSCLC) に対する2nd-lineにおける第III相試験である。標準治療のDocetaxel単剤に対し、主要評価項目OSの有意な延長が認められた (中央値12.2ヵ月 vs. 9.4ヵ月, HR=0.73, p=0.0015)。現在注目の薬剤である。
本報告で取り上げた肝細胞癌は、原発巣そのものが主要臓器であり、かつ背景に抗癌治療に大きく影響するウイルス感染や肝線維化があるため、全身化学療法の難しい領域である。抗腫瘍効果のみならず肝障害等への影響をできるだけ減らすことが、治療戦略として求められていたが、本試験結果はこれらを満たす内容であった。また、本試験における用量漸増規定が細やかに設定されていたことを評価したい。今後の臨床展開が大変期待される状況である。ディスカッションにおいても取り上げられていたが、臨床開発においてウイルス量との問題等がより詳細にデータ化され、さらなる安全性が確保できることを望む。
(レポート:谷口 浩也 監修・コメント:佐藤 温)
- Reference
-
- 1) Sangro B, et al.: J Hepatol. 59(1):81-88, 2013[PubMed]
- 2) Luis Paz-Ares, et al.: 2015 Annual Meeting of the American Society of Clinical Oncology®: abst #LBA109


