背景と目的
切除不能進行・再発大腸癌の1st-lineにおけるCapecitabine + L-OHP (CapeOX) に対するS-1 + L-OHP (SOX) の非劣性を検証するために第III相試験が韓国で行われ、既に報告されている1)。既報では、SOX群がCapeOX群に比べPFSで約2ヵ月延長し、SOX療法は1st-lineにおける2剤併用レジメンの選択肢となった。ただ、長期追跡のデータがないため、実臨床においてS-1がCapecitabineに置き換わるかは、議論の余地がある。
そこで今回、OSおよびPFSの結果をアップデートし、特定のサブグループでS-1の効果が変わり得るか探索的に解析した。
対象と方法
本試験は、SOXとCapeOXを比較した無作為化比較第III相試験であり、主要評価項目であるSOXのCapeOXに対するPFSは非劣性が示され、既に2012年に報告されている1)。
対象は、18歳以上で化学療法未施行、ECOG PS 0-2の切除不能進行・再発大腸癌患者であり、原発部位 (結腸/直腸)、前治療 (術後補助療法あり/なし)、病変の状況 (測定可能/評価可能) を割付け調整因子として、SOX群とCapeOX群に無作為に割り付けられた。なお、SOX療法は、S-1 (80mg/m2/day, day 1-14) + L-OHP (130mg/m2, day 1)、CapeOX療法はCapecitabine (2,000mg/m2/day, day 1-14) + L-OHP (130mg/m2, day 1) で、3週毎に増悪するまで繰り返し投与した。
結果
ITT集団は340例 (SOX群168例、CapeOX群172例) で、両群の背景に差はみられなかった (表1)。
表1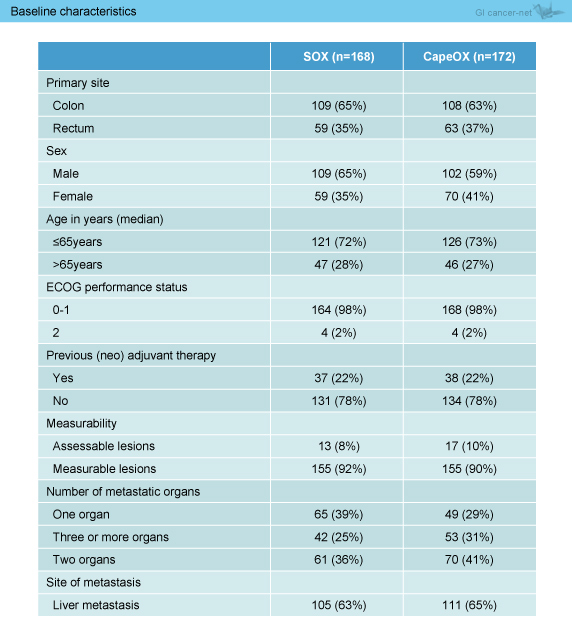
更新されたPFS中央値は、SOX群7.1ヵ月、CapeOX群6.3ヵ月 (p=0.10) であった (前回報告時:8.5ヵ月 vs. 6.7ヵ月, p=0.09)。
また、更新されたOS中央値は、SOX群19.0ヵ月、CapeOX群18.5ヵ月 (p=0.19) であった (前回報告時:21.2ヵ月 vs. 20.5ヵ月, p=0.18) (図1)。
図1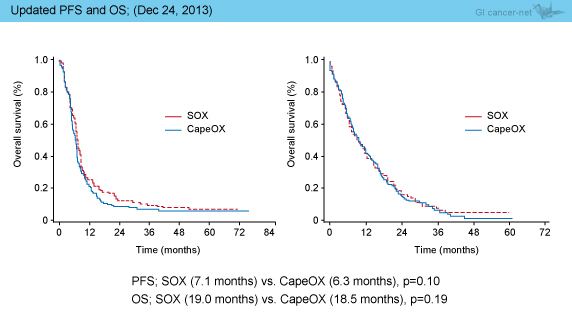
サブグループ解析では、OS、PFSともに患者背景因子別においても有意差を認めなかった (図2)。
図2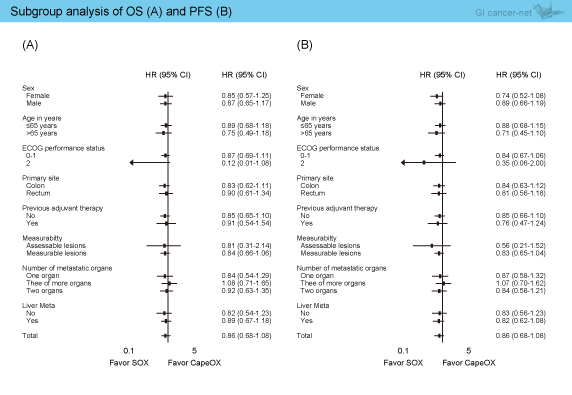
結論
更新された生存解析においてSOX療法とCapeOX療法の結果は同等であった。当初のPFS解析を確定するものであり、SOX療法は切除不能進行・再発大腸癌の1st-lineにおける2剤併用療法レジメンとして置き換わり得るだろう。
コメント
CapeOX療法に対するSOX療法の非劣性試験のupdateが報告された。前回の報告では、PFSがSOX療法において約2ヵ月延長していることが注目されたが、今回の追加解析では、両群類似した結果に落ち着いていることが興味深い。CapeOX療法はFOLFOX療法に対する非劣性が既に証明されており(NO16966 試験)、これでFOLFOX療法、CapeOX療法、SOX療法のいずれも生存延長と忍容性について、すべて同等に期待ができる。
この結果は実臨床での感覚に近いものがあり、エビデンスとして納得しやすい。SOX療法は、同日報告されたSOFT試験のupdate2) の結果よりBevacizumab併用においても同様の結果は得られており、標準1st-lineの選択肢となる。今回は毒性の検討報告はされていないが、前回の解析報告では両群において副作用プロファイルが若干異なっていた。実臨床では、それぞれの薬剤の特性を踏まえ、2nd-line以降の戦略を立てた上で、選択することになる。
(レポート:坂井 大介 監修・コメント:佐藤 温)
- Reference

