ESMO 2014 Congress
大腸癌
Abstract #546P/548P
切除不能進行・再発大腸癌に対する2nd-lineとしてFOLFIRI ± Panitumumabを検討した20050181試験のRAS 野生型における腫瘍縮小/ベースライン因子による解析
20050181試験では、KRAS exon 2野生型の切除不能進行・再発大腸癌に対する2nd-lineとしてFOLFIRI ± Panitumumabを検討した結果、PFSで有意な延長、OSでは良好な傾向を認めており、今年の消化器癌シンポジウムおよび米国臨床腫瘍学会年次集会においては、RAS 野生型では群間差が広がることが報告されていた。今回は、RAS 野生型における腫瘍縮小についての解析 (#546P) と、ベースライン因子による解析 (#548P) が発表されたので、併せてレポートする。
Expert's view

仁科 智裕 先生
国立病院機構
四国がんセンター
消化器内科
本研究は20050181試験のRAS 野生型の症例における腫瘍縮小とベースライン因子を検討したものであるが、FOLFIRI + Panitumumabの有効性の特徴が示唆されているものと思われる。#546Pの報告では、 Panitumumab群においては奏効率41%、8週以内に30%以上の腫瘍縮小が約4割に認められ、腫瘍量のベースラインからの変化率も56週にわたって優れるというものであった。奏効が得られにくい2nd-lineの結果としては非常に良好で魅力的なものである。2nd-lineにおいては腫瘍による有症状例が少なからずおり、その場合の治療選択には早期に腫瘍縮小が期待できるレジメンが望ましい。FOLFIRI + Panitumumabはそのような症例には間違いなく適したレジメンであると思われる。
また、#548Pの報告では、ベースライン因子にかかわらずPanitumumab併用の有効性が示唆されていることから、早期の腫瘍縮小を求めないような症例に対しても選択肢にはなると思われるが、Bevacizumab併用レジメンとの使い分けが悩ましくなる。今後、head-to-headの無作為化比較第II相試験であるSPIRITT試験やWJOG6210G試験において検討がなされ、両剤の使い分のためのベースライン因子やバイオマーカー等の報告がなされることを期待したい。
大腸癌
Abstract #546P
2nd-lineとしてのFOLFIRI + Panitumumab vs. FOLFIRIにおける腫瘍縮小と奏効によるアウトカム
Tumour Shrinkage and Response Outcomes during Second-line Panitumumab + FOLFIRI vs. FOLFIRI Treatment
Marc Peeters, et al.

切除不能進行・再発大腸癌の1st-lineにおいては、早期腫瘍縮小と奏効が得られれば外科的切除の可能性が高くなることが報告されている。一方、2nd-lineにおいては、早期腫瘍縮小と奏効が症状軽減と進行遅延の面でベネフィットをもたらす可能性がある。
そこで、2nd-lineにおいてFOLFIRI ± Panitumumabを検討した20050181試験のRAS 野生型患者の腫瘍縮小と奏効によるアウトカムについて解析した。
そこで、2nd-lineにおいてFOLFIRI ± Panitumumabを検討した20050181試験のRAS 野生型患者の腫瘍縮小と奏効によるアウトカムについて解析した。
20050181試験に参加したKRAS exon 2野生型患者の腫瘍サンプルを用いて、双方向性のサンガー法とWAVE-based SURVEYOR® Scan Kitにより、KRAS exon 3, 4、NRAS exon 2, 3, 4およびBRAF exon 15の遺伝子解析を行った。また、各治療の奏効率と奏効期間、奏効の深さ (deepness of response: DpR)、腫瘍量 (標的病変の最長径和) のベースラインからの変化率などを計測した。
1,186例が無作為化され、1,014例でRAS statusが判定された。KRAS exon 2野生型597例中107例 (18%) で、いずれかのRAS 変異が認められた。
RAS 野生型421例のベースラインの患者背景や疾患特性は、原発巣はPanitumumab群 (208例) で直腸癌、FOLFIRI群 (213例) で結腸癌が多く、後治療で抗EGFR抗体薬を投与した患者はFOLFIRI群で多かったものの、両群でバランスがとれていた。
奏効率は、Panitumumab群41%、FOLFIRI群10%であり、Panitumumab群で良好であった (表1)。奏効期間中央値はそれぞれ7.7ヵ月、9.3ヵ月であったが、DpR中央値はそれぞれ37%、10%でPanitumumab群が有意に良好であった (p<0.0001)。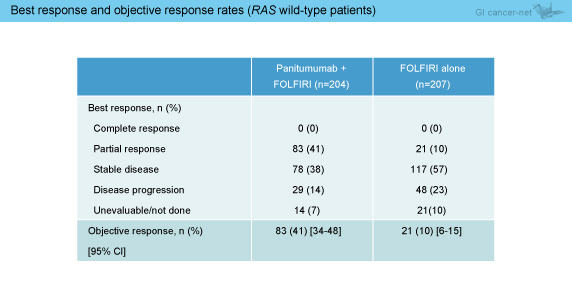 治療開始から56週間における腫瘍量のベースラインからの変化率は、Panitumumab群がFOLFIRI群に比べて一貫して優れていた (図1)。
治療開始から56週間における腫瘍量のベースラインからの変化率は、Panitumumab群がFOLFIRI群に比べて一貫して優れていた (図1)。
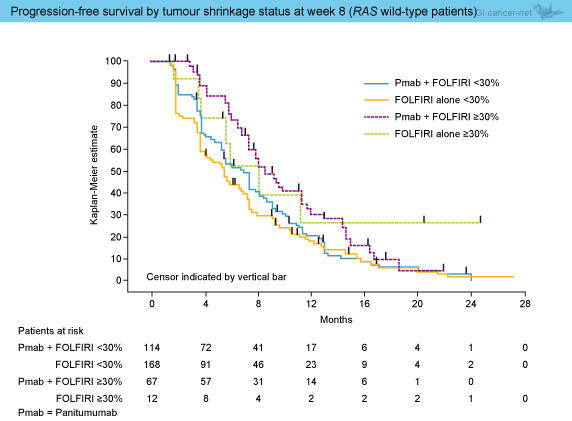
8週時点で30%以上の腫瘍縮小を得た症例は、Panitumumab群37%、FOLFIRI群7%であり、Panitumumab群で多かった。また、8週時点で30%以上の腫瘍縮小を得た症例は、30%未満であった症例に比べ、両群ともにPFSが延長し、8週時点における30%の腫瘍縮小にかかわらず、PFSはPanitumumab群がFOLFIRI群より良好であった (図2)。
なお、治療後に外科的切除を受けた症例も、Panitumumab群7例 (3%)、FOLFIRI群2例 (1%) であり、Panitumumab群で多かった。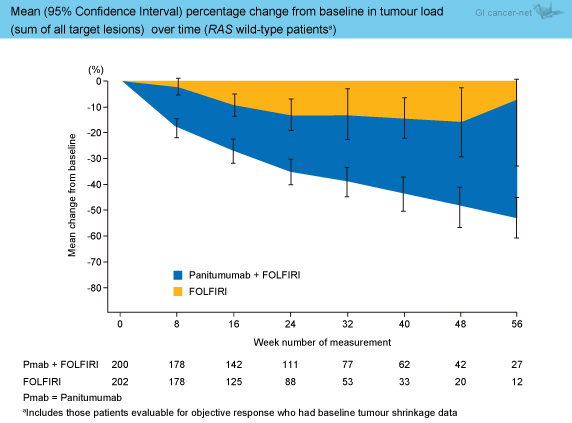
RAS 野生型421例のベースラインの患者背景や疾患特性は、原発巣はPanitumumab群 (208例) で直腸癌、FOLFIRI群 (213例) で結腸癌が多く、後治療で抗EGFR抗体薬を投与した患者はFOLFIRI群で多かったものの、両群でバランスがとれていた。
奏効率は、Panitumumab群41%、FOLFIRI群10%であり、Panitumumab群で良好であった (表1)。奏効期間中央値はそれぞれ7.7ヵ月、9.3ヵ月であったが、DpR中央値はそれぞれ37%、10%でPanitumumab群が有意に良好であった (p<0.0001)。
表1

8週時点で30%以上の腫瘍縮小を得た症例は、Panitumumab群37%、FOLFIRI群7%であり、Panitumumab群で多かった。また、8週時点で30%以上の腫瘍縮小を得た症例は、30%未満であった症例に比べ、両群ともにPFSが延長し、8週時点における30%の腫瘍縮小にかかわらず、PFSはPanitumumab群がFOLFIRI群より良好であった (図2)。
なお、治療後に外科的切除を受けた症例も、Panitumumab群7例 (3%)、FOLFIRI群2例 (1%) であり、Panitumumab群で多かった。
図1

図2

RAS 野生型の切除不能進行・再発大腸癌の2nd-lineにおいてFOLFIRIにPanitumumabを併用することで奏効率が30%改善し、8週時点で30%以上の腫瘍縮小を得た症例もPanitumumab群で多かった。また、2nd-lineにおける早期腫瘍縮小はPFS延長と関連すると考えられた。以上より、RAS 野生型においてFOLFIRI + PanitumumabはFOLFIRIに比べ、より早く、より深い奏効を示すと考えられた。
大腸癌
Abstract #548P
2nd-lineにおけるFOLFIRI + Panitumumab vs. FOLFIRI の有効性に対するベースライン因子および前治療の影響
Impact of Baseline Covariates and Prior Therapy on the Efficacy of Second-line Panitumumab + FOLFIRI vs. FOLFIRI Treatment
Marc Peeters, et al.

RAS 野生型の切除不能進行・再発大腸癌においては、1st-lineでFOLFOX4 + PanitumumabがFOLFOX4に比べてPFSとOSを改善することが報告されており1)、20050181試験では、2nd-lineでFOLFIRI + PanitumumabがFOLFIRIに比べてPFSとOSを改善することが示され2)、全RAS 検査の重要性が裏付けられた。
今回、20050181試験におけるRAS 野生型患者のサブグループ解析を行い、治療の有効性に対するベースライン因子や前治療の影響を検討した。
今回、20050181試験におけるRAS 野生型患者のサブグループ解析を行い、治療の有効性に対するベースライン因子や前治療の影響を検討した。
今回、20050181試験のRAS 野生型患者を対象として、層別化因子 (ECOG PS 0/1 vs. 2、Oxaliplatin (L-OHP) 治療歴の有無、Bevacizumab治療歴の有無)、事前に定めたベースライン因子 (年齢、BRAF status)、およびその他の因子 (BMI、肝限局転移 vs. その他転移、術後補助療法の完遂からPDまでの期間6ヵ月以内 vs. 6ヵ月超) について、PFSとOSのサブグループ解析を行った。
1,186例が無作為化され、1,014例でRAS statusが判定された。KRAS exon 2野生型597例中107例 (18%) で、いずれかのRAS 変異が認められた。
RAS 野生型421例において、両群の患者背景はバランスがとれていた。RAS 野生型におけるPFS中央値は、Panitumumab群6.4ヵ月、FOLFIRI群4.6ヵ月であり、Panitumumab群で有意に良好であった (HR=0.70, 95% CI: 0.54-0.91, p=0.007)。PFSに関するサブグループ解析では、中央値はすべてのサブグループでPanitumumab群が良好であり (表2)、ハザード比に基づくと、術後補助療法の完遂からPDまでの期間が6ヵ月超の症例以外のすべてのサブグループでPanitumumab群が良好であった。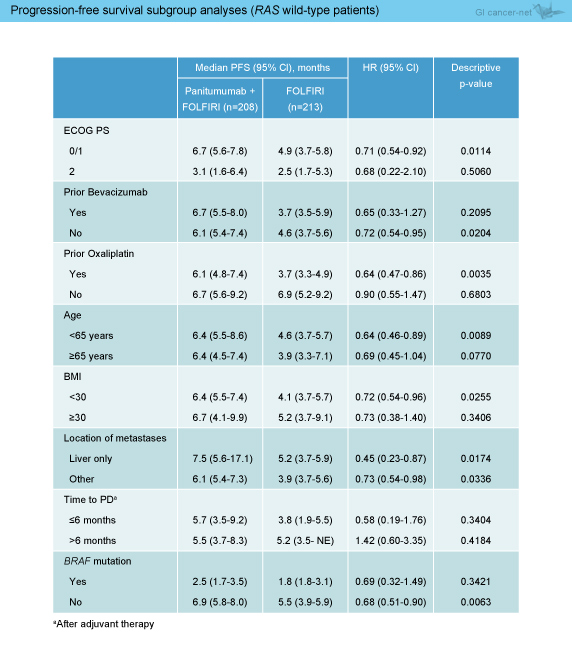 RAS 野生型におけるOS中央値は、Panitumumab群16.2ヵ月、FOLFIRI群13.9ヵ月であり、Panitumumab群で良好な傾向がみられた (HR=0.81, 95% CI: 0.63-1.03, p=0.08)。OSに関するサブグループ解析では、中央値はECOG PS 2およびBRAF 変異型以外のすべてのサブグループでPanitumumab群が良好であり (表3)、ハザード比に基づくと、BMI30以上および術後補助療法の完遂からPDまでの期間が6ヵ月超の症例以外のすべてのサブグループでPanitumumab群が良好であった。
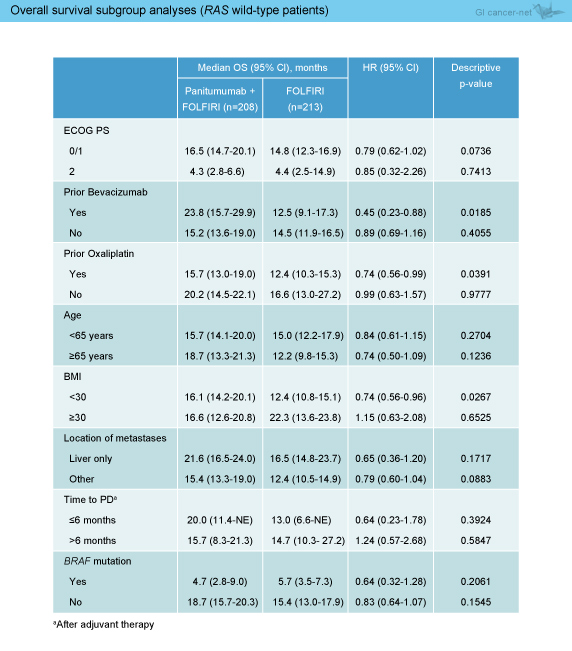
RAS 野生型におけるOS中央値は、Panitumumab群16.2ヵ月、FOLFIRI群13.9ヵ月であり、Panitumumab群で良好な傾向がみられた (HR=0.81, 95% CI: 0.63-1.03, p=0.08)。OSに関するサブグループ解析では、中央値はECOG PS 2およびBRAF 変異型以外のすべてのサブグループでPanitumumab群が良好であり (表3)、ハザード比に基づくと、BMI30以上および術後補助療法の完遂からPDまでの期間が6ヵ月超の症例以外のすべてのサブグループでPanitumumab群が良好であった。
 Grade 3/4の有害事象は、いずれのサブグループにおいてもFOLFIRI群に比べてPanitumumab群のほうが高く、同治療群内におけるベースライン因子毎の比較では、いずれの因子においても同様であった。
Grade 3/4の有害事象は、いずれのサブグループにおいてもFOLFIRI群に比べてPanitumumab群のほうが高く、同治療群内におけるベースライン因子毎の比較では、いずれの因子においても同様であった。
RAS 野生型421例において、両群の患者背景はバランスがとれていた。RAS 野生型におけるPFS中央値は、Panitumumab群6.4ヵ月、FOLFIRI群4.6ヵ月であり、Panitumumab群で有意に良好であった (HR=0.70, 95% CI: 0.54-0.91, p=0.007)。PFSに関するサブグループ解析では、中央値はすべてのサブグループでPanitumumab群が良好であり (表2)、ハザード比に基づくと、術後補助療法の完遂からPDまでの期間が6ヵ月超の症例以外のすべてのサブグループでPanitumumab群が良好であった。
表2

表3

RAS 野生型の切除不能進行・再発大腸癌に対する2nd-lineとしてのFOLFIRI + Panitumumabは、FOLFIRI単独に比べて大部分のサブグループで良好なPFSとOSを示した。ECOG PS 2のOS中央値は両群で同様であったが、サンプルサイズが小さいため、結論付けることはできない。なお、BRAF 変異型は2nd-lineにおいても予後不良因子であったが、効果予測因子とはならなかった。
1) Douillard JY, et al.: N Engl J Med. 369(11), 1023-1034, 2013 [PubMed]
2) Peeters M, et al.: 2014 Annual Meeting of the American Society of Clinical Oncology®: abstr #3568
2) Peeters M, et al.: 2014 Annual Meeting of the American Society of Clinical Oncology®: abstr #3568
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。

