Abstract #11
RAINBOW試験の年齢グループによる解析:1st-lineとしてプラチナ製剤およびフッ化ピリミジン系製剤を含む併用療法施行後に病勢進行となった胃および胃食道接合部腺癌に対するPaclitaxelへのRamucirumabの上乗せ効果を検討した国際二重盲検第III相試験
RAINBOW: A Global, Phase 3, Double-blind Study of Ramucirumab (RAM) Plus Paclitaxel (PTX) Versus Placebo (PL) + PTX in the Treatment of Advanced Gastric and Gastroesophageal Junction (GEJ) Adenocarcinoma Following Disease Progression on First-line Platinum- and Fluoropyrimidine-Containing Combination Therapy: An Age-Group Analysis
Kei Muro, et al.
高齢者においても有効性、安全性が確認
高齢者に抗癌剤を投与する際に問題になるのが、毒性の増加に見合った効果が得られるのか?という点である。高齢の患者では骨髄抑制、殊に発熱性好中球減少 (FN) や、血栓、塞栓のイベント増加が懸念され、それらの懸念に見合った臨床的有用性が期待できるかが重要である。
本試験では、65歳で区切った際における年齢による有効性の違いは、ほぼみられなかった。また、致死的なイベントにおいても、年齢、治療アームによる差が認められていない点は、この治療の使いやすさを示唆している。血栓症を来しやすい胃癌であるにもかかわらず、高齢者のRamucirumab群でもプラセボ群と変わらない点は、安全性の面で高く評価できる。臨床試験のためPSの良好な若い患者が中心となっていても、高齢者における安全性と有効性が確認されたことは、胃癌の発症年齢が高齢にシフトしてきている日本において有用なデータである。
しかしながら、5%以下ではあるが、FNは65歳以上のRamucirumab群で多くみられる傾向があり、注意が必要である。早晩、上市が見込まれるが、実臨床に導入された際には、やはり高齢者のFNの増加には注意をしながら使用すべきである。また、さらに70歳、75歳以上の高齢者のデータを早期に集積することが望まれる。
背景と目的
Ramucirumabは、ヒト免疫グロブリンG1 (IgG1) モノクローナル抗体薬で、血管内皮増殖因子 (VEGF) 受容体-2 (VEGFR-2) の拮抗薬であり、最近、切除不能胃および胃食道接合部腺癌に対する2nd-lineとして、単剤またはPaclitaxel (PTX) との併用で米国FDAにより承認された
1-3)。
RAINBOW試験は、胃および胃食道接合部腺癌を対象に、プラチナ製剤およびフッ化ピリミジン系製剤ベースの併用化学療法を施行後に病勢が進行した患者に対する2nd-lineとして、PTXに対するRamucirumabの上乗せ効果を検討したプラセボ対照無作為化第III相試験であり、Ramucirumab併用によりOS、PFS、奏効率が有意に改善することが示されている
4. 5)。
今回は、
RAINBOW試験における年齢別 (65歳未満、65歳以上) の有効性および安全性の解析を行った。
対象と方法
対象は、年齢18歳以上、ECOG PS 0/1で、プラチナ製剤 + フッ化ピリミジン系製剤ベースの併用化学療法による1st-line治療中または最終投与後4ヵ月以内に病勢進行した、胃癌および胃食道接合部腺癌患者であった。Ramucirumab (8mg/kg, day 1, 15) + PTX (80mg/m2, day 1, 8, 15) を投与する群 (Ramucirumab群) またはプラセボ + PTXを投与する群 (プラセボ群) に無作為に割り付けられ、増悪または忍容できない有害事象が発生するまで投与された。なお、主要評価項目はOS、副次評価項目はPFS、奏効率であった。
結果
無作為化された665例 (Ramucirumab群330例、プラセボ群335例) のうち、65歳未満は416例 (Ramucirumab群204例、プラセボ群212例)、65歳以上は249例 (それぞれ126例、123例) であり、患者背景は年齢および治療群間でバランスがとれていたが、65歳以上では65歳未満に比べ、intestinal typeおよび1st-lineの治療期間が6ヵ月以上の患者が多かった。
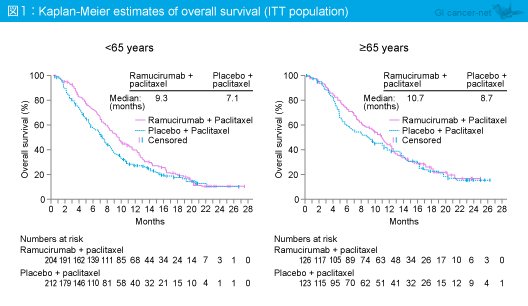
OS中央値は、65歳未満でRamucirumab群9.3ヵ月、プラセボ群7.1ヵ月 (HR=0.753, 95% CI: 0.604-0.939, p=0.0112)、65歳以上でそれぞれ10.7ヵ月、8.7ヵ月 (HR=0.861, 95% CI: 0.636-1.165, p=0.3394) と、Ramucirumab群はプラセボ群に対して65歳未満では有意に良好であり、65歳以上でも良好な傾向がみられた (図1)。
同様に奏効率は、65歳未満でRamucirumab群28.4%、プラセボ群14.2% (OR=2.66, 95% CI: 1.60-4.44, p<0.0001)、65歳以上でそれぞれ27.0%、19.5% (OR=1.55, 95% CI: 0.85-2.85, p=0.1529) と、Ramucirumab群は65歳未満では有意に良好であり、65歳以上でも良好な傾向がみられた。
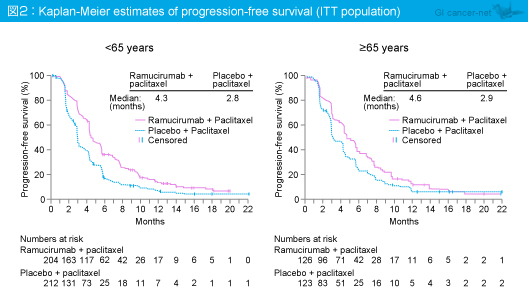
PFS中央値は、65歳未満でRamucirumab群4.3ヵ月、プラセボ群2.8ヵ月 (HR=0.572, 95% CI: 0.460-0.711, p<0.0001)、65歳以上でそれぞれ4.6ヵ月、2.9ヵ月 (HR=0.673, 95% CI: 0.506-0.894, p=0.0066) と、Ramucirumab群はプラセボ群に対して65歳未満、65歳以上いずれも有意に良好であった (図2)。
治療期間や治療サイクル数、相対用量強度は、いずれも65歳未満、65歳以上で違いは認められなかった。同様に、用量調節、有害事象による治療中止においても、年齢別の差はほぼみられなかったが、PTXの用量調節は65歳以上で多くみられた。
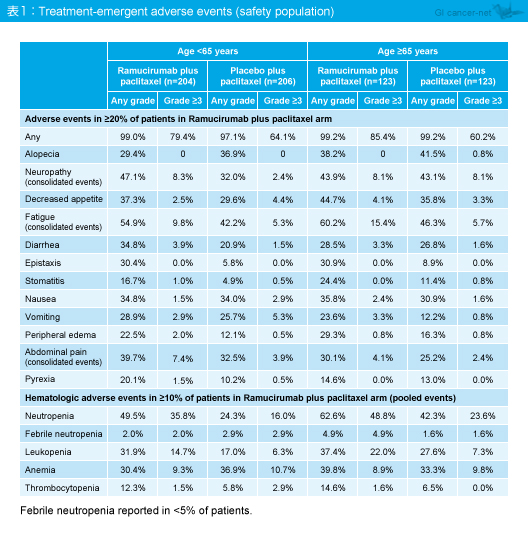
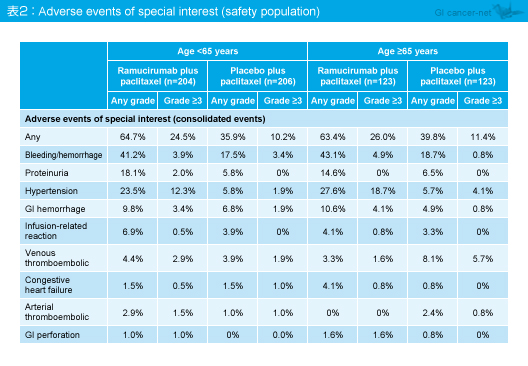
毒性プロファイルは65歳未満、65歳以上で類似していたが、grade 3以上の好中球減少および白血球減少は65歳以上で高い傾向が認められた (表1)。好中球減少は主にPTXの用量調節で管理可能であり、発熱性好中球減少症の頻度は年齢を問わず5%未満であった。なお、特に注目すべき有害事象においても年齢による違いは認められなかった (表2)。
結論
PTXに対するRamucirumabの上乗せ効果は65歳未満、65歳以上ともに認められ、OS、PFS、奏効率いずれもRamucirumab群で良好であった。また、毒性プロファイルも年齢による差はほとんどみられなかった。
Reference
1) Ku GY, et al.: Curr Opin Gastroenterol. 30(6): 596-602, 2014[
PubMed]
2) Poole RM, et al.: Drugs. 74(9): 1047-1058, 2014[
PubMed]
3) Spratlin J: Curr Oncol Rep. 13(2): 97-102, 2011[
PubMed]
4) Wilke H, et al.: Lancet Oncol. 15(11): 1224-1235, 2014[
PubMed]
5) Aprile G, et al.: Onco Targets Ther., 7: 1997-2006, 2014[
PubMed]