
|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。 |
RAINBOW試験:プラチナ製剤 + フッ化ピリミジン系製剤を含む併用化学療法施行後に病勢が進行した切除不能胃および胃食道接合部腺癌に対するRamucirumab + Paclitaxel vs. placebo + Paclitaxelの国際共同二重盲検無作為化第III相試験
RAINBOW: a Global, Phase 3, Randomized, Double-blind Trial of Ramucirumab and Paclitaxel (PTX) versus Placebo and PTX in the Treatment of Metastatic Gastric or Gastroesophageal Junction (GEJ) Adenocarcinoma Following Disease Progression on First-line Platinum- and Fluoropyrimidine-Containing Combination Therapy
Hansjochen Wilke, et al.

胃癌2nd-lineにおける新たな治療として期待

主要評価項目のOSだけでなく、PFS、奏効率でもPaclitaxelに対する上乗せ効果が認められており、文句のつけようのない結果である。
今後明らかにしてほしい関心事として以下の7点を挙げる。①Bevacizumabが1st-lineにおけるXP (Capecitabine + Cisplatin) 療法との併用でnegativeな結果になった2)ことを考えると、Ramucirumabを1st-lineで使用するのは適切か。②その際の併用レジメンは。③Bevacizumabも2nd-lineで開発していれば成功していたのではないか。④VEGF-Aを標的とすることと、VEGFR-2を標的とすることに生物学的な違いがあるのか。⑤今回の試験でpredictive biomarkerが同定され得るのか。⑥3rd-lineでCPT-11等との併用によりbeyond progressionを行うことで、生存期間の上乗せがみられるのか。⑦HER2陽性の2nd-lineの患者に対し、Trastuzumabを選択すべきなのか、本薬剤を選択すべきなのか (Trastuzumab beyond progressionのデータはないが) 。
臨床的現場からの観点では、奏効率の上乗せが明瞭であることから、腫瘍縮小による症状緩和が望まれるような2nd-lineの対象に対しても効果が期待でき、一日も早い承認が望まれる。
プラチナ製剤 + フッ化ピリミジン系製剤ベースの化学療法による1st-line施行後に増悪した胃および胃食道接合部腺癌に対する2nd-line治療のOS中央値は約5ヵ月と短く3-5)、新規の有効な治療法の開発が求められている。VEGFR-2等の血管新生に関わる増殖因子受容体およびそのリガンドは胃癌の病因に関与していると考えられており、胃癌の重要な治療標的となる可能性がある6)。また、最近報告された無作為化試験により、weekly PaclitaxelはCPT-11やDocetaxelなど2nd-lineで使用される他の薬剤に対して、同程度の有効性および良好な忍容性が示されている7)。
RAINBOW試験は、胃癌患者に対する2nd-lineにおいて、VEGFR-2に対する拮抗作用を有するヒトIgG1モノクローナル抗体薬であるRamucirumabとPaclitaxel併用療法の有効性を検討する、国際共同二重盲検無作為化第III相試験である。
RAINBOW試験は、胃癌患者に対する2nd-lineにおいて、VEGFR-2に対する拮抗作用を有するヒトIgG1モノクローナル抗体薬であるRamucirumabとPaclitaxel併用療法の有効性を検討する、国際共同二重盲検無作為化第III相試験である。
対象は、ECOG PS 0-1でプラチナ製剤 + フッ化ピリミジン系製剤ベースの併用化学療法による1st-line施行中または終了後4ヵ月以内にPDとなった、胃癌および胃食道接合部腺癌患者である。Ramucirumab (8mg/kg, day 1, 15) + Paclitaxel (80mg/m2, day 1, 8, 15) を投与する群 (RAM + PTX群) とplacebo (day 1, 15) + Paclitaxel (80mg/m2, day 1, 8, 15) を投与する群 (PBO + PTX群) とに無作為に割り付けられ、増悪または忍容できない有害事象が発生するまで投与された (図1)。また、地域 (欧州/米国/豪州, 中南米, アジア) 、測定可能病変の有無、1st-line治療のTTP (time to progression) (6ヵ月未満 vs. 6ヵ月以上) で層別化された。
主要評価項目はOS、副次評価項目はPFS、TTP、客観的奏効率、安全性などであった。OS中央値をRAM + PTX群9.33ヵ月、PBO + PTX群7.0ヵ月と仮定し (HR=0.75) 、検出力90%で、663例510イベントが必要とされた。
主要評価項目はOS、副次評価項目はPFS、TTP、客観的奏効率、安全性などであった。OS中央値をRAM + PTX群9.33ヵ月、PBO + PTX群7.0ヵ月と仮定し (HR=0.75) 、検出力90%で、663例510イベントが必要とされた。
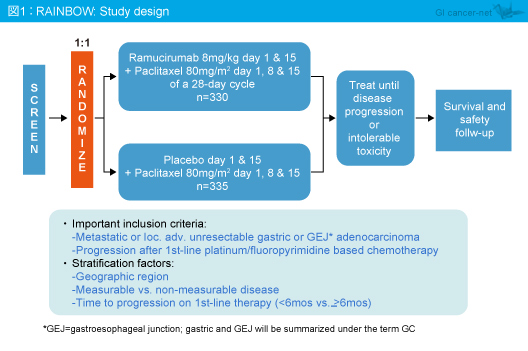
2010年12月〜2012年9月の間に27ヵ国170施設から665例 (日本140例) が登録され、RAM + PTX群330例、PBO + PTX群335例に割り付けられた。なお、ベースラインの患者背景は両群でバランスがとれていた。
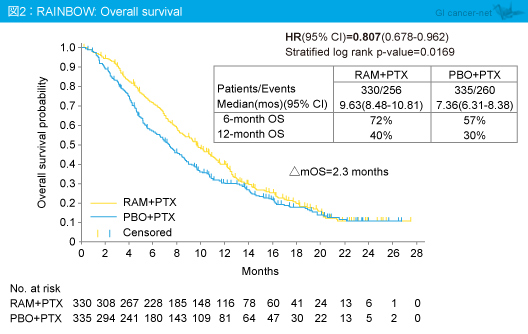
主要評価項目のOS中央値はRAM + PTX群9.63ヵ月、PBO + PTX群7.36ヵ月であり、Ramucirumab併用による有意な延長が認められた (HR=0.807, 95% CI: 0.678-0.962, p=0.0169) (図2)。また、OSのサブグループ解析では、大部分のサブグループでRAM + PTX群が良好であった。
主要評価項目のOS中央値はRAM + PTX群9.63ヵ月、PBO + PTX群7.36ヵ月であり、Ramucirumab併用による有意な延長が認められた (HR=0.807, 95% CI: 0.678-0.962, p=0.0169) (図2)。また、OSのサブグループ解析では、大部分のサブグループでRAM + PTX群が良好であった。
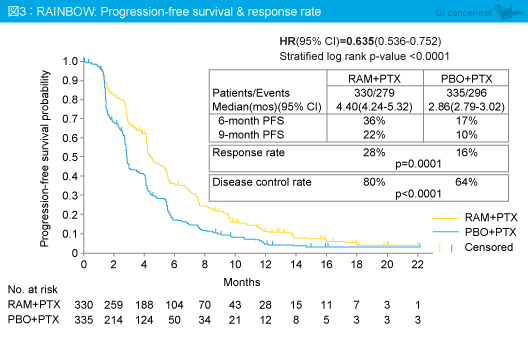
PFS中央値はRAM + PTX群4.40ヵ月、PBO + PTX群2.86ヵ月であり、Ramucirumab併用により有意に延長し (HR=0.635, 95% CI: 0.536-0.752, p<0.0001) (図3)、PFSのサブグループ解析においては、大部分のサブグループでRAM + PTX群が有意に良好であった。また、奏効率はRAM + PTX群28%、PBO + PTX群16% (p=0.0001) 、病勢コントロール率はRAM + PTX群80%、PBO + PTX群64% (p<0.0001) であり、いずれもRAM + PTX群で有意に良好だった。
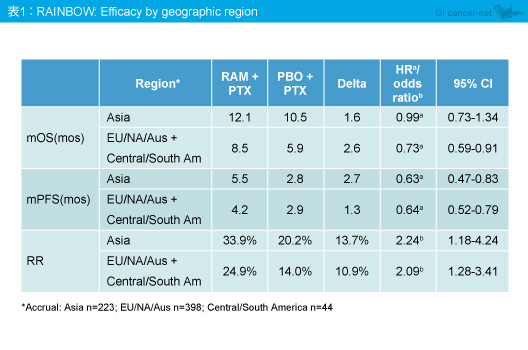
地域別の解析 (アジアとアジア以外) では、OS中央値、PFS中央値、奏効率はいずれも全般に良好な傾向がみられた。しかし、アジア以外のOS中央値は、RAM + PTX群8.5ヵ月、PBO + PTX群5.9ヵ月とRAM + PTX群で有意に延長したのに対し (HR=0.73, 95% CI: 0.59-0.91) 、アジアではRAM + PTX群12.1ヵ月、PBO + PTX群10.5ヵ月であり、有意差を認めなかった (HR=0.99, 95% CI: 0.73-1.34) (表1)。
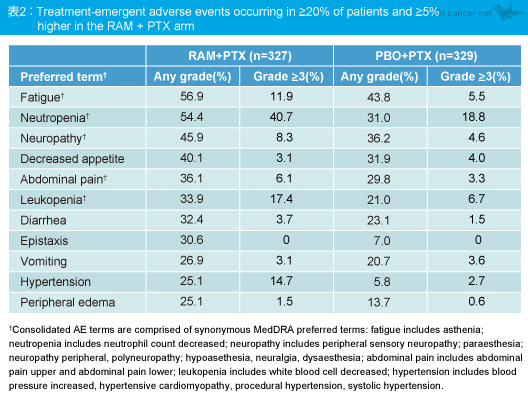
治療下で発現した有害事象は倦怠感、好中球減少、神経障害、食欲不振などがRAM + PTX群で多くみられ (表2)、好中球減少はgrade 3 (22 vs. 16%) 、grade 4 (19 vs. 3%) いずれもRAM + PTX群で多くみられた。なお、発熱性好中球減少症は両群とも低く同程度であった (3.1 vs. 2.4%) 。
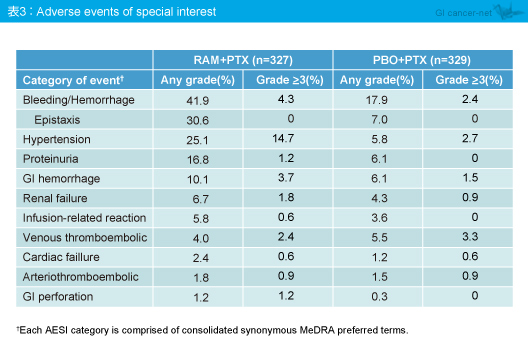
RAM + PTX群で特に留意すべき有害事象としては、出血、高血圧、蛋白尿、消化管出血などの頻度が高く、出血のなかでも鼻出血の頻度が高かった (表3)。また、担当医判定の有害事象による死亡は、両群で同程度だった (4.0 vs. 4.6%) 。
RAM + PTX群で特に留意すべき有害事象としては、出血、高血圧、蛋白尿、消化管出血などの頻度が高く、出血のなかでも鼻出血の頻度が高かった (表3)。また、担当医判定の有害事象による死亡は、両群で同程度だった (4.0 vs. 4.6%) 。
RAM + PTX群はPBO + PTX群に対して、臨床的に意味のある2ヵ月以上のOS延長をもたらし、死亡リスクを19%低減させた。最近、論文化されたREGARD試験の成果を併せて考慮すると、化学療法施行後の切除不能胃癌および胃食道接合部腺癌患者に対して、Ramucirumabが有効であることが認められ、効果的な2nd-line治療は切除不能胃癌患者に対してOSの延長をもたらすことが明確に示された。
Reference
1) Fuchs CS, et al.: Lancet. 383(9911): 31-39, 2014 [PubMed]
2) Ohtsu A, et al.: J Clin Oncol. 29(30): 3968-3976, 2011 [PubMed]
3) Thuss-Patience PC, et al.: Eur J Cancer. 47(15): 2306-2314, 2011 [PubMed]
4) Kang JH, et al.: J Clin Oncol. 30(13): 1513-1518, 2012 [PubMed]
5) Ford HE, et al.: Lancet Oncol. 15(1): 78-86, 2014 [PubMed]
6) Clarke JM, et al.: Expert Opin Biol Ther. 13(8): 1187-1196, 2013 [PubMed]
7) Hironaka S, et al.: J Clin Oncol. 31(35): 4438-4444, 2013 [PubMed]
1) Fuchs CS, et al.: Lancet. 383(9911): 31-39, 2014 [PubMed]
2) Ohtsu A, et al.: J Clin Oncol. 29(30): 3968-3976, 2011 [PubMed]
3) Thuss-Patience PC, et al.: Eur J Cancer. 47(15): 2306-2314, 2011 [PubMed]
4) Kang JH, et al.: J Clin Oncol. 30(13): 1513-1518, 2012 [PubMed]
5) Ford HE, et al.: Lancet Oncol. 15(1): 78-86, 2014 [PubMed]
6) Clarke JM, et al.: Expert Opin Biol Ther. 13(8): 1187-1196, 2013 [PubMed]
7) Hironaka S, et al.: J Clin Oncol. 31(35): 4438-4444, 2013 [PubMed]
