|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。
|

日本人治癒切除不能進行・再発大腸癌患者におけるPanitumumabの製造販売後調査:最終報告
Final Report of Post-Marketing Survey of Panitumumab in Japanese Patients with Unresectable Advanced or Recurrent Colorectal Cancer
Tetsuya Hamaguchi, et al.

抗EGFR抗体薬は、日本に完全に根付いたか

副作用としてもっとも多く認められ臨床現場でも時にマネジメントが困難となる、皮膚障害の頻度・程度、そして時に致死的となるILDの頻度・程度は、既報の臨床試験やもう一方の抗EGFR抗体薬 (Cetuximab) の結果とほぼ同様であり、予想通りinfusion reactionの発現率はCetuximabより明らかに低かった。
今回の製造販売後調査は、Cetuximabが広く使われるようになってからのものであり、このたび報告された安全性と有効性のデータから、わが国で、進行大腸癌症例における抗EGFR抗体薬が、完全に根付いた治療として適正に施行されていることを物語る結果と言える。その他、低マグネシウム血症のみならず、低カルシウム血症、低カリウム血症などの複合的な電解質異常を来しうることに注意が必要である。また、決して高い頻度ではないものの、ILDを1.3%に認め、0.6%が死亡に至っている点については、実地臨床での使用において、特別な留意が必要であるのは言うまでもない。
上皮成長因子受容体 (EGFR: epidermal growth factor receptor) は、大腸癌をはじめとした多くの癌腫の治療において重要な標的である1)。PanitumumabはEGFRを特異的に標的とする完全ヒト型IgG2モノクローナル抗体であり2)、KRAS 野生型の切除不能進行・再発大腸癌における1st-lineから3rd-line治療以降まで、単剤または細胞毒性抗癌剤との併用療法で使用され、良好な治療成績と忍容性を示している。
日本においては2010年4月に承認されたが、臨床試験への日本人症例の登録が限られていたため、製造販売後調査として日本人患者における全例調査が行われた。
日本においては2010年4月に承認されたが、臨床試験への日本人症例の登録が限られていたため、製造販売後調査として日本人患者における全例調査が行われた。
製造販売後調査として2010年6月よりPanitumumab投与全例調査が開始され、2010年11月までに登録された患者のデータに対する最終解析が行われた。なお、皮膚障害、電解質異常、infusion reaction、間質性肺疾患 (ILD)、心毒性が重点調査項目として調査された。
患者背景
適応条件を満たした3,091例が登録され、そのうちPanitumumabが投与された3,085例についての最終報告を行った。ベースライン時の患者背景は表1の通りであり、KRAS 変異型への投与は3例、ECOG PS 4への投与は3例であった。
適応条件を満たした3,091例が登録され、そのうちPanitumumabが投与された3,085例についての最終報告を行った。ベースライン時の患者背景は表1の通りであり、KRAS 変異型への投与は3例、ECOG PS 4への投与は3例であった。
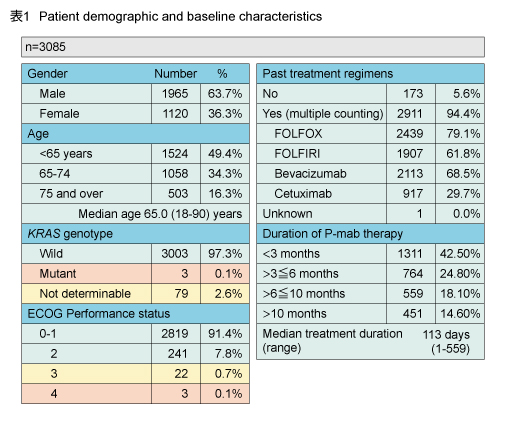
治療ラインの割合は1st-line10.0%、2nd-line17.6%、3rd-line以降72.4%であり、Panitumumabを含む治療レジメンは併用療法が半数以上を占めた。治療ライン別の選択された頻度の高かったレジメン内容は、1st-lineではFOLFOX (62.3%)、2nd-lineではFOLFIRI (50.8%)、3rd-line以降ではPanitumumab単独 (47.6%) であった。
安全性
全体の副作用発現率は84.1%であり、重点調査項目の皮膚障害、電解質異常、infusion reaction、ILD、心毒性の発現率は図1の通りであった。
安全性
全体の副作用発現率は84.1%であり、重点調査項目の皮膚障害、電解質異常、infusion reaction、ILD、心毒性の発現率は図1の通りであった。
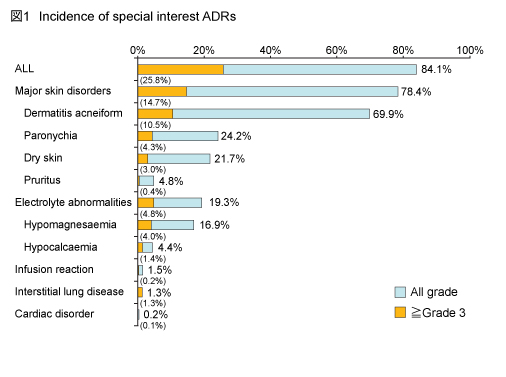
なお、各副作用の詳細は以下の通りである。
| ・ | 皮膚障害 全gradeの発現率は78.4% (2,419 / 3,085例) であり、皮膚障害による治療中止は7.0% (168 / 2,419例) であった。 |
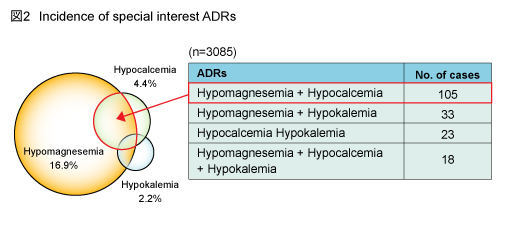
| ・ | 電解質異常 全gradeの発現率は19.3%であり、血清マグネシウムが低値の症例では血清カルシウムも低値である傾向がみられた (図2)。また、電解質異常が認められた症例で致死的な症例は認められなかった。なお、QTc延長が認められた症例は3例であり、3例ともに電解質異常が併存していた。 |
| ・ | Infusion reaction Grade 3以上の発現率は0.2% (6 / 3,085例) であったが、grade 4および死亡に至った症例は認められなかった。なお、前治療でCetuximabを投与された917例中70例がCetuximab投与中にinfusion reactionを発症し、そのうち20例が重篤な症例であり、非重篤症例は2例報告された。なお、Cetuximab投与時にinfusion reactionを発現しなかった847例中9例では、Panitumumab 投与によりinfusion reactionを発現した。 |
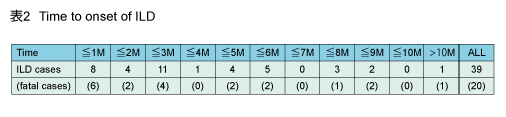
| ・ | ILD ILDは1.3% (39*/ 3,085例) にみられ、0.6% (20*/ 3,085例) が死亡に至った。この数値はCetuximabの日本の製造販売後調査の発現率と大きな差はなかった3)。また、発現の時期に一定の傾向は認められなかった (表2)。 *ILD分科会の評価に基づく |
臨床効果
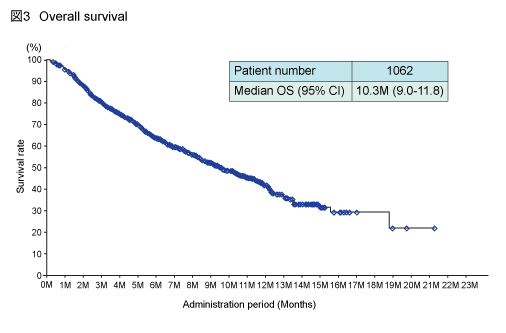
3rd-line治療以降にPanitumumabを単独投与した場合のOS (overall survival) 中央値は10.3ヵ月 (95% CI: 9.0-11.8) であった (図3)。
3rd-line治療以降にPanitumumabを単独投与した場合のOS (overall survival) 中央値は10.3ヵ月 (95% CI: 9.0-11.8) であった (図3)。
日本において、Panitumumabは治癒切除不能進行・再発大腸癌患者に対して推奨される症例に適正に使用されていた。また、製造販売後調査におけるPanitumumabの安全性、有効性は、既報の臨床試験と同様であり、新たな安全性における懸念は認められなかった。治癒切除不能進行・再発大腸癌患者に対するPanitumumabのリスクとベネフィットのバランスは良好であった。
Reference
1) Wainberg ZA, Hecht JR.: Expert Rev Anticancer Ther. 7(7): 967-973, 2007 [PubMed]
2) Martinelli E, et al.: Clin Exp Immunol. 158(1): 1-9, 2009 [PubMed]
3) Ishiguro M, et al.: Jpn J Clin Oncol. 42(4): 287-294, 2012 [PubMed]
1) Wainberg ZA, Hecht JR.: Expert Rev Anticancer Ther. 7(7): 967-973, 2007 [PubMed]
2) Martinelli E, et al.: Clin Exp Immunol. 158(1): 1-9, 2009 [PubMed]
3) Ishiguro M, et al.: Jpn J Clin Oncol. 42(4): 287-294, 2012 [PubMed]
関連リンク
・2011年 米国臨床腫瘍学会年次集会 abst #3510 「切除不能進行・再発大腸癌初回治療例に対するPanitumumab + FOLFOX4療法とFOLFOX4療法の無作為化比較第III相試験 (PRIME試験): 最終報告」
・2012年 消化器癌シンポジウム abst #387 「切除不能進行・再発大腸癌2nd-line治療例に対するPanitumumab + FOLFIRI療法とFOLFIRI療法の無作為化比較第III相試験 (20050181試験) :最終報告」
・ESMO 2012 abst #587P 「日本人治癒切除不能大腸癌患者におけるPanitumumabの製造販売後調査:中間報告(3,005例)」
・副作用対策講座「皮膚障害-1 分子標的薬の皮膚障害」
・2011年 米国臨床腫瘍学会年次集会 abst #3510 「切除不能進行・再発大腸癌初回治療例に対するPanitumumab + FOLFOX4療法とFOLFOX4療法の無作為化比較第III相試験 (PRIME試験): 最終報告」
・2012年 消化器癌シンポジウム abst #387 「切除不能進行・再発大腸癌2nd-line治療例に対するPanitumumab + FOLFIRI療法とFOLFIRI療法の無作為化比較第III相試験 (20050181試験) :最終報告」
・ESMO 2012 abst #587P 「日本人治癒切除不能大腸癌患者におけるPanitumumabの製造販売後調査:中間報告(3,005例)」
・副作用対策講座「皮膚障害-1 分子標的薬の皮膚障害」
