|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。
|

高リスク直腸癌に対する術前補助療法としてのCapecitabine + L-OHP (CAPOX) + 化学放射線療法 (CRT) へのCetuximab上乗せを検討した無作為化第II相試験 (EXPERT-C試験) におけるHER2解析
HER-2 in High Risk Rectal Cancer Patients Treated in EXPERT-C, A Randomized Phase II Trial of Neoadjuvant Capecitabine and Oxaliplatin (CAPOX) and Chemoradiotherapy (CRT) With or Without Cetuximab.
Francesco Sclafani, et al.

直腸癌においてHER2発現の頻度は低く、術前化学放射線療法におけるバイオマーカーとしての意義は不明であった

結果としては、HER2発現が検索された141例のうち陽性と判断されたのはわずか6例、4.3%と低率であった。したがって病理学的抗腫瘍効果 (CR、PR) においても生存 (PFS、OS) においても、HER2発現との相関を論じることは不可能であろう。切除可能な直腸癌に対する術前化学放射線療法は欧米の標準治療の一選択肢となっているが、切除可能な直腸癌全例に対して一様に術前化学放射線療法を行うことは再検討されている。現在、再発高リスク症例に対して分子標的薬併用レジメンの有用性を検討するEXPERT-C試験や、術前に十分量の化学療法 (mFOLFOX6) を施行して術後補助化学療法は行わないCONTRE試験など、対象症例や治療レジメンの検討がなされている。
本研究ではHER2のバイオマーカーとしての意義が検討されたが、発現頻度が低く有用性は明らかでなかった。しかし、術前化学放射線療法におけるバイオマーカー検索は、対象症例の絞り込みや至適レジメンの決定に寄与すると考えられ、今後も重要な課題である。当然、わが国において術前化学放射線療法を導入する際にも、バイオマーカーは有力な情報となり得る。
HER2は乳癌や胃癌の治療標的として確立されているが、直腸癌のHER2発現状況については相反するデータが報告されており2, 3)、直腸癌におけるHER2の役割は不明である。また、最近の前臨床試験の結果より、直腸癌の化学放射線療法 (CRT) およびCetuximabへの治療抵抗性の誘導においてHER2の役割が示されている4)。
EXPERT-C試験は、高リスク直腸癌に対する術前補助化学療法としてのCapecitabine + L-OHP (CAPOX) およびCRTへのCetuximabの上乗せ効果を検討するため、欧州で実施された大規模無作為化比較第II相試験である (図) 5)。今回、EXPERT-C試験の対象患者のHER2遺伝子変異と試験評価項目に及ぼす影響について検討した。
EXPERT-C試験は、高リスク直腸癌に対する術前補助化学療法としてのCapecitabine + L-OHP (CAPOX) およびCRTへのCetuximabの上乗せ効果を検討するため、欧州で実施された大規模無作為化比較第II相試験である (図) 5)。今回、EXPERT-C試験の対象患者のHER2遺伝子変異と試験評価項目に及ぼす影響について検討した。
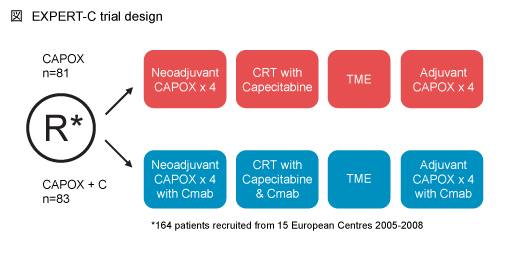
EXPERT-C試験では、組織学的に直腸癌と診断され、転移巣を有さず、MRIで切除可能な高リスク直腸癌と判定された患者を対象とした。HER2解析は中央検査室でレトロスペクティブに実施し、生検もしくは手術検体を用いて、免疫組織化学 (IHC) スコア3+ をHER2陽性、0/1+ をHER2陰性と判定し、IHC 2+ に関してはB-DISH (brightfield dual in situ hybridization) 法でHER2の増幅を検査し、B-DISH比≧2.0の場合にHER2陽性と判定した6)。なお、探索的解析として、IHC 0/1+ の検体のなかから20%を無作為に選択し、HER2増幅検査を実施した。
ここでは、EXPERT-C試験の主要評価項目であるCR、および副次評価項目である奏効率、PFS、OSに及ぼすHER2発現の影響について解析した。
ここでは、EXPERT-C試験の主要評価項目であるCR、および副次評価項目である奏効率、PFS、OSに及ぼすHER2発現の影響について解析した。
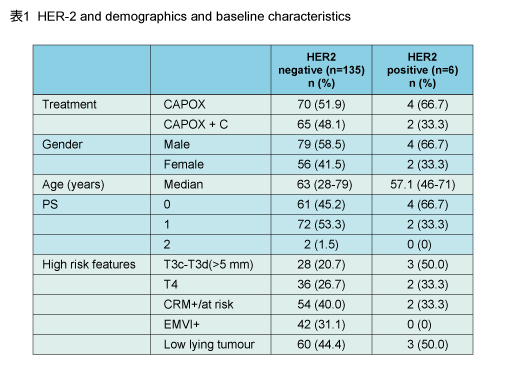
EXPERT-C試験には2005〜2008年の間に15施設から164例が登録され、HER2の評価が可能であったのは141例であった (生検104件、手術検体114件) 。HER2陽性率は生検2.9% (3/104件) 、手術検体2.6% (3/114件) であり、1つ以上の検体でHER2陽性の患者は6例 (4.3%) であった (表1) 。なお、生検および手術検体の両方の解析を行った77例のうち、ともにHER2陽性であった症例は認められず、ともにHER2陰性であったのは74例 (96%) だった。
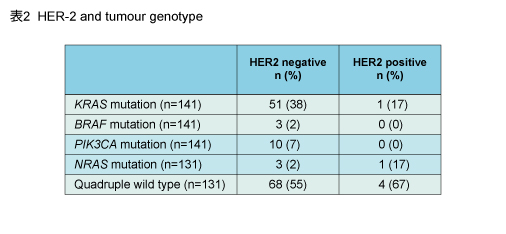
KRAS などの遺伝子解析については、KRAS 変異型がHER2陰性群135例中51例 (38%) 、HER2陽性群6 例中1例含まれており、KRAS 、BRAF 、PIK3CA 、NRAS すべて野生型の症例は、それぞれ68例 (55%) 、4例であった (表2) 。
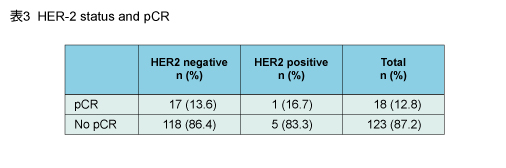
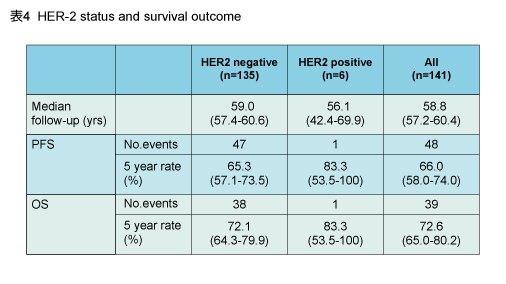
追跡期間中央値58.7ヵ月の時点において、病理学的CR (pCR) はHER2陰性、陽性との関連はみられなかった (表3) 。なお、HER2陽性群では、PFSおよびOSのイベント数は1件のみであった (表4) 。
EXPERT-C試験の対象患者におけるHER2の発現率は低く、HER2は高リスク直腸癌における有用な治療標的とはならなかった。今回の解析では、直腸癌に対するCetuximabベース治療の予後因子または効果予測因子としてのHER2の役割は確認されなかった。
Reference
1) Hwang JJ, et al.: 2001 Annual Meeting of the American Society of Clinical Oncology®: abst #565 [学会レポート]
2) Marx AH, et al.: Hum Pathol. 41(11): 1577-1585, 2010 [PubMed]
3) Conradi LC, et al.: 2012年 消化器癌シンポジウム: abst #493
4) Yonesaka K, et al.: Sci Transl Med. 3(99): 99ra86, 2011 [PubMed]
5) Dewdney A, et al.: J Clin Oncol. 30(14): 1620-1627, 2012 [PubMed]
6) Hofmann M, et al.: Histopathology. 52(7): 797-805, 2008 [PubMed]
1) Hwang JJ, et al.: 2001 Annual Meeting of the American Society of Clinical Oncology®: abst #565 [学会レポート]
2) Marx AH, et al.: Hum Pathol. 41(11): 1577-1585, 2010 [PubMed]
3) Conradi LC, et al.: 2012年 消化器癌シンポジウム: abst #493
4) Yonesaka K, et al.: Sci Transl Med. 3(99): 99ra86, 2011 [PubMed]
5) Dewdney A, et al.: J Clin Oncol. 30(14): 1620-1627, 2012 [PubMed]
6) Hofmann M, et al.: Histopathology. 52(7): 797-805, 2008 [PubMed]
