|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。
|

KRAS 変異型切除不能進行・再発大腸癌に対する2nd-lineにおけるMEK阻害薬Selumetinib + CPT-11併用療法:AGICC試験
Second-line Therapy of KRAS -mutated Metastatic Colorectal Cancer with the MEK Inhibitor, Selumetinib (AZD6244, ARRY-142886), in Combination with Irinotecan: An AGICC study
Howard S. Hochster, et al.

MEK阻害薬はKRAS 変異型に対する新たな治療選択となるか?

本会では同じくKRAS 遺伝子変異を有する大腸癌の2nd-lineを対象としてCPT-11との併用における用量設定の第II相試験結果が報告された。本試験は早期中止となっており、その中止理由に関しては言及されていない。筆者らは奏効率10%、PFS中央値105日の結果をもって有効性を期待する内容で結論づけていたが、昨年報告されたBevacizumab Beyond Progression (BBP) の有効性を検証するML18147試験2)では、サブセット解析においてKRAS 変異型におけるBBPのPFSが5.5ヵ月と報告されており、有害事象などを加味しても、残念ながら今回の結果がそれを凌駕するものとは考えにくい。
さらに、Selumetinibは2010年 米国臨床腫瘍学会年次集会において、単一の経路阻害ではクロストークによってシグナル伝達が維持されるという仮説に基づき、AKT阻害薬であるMK-2206との併用でMAPK経路とPI3K経路の二重阻害を検証した試験が報告されている3)。しかし有害事象が強く、両剤とも単剤投与時の推奨用量を投与することができず、わずかな有効性が示されたのみである。
大腸癌領域では他にもMEK阻害薬の開発が進行しているようであるが、BBPやRegorafenibのKRAS 変異型に対するサブ解析結果が報告された現状においては、これらを凌駕するような有効性が求められ、その結果を期待したい。
SelumetinibはMEKを阻害する低分子化合物であり、前臨床試験ではKRAS やBRAF 変異を有する患者に対し抗腫瘍活性を発揮する可能性が示されている。また、無作為化第II相試験において、Selumetinibは大腸癌でCapecitabineと同等のPFSが示されているほか、KRAS 変異型の非小細胞肺癌ではDocetaxel併用でPFSを有意に延長したことが報告されている1)。
現在、進行大腸癌の1st-lineにおける標準治療はL-OHPおよびフッ化ピリミジン製剤とBevacizumabとの併用であり、CPT-11は2nd-lineとして一貫してPFSで2.5ヵ月、奏効率で4%を示している4, 5)。また、抗EGFR抗体薬はKRAS 変異型の症例に対してbenefitがないことが知られているが、MEK阻害薬であるSelumetinibはKRAS またはBRAF 変異型の患者に対して効果がみられる可能性がある。
そこで、KRAS 変異型大腸癌に対する2nd-lineにおけるCPT-11 + Selumetinibの用量設定/第II相試験 (AGICC試験) が実施された。
現在、進行大腸癌の1st-lineにおける標準治療はL-OHPおよびフッ化ピリミジン製剤とBevacizumabとの併用であり、CPT-11は2nd-lineとして一貫してPFSで2.5ヵ月、奏効率で4%を示している4, 5)。また、抗EGFR抗体薬はKRAS 変異型の症例に対してbenefitがないことが知られているが、MEK阻害薬であるSelumetinibはKRAS またはBRAF 変異型の患者に対して効果がみられる可能性がある。
そこで、KRAS 変異型大腸癌に対する2nd-lineにおけるCPT-11 + Selumetinibの用量設定/第II相試験 (AGICC試験) が実施された。
対象は、L-OHP + Bevacizumabベースのレジメンによる1st-line治療後にPDまたは毒性により治療中止になった、またはFOLFOXによる術後補助化学療法を開始後12ヵ月以内に再発したstage IVの大腸癌患者で、18歳以上、ECOG PS 0-1、KRAS またはBRAF 遺伝子の変異陽性の患者とした。
用量設定試験の投与スケジュールは、CPT-11 (180mg/m2, day 1, 2週毎) を固定し、Selumetinibは75mg/day (レベル-1) 、50mg/day/bid (レベル1) 、75mg/day/bid (レベル2) と増量し、day 1-28まで経口投与することとした(表1)。
用量設定試験の投与スケジュールは、CPT-11 (180mg/m2, day 1, 2週毎) を固定し、Selumetinibは75mg/day (レベル-1) 、50mg/day/bid (レベル1) 、75mg/day/bid (レベル2) と増量し、day 1-28まで経口投与することとした(表1)。
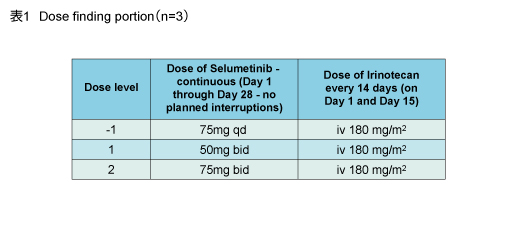
また、第II相試験では、CPT-11 (180mg/m2, day 1, 2週毎) + Selumetinib (用量設定試験で決定した用量を4週毎) 投与することとした。
主要評価項目は奏効率であり、これまでの報告より4%を比較値とした。また、副次評価項目は毒性およびPFSであった。
主要評価項目は奏効率であり、これまでの報告より4%を比較値とした。また、副次評価項目は毒性およびPFSであった。
用量設定試験ではレベル1 (3例) 、レベル2 (3例) とも用量制限毒性 (DLT) は発現せず、第II相試験におけるSelumetinibの推奨用量は75mg/day/bidに決定された。
第II相試験には32例が登録され、31例が実際に治療を受けたが、試験はプロトコール不適合により早期中止となった。
治療を受けた31例の患者背景は、年齢中央値56歳、男性18例 (58%) 、白人24例 (77%) 、ECOG PS 0が11例、PS 1が20例であり、9例に放射線療法歴があり、全例に化学療法歴があった。
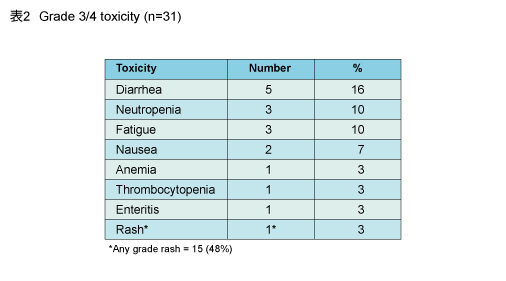
Grade 3/4の有害事象は、下痢16%、好中球数減少10%、疲労10%であり、全gradeの皮膚障害は48%に認められた (表2) 。なお、減量せずにCPT-11の投与を完遂したのは66%、Selumetinibは42%であった。
第II相試験には32例が登録され、31例が実際に治療を受けたが、試験はプロトコール不適合により早期中止となった。
治療を受けた31例の患者背景は、年齢中央値56歳、男性18例 (58%) 、白人24例 (77%) 、ECOG PS 0が11例、PS 1が20例であり、9例に放射線療法歴があり、全例に化学療法歴があった。
Grade 3/4の有害事象は、下痢16%、好中球数減少10%、疲労10%であり、全gradeの皮膚障害は48%に認められた (表2) 。なお、減量せずにCPT-11の投与を完遂したのは66%、Selumetinibは42%であった。
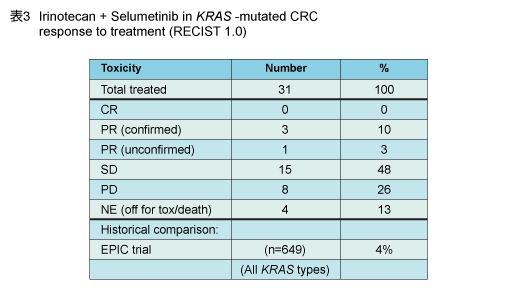
確証されたPRは3例で得られ、奏効率は10%であった (表3) 。これはEPIC試験におけるCPT-11単独の4%よりも優れた成績であった4)。
TTP (time to progression) 中央値は120日で、治療期間6ヵ月超の症例が7例、1年以上の症例は3例認められた。
また、PFS中央値は105日であり、8ヵ月超のPFSを達成した症例が20%認められた。
また、PFS中央値は105日であり、8ヵ月超のPFSを達成した症例が20%認められた。
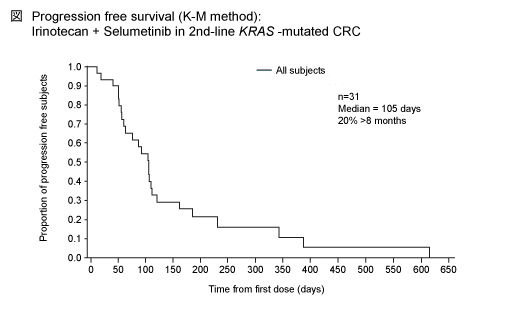
CPT-11 (180mg/m2, day 1, 2週毎) + Selumetinib (75mg/day/bid) 療法は良好な忍容性を示した。また、奏効率は10%、PFS中央値は105日であり、historical comparisonとしたEPIC試験のCPT-11単独群 (奏効率4%、PFS中央値2.5ヵ月) よりも良好であった。
これらの知見はMEK阻害薬がKRAS 変異型進行大腸癌の治療戦略として有効であるという仮説を支持するもので、さらなる検討が望まれる。
これらの知見はMEK阻害薬がKRAS 変異型進行大腸癌の治療戦略として有効であるという仮説を支持するもので、さらなる検討が望まれる。
