CRYSTALおよびOPUS試験の最新報告
2008年 米国臨床腫瘍学会年次集会(Van Cutsem E, et al.: abst #LBA2)にて発表されたCRYSTAL試験のサブ解析により、腫瘍のKRAS 変異が転移再発大腸癌に対するcetuximabの効果不良因子であることが示され、大腸癌化学療法はpersonalized therapyの時代を迎えた。その後、抗EGFR抗体薬併用化学療法が施行された転移再発大腸癌におけるKRAS statusの解析結果が相次いで報告され、KRAS 変異型では、抗EGFR抗体薬の治療効果が得られないことは明らかになった。
KRAS に続き、抗EGFR抗体薬の効果予測因子として有力視されてきたのが、KRAS の下流に位置するセリン・スレオニンキナーゼのBRAF である。Di Nicolantonioらの報告では、既治療例における腫瘍のBRAF 変異が効果予測因子になり得ることが示唆されている1)。
今回、転移再発大腸癌における1st-line治療としてのcetuximab併用療法を比較・検討したCRYSTALおよびOPUS試験において、KRAS /BRAF 測定検体数を増やし、追跡期間を延長した最新の解析結果が報告された。本レポートでは、#281:CRYSTAL試験の最新結果、ならびに#406:CRYSTAL/OPUS試験のメタ解析の2演題を紹介する。
|
||||||
CRYSTAL試験の最新結果
Cetuximab plus FOLFIRI in the treatment of metastatic colorectal cancer (mCRC): The influence of KRAS and BRAF biomarkers on outcome: Updated data from the CRYSTAL trial.
Eric Van Cutsem, et al.
CRYSTAL試験は、オープンラベル無作為化他施設共同第III相試験である(2007年 米国臨床腫瘍学会年次集会: abst #4000)。 |
Intention to treat解析の対象は1,198例である。KRAS /BRAF 測定は、KRAS では1,063例(89%)、BRAF では1,000例(83%)と症例数を増やし再解析された[前回KRAS 540例(45%)、BRAF 529例(44%)]2)。 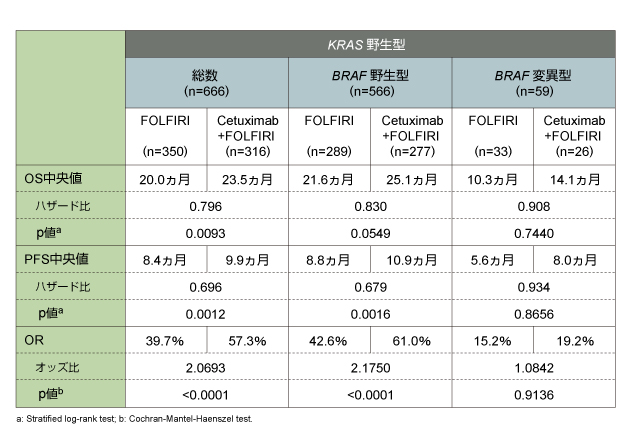
|
1st-line治療におけるcetuximab+FOLFIRI療法は、KRAS 野生型大腸癌患者のOSを有意に改善し、また腫瘍のKRAS 変異の有無はcetuximabの効果予測因子であることが実証された。 |
KRAS およびBRAF 遺伝子変異によるCRYSTAL試験とOPUS試験のメタ解析
Cetuximab with chemotherapy (CT) as first-line treatment for metastatic colorectal cancer (mCRC): A meta-analysis of the CRYSTAL and OPUS studies according to KRAS and BRAF mutation status.
Claus-Henning Köhne, et al.
CRYSTAL試験およびOPUS試験のKRAS 評価症例を対象に、1st-line治療としてのFOLFOX/FOLFIRI療法とcetuximab併用療法の治療成績を比較・検討した。評価項目はPFSおよびORとした。
CRYSTAL : 1,063/1,198例 (89%)
OPUS : 315/337例 (93%)
CRYSTAL : 1,000/1,198例 (83%) OPUS : 309/337例 (92%) |
両試験のプール解析によるKRAS 野生型の治療成績(全体およびBRAF status別)を下表に示した。OS、PFS、ORのいずれも、FOLFOX/FOLFIRI療法に比べ、cetuximab併用化学療法のほうが優れていた。 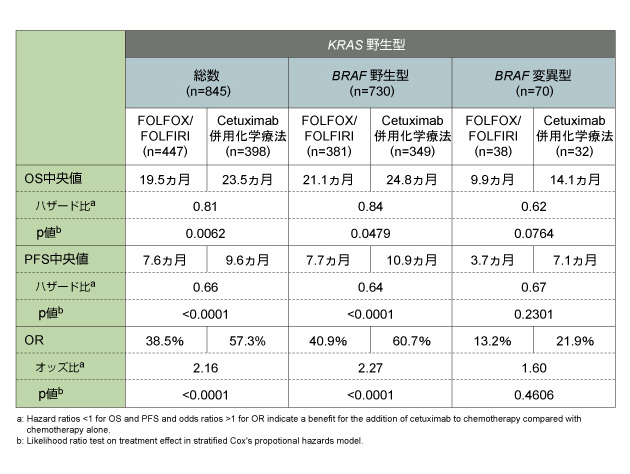
|
今回のプール解析によって、KRAS 野生型における1st-line治療としてのcetuximab併用化学療法は、OSを有意に延長することが確認された。さらに、CRYSTALおよびOPUS試験の解析において既に示されていたPFS、ORの改善効果をより確固たるものにした。 |
Reference |
【関連情報】
「転移性結腸・直腸癌に対するpanitumumabまたはcetuximabの奏効には野生型BRAF が必要である」
Di Nicolantonio F, et al., J Clin Oncol. 2008; 26(35): 5705-5712
2008年 米国臨床腫瘍学会年次集会 速報演題レポート #LBA2
「転移を有する大腸癌患者に対する一次治療におけるFOLFIRI単独またはcetuximab併用療法の治療効果と
K-RASの関連: CRYSTAL試験の結果のレトロスペクティブな解析」


