The European Cancer Congress 2013 - ESMO


�@�����ԁAEGFR�ɑ��郂�m�N���[�i���R�̖�ł���Panitumumab��Cetuximab�͒��ڔ�r���s��ꂸ�ɂ������A�{��ɂăt�b���s���~�W���n����/CPT-11/L-OHP�̓��^��������KRAS exon 2�쐶�^�̏Ǘ��ΏۂƂ���head-to-head�̑�III�������ł���ASPECCT�����̌��ʂ�����APanitumumab��Cetuximab�ɑ����������ꂽ�B
�@�{�M�ɂ����Ă͌��݁AKRAS exon 2�쐶�^��3rd-line��ΏۂƂ���CPT-11 + Panitumumab��CPT-11 + Cetuximab���r���閳�����II������ (WJOG6510G) ���s���Ă��邪�A�܂����ʂ����Ɏ����Ă��Ȃ��B
�@����A���ꂽ�̂͂��ꂼ��Cetuximab��Panitumumab��2�̌��������� (HGCSG0901�AHGCSG1002) �̃f�[�^�x�[�X��p������͂ŁA�t�b���s���~�W���n����/CPT-11/L-OHP�ɕs���AKRAS exon 2�쐶�^�A�P�ܓ��^�Ȃǂ̏����ꂵ���Ǘ� (Cetuximab 31��APanitumumab 51��) ��ΏۂƂ��ėL��������ш��S�����r�����������̂ł���B
�@�����̌����������͓��ɍׂ��ȓK�i���݂��Ă��炸�AASPECCT���������S�g��ԕs�ǂ̏ǗႪ�����������A2�܂̊Ԃɍ��ق�F�߂��A�قړ��l�̗L��������ш��S���������ꂽ�B2�̎����͇@�����������A�A�o�^�������قȂ�A�B�Ǘᐔ�����Ȃ��A�Ȃǂ�limitation�����݂��A�f��I�Ȃ��Ƃ����_�Â��邱�Ƃ��ł��Ȃ����A�{�M�ɂ����钼�ڔ�r���������݂��Ȃ�����ł́A�\���Q�Ƃɒl����ł������B
�@�REGFR�R�̖�ł���Cetuximab��Panitumumab��KRAS �쐶�^�̐؏��s�\�i�s�E�Ĕ��咰���ɑ��ėL��������ш��S�����F�߂��Ă���A�T���x�[�W���C���ɂ�����P�ܗÖ@�����ꂼ��L�����������Ă��邪�A���ڔ�r���������͍���̃A�u�X�g���N�g��o���_�ŕ���Ă��Ȃ��B
�@����AHGCSG (Hokkaido Gastrointestinal Cancer Study Group) �ɂ�����Cetuximab��Panitumumab��2�̌����������̃f�[�^��p���āA�L��������ш��S���ɂ��Ĕ�r��͂����B
�@�؏��s�\�i�s�E�Ĕ��咰����ΏۂƂ������L��2�����̂����AKRAS �쐶�^�ɑ���T���x�[�W���C���Ƃ���Cetuximab�܂���Panitumumab���P�ܓ��^���ꂽ�ǗႪ��͑ΏۂƂȂ����B
| �E | HGCSG0901�����F2008�N9���`2010�N7����27�{�݂œo�^����ACetuximab���܂ގ��Â��{�s���ꂽ269�� |
| �E | HGCSG 1002�����F2010�N6���`2011�N10����21�{�݂œo�^����APanitumumab���܂ގ��Â��{�s���ꂽ200�� |
�@�L�����̕]���͑t���� (RECIST v1.0��p�����]��)�APFS�ɂ��čs�����B
�@���Ҕw�i�A�L�Q���ہA�t�����ɂ��ẮAFisher�̐��m�m�������p���č��v�I�ɕ]�������B11�̍��ڂ�log-rank����ɂ��P�ϗʉ�͂��s���Ap<0.15�ł��������ڂƃ��W�����ɂ��āA�ϐ������@�ɂ��Cox���n�U�[�h���f����p�������ϗʉ�͂��s�����B
�@��͑ΏۂƂȂ���Cetuximab�Q31��APanitumumab�Q51��̊��Ҕw�i�ɂ����āA�N��A���ʁA���������ʁA�؏��ABevacizumab�̑O���Âɍ��͂Ȃ��������AECOG PS 0 (p=0.006)�A�̓]�� (p=0.003) ��Panitumumab�Q�ő����F�߂�ꂽ�B
�@�L�Q���ۂ�Cetuximab�Q��Panitumumab�Q�ő傫�ȍ��͔F�߂��Ȃ����� (�\1)�B
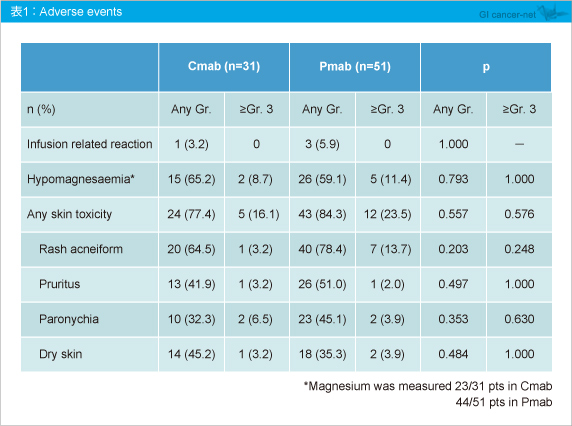
�@�܂��A�t������Cetuximab�Q19.4%�APanitumumab�Q13.7%�ƍ��݂͂��Ȃ����� (p=0.543) (�\2)�B
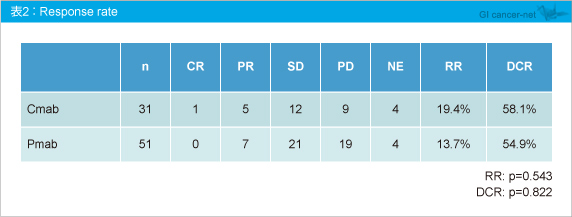
�@PFS�����l��Cetuximab�Q3.8�����APanitumumab�Q3.1�����ł���A���Q�ɍ���F�߂Ȃ����� (HR=0.960, 95% CI: 0.823-1.118, p=0.595) (�})�B�܂��AOS�����l�����ꂼ��8.4�����A8.1�����ł���A���Q�ɍ���F�߂Ȃ����� (HR=0.920, 95% CI: 0.780-1.084, p=0.318)�B
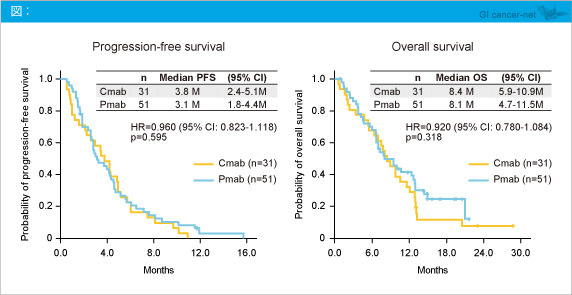
�@�P�ϗʉ�͂̌��ʁAPFS�ł̓��W�����A���ʁAECOG PS�A�����d��̗L���A�]�ڑ���̐����AOS�ł̓��W�����AECOG PS�A�؏��A�̓]�ڂ̗L���A�]�ڑ���̐��ɂ��đ��ϗʉ�͂��s��ꂽ�B���̌��ʁAPFS�ł�ECOG PS 0-1/2-3 (p=0.001)�AOS�ł�ECOG PS 0-1/2-3 (p<0.001)�A�]�ڑ���̐�1-2/3-4 (p=0.002) �ɂ����ėL�Ӎ����F�߂�ꂽ�B
�@����̌�������͂ł́A�؏��s�\�i�s�E�Ĕ��咰���ɑ���T���x�[�W���C���̒P�ܗÖ@�ɂ�����Cetuximab��Panitumumab�Ƃ̊ԂɗL�����ɍ��݂͂��Ȃ������B


