背景と目的
20050181試験ではKRAS 遺伝子変異を有さない切除不能進行・再発大腸癌2nd-line治療例に対するFOLFIRI療法へのPanitumumabのPFS (progression-free survival) における上乗せ効果が証明された。今回、事前に計画されていた最終登録症例から30ヵ月後のPFS、OS (overall survival) の解析結果が報告された。
対象と方法
20050181試験1)に登録された症例について、以下の解析を実施した。
主要評価項目:KRAS status別のPFS、OS
副次評価項目: ORR (objective response rate) 、patient reported outcome (PRO) 、安全性
結果
全登録患者1,186例 (Panitumumab + FOLFIRI群591例、FOLFIRI群595例) のうち、KRAS statusが確認できたのは1,083例 (KRAS 野生型55%、KRAS 変異型45%) であった。各々のKRAS statusにおける両治療群の患者背景に大きな隔たりはなかった。
KRAS 野生型における結果を下記に示す (括弧内はKRAS 変異型) 。- ・PFS: Panitumumab + FOLFIRI群 vs. FOLFIRI群
6.7ヵ月 vs. 4.9ヵ月, HR=0.82, p=0.02
(5.3ヵ月 vs. 5.4ヵ月, HR=0.94, p=0.56) - ・OS
14.5ヵ月 vs. 12.5ヵ月, HR=0.92, p=0.37
(11.8ヵ月 vs. 11.1ヵ月, HR=0.93, p=0.48) - ・ ORR
36.0% vs. 9.8%, OR=5.5, p<0.0001
(13.4% vs. 14.4%, OR=0.9, p=0.88) - ・
Grade 3-4の主な有害事象
皮膚関連毒性37% vs. 2%、下痢14% vs. 9%、口内炎8% vs. 3%、低カリウム血症7% vs. 1%、低マグネシウム血症3% vs. <1%
(皮膚関連毒性32% vs. 1%、下痢14% vs. 10%、口内炎10% vs. 4%、低カリウム血症4% vs. 1%、低マグネシウム血症 5% vs. 0%) - ・皮膚障害とPFS (図1)
Grade 0-1: Panitumumab + FOLFIRI群 4.0 ヵ月
Grade 2-4: Panitumumab + FOLFIRI群 7.4 ヵ月、FOLFIRI群 5.1ヵ月
HR=0.72, p=0.0006
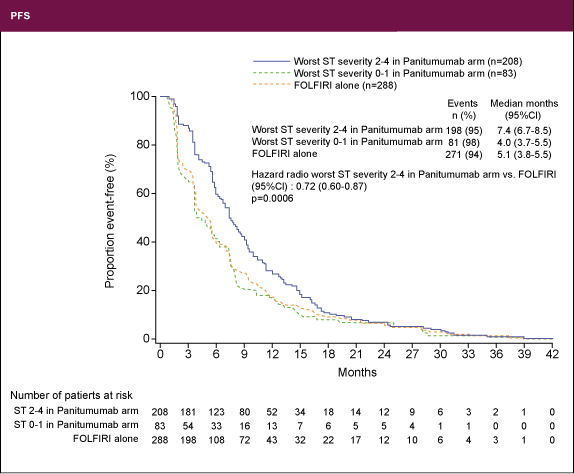 図1
図1- ・皮膚障害とOS (図2)
Grade 0-1: Panitumumab + FOLFIRI群 8.4ヵ月
Grade 2-4: Panitumumab + FOLFIRI群 16.6ヵ月、FOLFIRI群 12.7ヵ月
HR=0.80, p=0. 025
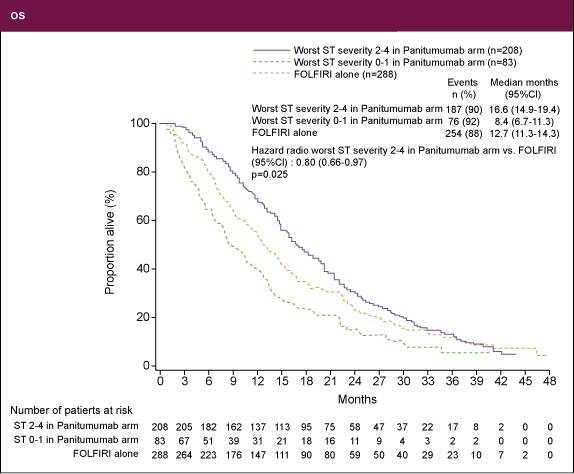 図2
図2結論
今回の最終解析においても既報と同様、KRAS 野生型切除不能進行・再発大腸癌2nd-line治療例に対するFOLFIRI + Panitumumab併用療法は、FOLFIRI療法と比較して有意にPFS、ORRが良好で、OSも良好な傾向であった。KRAS 変異型症例に対してPanitumumabを併用することで予後が悪化することはなかった。FOLFIRI療法群の1/3の症例が後治療に抗EGFR療法が行われており、予後に影響した可能性が考えられる。有害事象は既報と同様であった。KRAS 野生型症例では皮膚毒性grade 2-4を認めた症例ではPFS、OSが良好であった。
コメント
本試験は、20050181試験の最終登録から30ヵ月後に実施されることが最初から予定されており、updateデータを解析するものであった。切除不能進行・再発大腸癌の2nd-lineにおいて、FOLFIRIはPanitumumabを併用した方が単独療法より有意にPFS、ORRが良好で、OSも良い傾向にあり、KRAS 野生型は変異型よりも良好な結果であった。さらにKRAS 変異型への投与についても、副作用などで生存期間が短縮するなど、患者さんの不利益になることはみられなかった。この試験終了後30ヵ月という観察期間の成績により、新規抗EGFR抗体薬として登場したPanitumumabが、このlineで安全かつ有効に使用が可能であることが示されたと考える。
一方で、本試験とは直接関係ないが、2012年の米国臨床腫瘍学会年次集会において、TML試験 (ML18147) の研究報告が成された。これはいわゆるBBP試験であるが、2nd-lineでBevacizumabを併用するとPFSは5.7ヵ月 (vs. 4.1ヵ月)、HR=0.68、p<0.0001と、本試験のPanitumumab併用のデータと匹敵する。さらにBBPではOSも良いデータが報告されている2) 。ただし、実際のところは別試験であり単純な比較はできないため、KRAS 遺伝子解析やその他の状況を判断して、適切な薬剤を使用することになるものと思われる。
(レポート:山﨑 健太郎 監修・コメント:小松 嘉人)

