ESMO 2014 Congress
大腸癌
Abstract #LBA10
CALGB/SWOG 80405試験:治療戦略の一環として手術を受けた患者の解析
CALGB/SWOG 80405: Patients Undergoing Surgery as Part of Treatment Strategy
Alan Venook, et al.

Expert's view

岩本 慈能 先生
関西医科大学附属枚方病院
消化管外科
切除施行例の約60%は、登録時の治療目的がpalliativeとされた症例であった。つまり、化学療法により切除不能が切除可能となる、いわゆるconversion therapyが明らかに存在し、OSの延長が得られたことになる。切除が施行された180例の内訳はCetuximab群が105例、Bevacizumab群が75例となっており (NED症例の内訳はBevacizumab群50例、Cetuximab群82例)、統計学的に検証されていないものの切除に対しCetuximabが有利な印象である。また、NED症例における奏効率はBevacizumab群82%、Cetuximab群68%であったが、切除可能となる理由は単に奏効率だけではなく、奏効の深さなども関連する可能性があると考えられる。しかし、DFSもOSも両群間に有意差は認めていない。切除症例における肝限局転移症例が50%程度であり、原発巣残存症例が30%程度あることから、高度リンパ節転移や局所進行癌も含まれている可能性が高い。そのため、CELIM試験やnew EPOC試験と比較することはできず、切除可能・不可能を1st-lineにおけるCetuximab、Bevacizumabの選択基準にすることはできないと思われた。
CALGB80405試験はKRAS 野生型の切除不能進行・再発大腸癌に対するFOLFIRI/mFOLFOX6 + Bevacizumab (Bev群) とFOLFIRI/mFOLFOX6 + Cetuximab (Cmab群) を比較した無作為化第III相試験であり、2014年米国臨床腫瘍学会年次集会で結果が報告された。
一方、切除不能進行・再発大腸癌は集学的治療によって治癒する可能性があることから、CALGB80405試験に参加し、化学療法後に手術を受けた患者の特徴と長期予後を調査するため、本サブセット解析が行われた。
一方、切除不能進行・再発大腸癌は集学的治療によって治癒する可能性があることから、CALGB80405試験に参加し、化学療法後に手術を受けた患者の特徴と長期予後を調査するため、本サブセット解析が行われた。
CALGB80405試験は2005年11月〜2012年3月の間に3,058例が登録されたが、KRAS 野生型の2,334例が無作為化され、プロトコール変更などにより最終的に1,137例が適格となった。なお、追跡期間中央値は32ヵ月で、年齢中央値は59歳、男性が61%を占めた。
CALGB80405試験において、化学療法後に手術を受けた症例は1,137例中180例 (15.8%) であり、Bev群75例に対しCmab群105例とCmab群で多かった (表)。
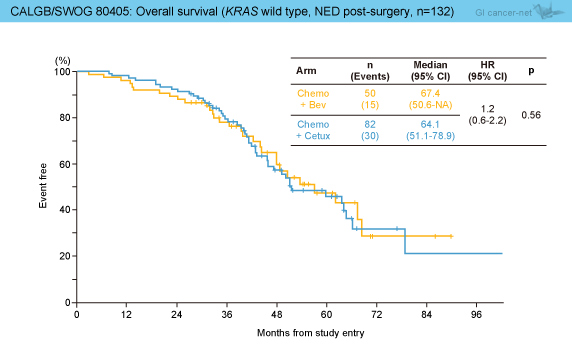
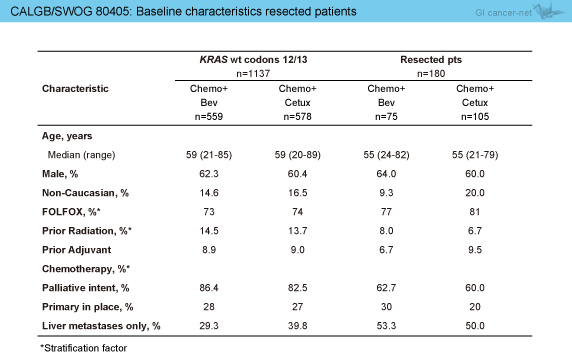 手術を受けた180例中132例は術直後に無病生存状態 (no evidence of disease: NED) であり、OS中央値は64.7ヵ月 (95% CI: 59.8-78.9) であった。なお、NED例はBev群50例、Cmab群82例であり、OS中央値はBev群が67.4ヵ月、Cmab群64.1ヵ月と、有意差は認めなかった (HR=1.2, 95% CI: 0.6-2.2, p=0.56) (図1)。
手術を受けた180例中132例は術直後に無病生存状態 (no evidence of disease: NED) であり、OS中央値は64.7ヵ月 (95% CI: 59.8-78.9) であった。なお、NED例はBev群50例、Cmab群82例であり、OS中央値はBev群が67.4ヵ月、Cmab群64.1ヵ月と、有意差は認めなかった (HR=1.2, 95% CI: 0.6-2.2, p=0.56) (図1)。
 奏効率は、全体ではBev群57%、Cmab群66%であり、化学療法別の解析では、mFOLFOX6ではBev群56%、Cmab群67%、FOLFIRIではBev群61%、Cmab群62%であった。NED例のうち奏効状態が評価できたのは111例で、Bev群82% (37/45例)、Cmab群68% (50/66例) であった。
奏効率は、全体ではBev群57%、Cmab群66%であり、化学療法別の解析では、mFOLFOX6ではBev群56%、Cmab群67%、FOLFIRIではBev群61%、Cmab群62%であった。NED例のうち奏効状態が評価できたのは111例で、Bev群82% (37/45例)、Cmab群68% (50/66例) であった。
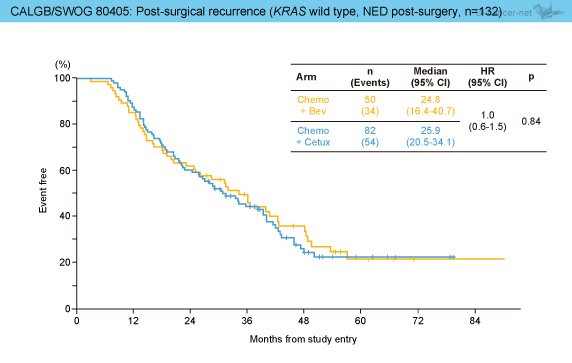
NED例における術後のDFS (disease free survival) 中央値は15.9ヵ月 (95% CI: 10.4-21.2) で、Bev群16.9ヵ月、Cmab群15.3ヵ月と両群に差はみられなかった (HR=1.0, 95% CI: 0.6-1.5, p=0.94) (図2)。また、NED例における無作為化から術後再発までの期間中央値は25.7ヵ月 (95% CI: 20.5-33.5) であり、Bev群24.8ヵ月、Cmab群25.9ヵ月であった (HR=1.0, 95% CI: 0.6-1.5, p=0.84) (図3)。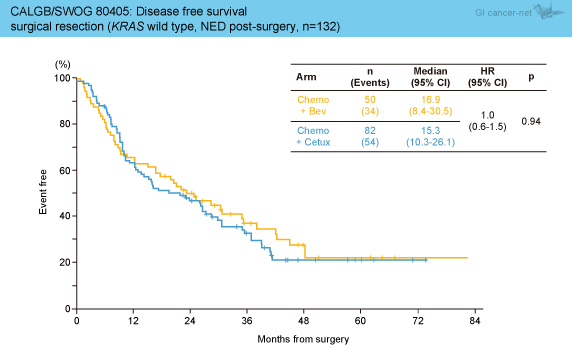
 NED例に対してRAS 解析を行った結果、132例中76例でRAS 評価され、OS中央値はRAS 野生型 (65例) 78.8ヵ月、何らかの変異を有するRAS 変異型 (11例) 47.9ヵ月であったが、症例数が少なく有意差は認めなかった (HR=0.52, 95% CI: 0.2-1.4, p=0.2)。同様に、手術後のDFS中央値はそれぞれ16.1ヵ月、9.5ヵ月で、両群に有意差は認めなかった (HR=0.84, 95% CI: 0.3-1.8, p=0.6)。
NED例に対してRAS 解析を行った結果、132例中76例でRAS 評価され、OS中央値はRAS 野生型 (65例) 78.8ヵ月、何らかの変異を有するRAS 変異型 (11例) 47.9ヵ月であったが、症例数が少なく有意差は認めなかった (HR=0.52, 95% CI: 0.2-1.4, p=0.2)。同様に、手術後のDFS中央値はそれぞれ16.1ヵ月、9.5ヵ月で、両群に有意差は認めなかった (HR=0.84, 95% CI: 0.3-1.8, p=0.6)。
表

図1

NED例における術後のDFS (disease free survival) 中央値は15.9ヵ月 (95% CI: 10.4-21.2) で、Bev群16.9ヵ月、Cmab群15.3ヵ月と両群に差はみられなかった (HR=1.0, 95% CI: 0.6-1.5, p=0.94) (図2)。また、NED例における無作為化から術後再発までの期間中央値は25.7ヵ月 (95% CI: 20.5-33.5) であり、Bev群24.8ヵ月、Cmab群25.9ヵ月であった (HR=1.0, 95% CI: 0.6-1.5, p=0.84) (図3)。
図2

図3

CALGB80405試験のサブセット解析では、化学療法後に手術を受け、NEDに達した症例のOS中央値は5年を超えた。Bevacizumab併用療法に比べ、Cetuximab併用療法を行った患者のほうがNEDに達しやすかったが、予後に差はなかった。RAS 解析の範囲を広げることで、予後の差を識別できる可能性がある。
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。

