


従来、抗EGFR抗体薬療法においてはCetuximab、Panitumumabの2剤の使用が可能であったが、その使い分けに関しては決まった方法はなく、NCCNガイドラインでもどちらかを使うことが推奨されていた。
近年KRAS codon 13D変異に対しCetuximabの有用性の報告とPanitumumabでの否定的な報告や、CetuximabはEGFR遺伝子変異がある症例において効果が乏しく、Panitumumabで有用性がありそうだとの報告1) などが相次いでいる。さらには抗EGFR抗体薬が有効であった症例に対し、無効になった後でも6ヵ月以上などの一定期間経過後に再度抗EGFR抗体薬が有効であるなどの報告2) がされるようになってきている。
本演題はCetuximabベース治療後に、Panitumumab療法を行った良好な成績についての報告である。ただ、様々なラインでの治療が混在し、増悪、毒性中止の理由の内訳などの詳細も不明であり、さらには多くのバイアスの存在が考えられる。今後よいデザインの臨床試験での検証が望まれる。
切除不能進行・再発大腸癌のマネジメントは、抗EGFR抗体薬 (Panitumumab、Cetuximab) をはじめとした分子標的薬により著しく改善されてきた。そして、KRAS 野生型でCetuximabベースのレジメン (CBR) による治療後に増悪した症例に対するPanitumumab単独療法 (PM) の有用性に関心が集まっている。
欧州医薬品庁 (EMA) の承認に従い、KRAS 野生型の切除不能進行・再発大腸癌に対してCBR療法を行った後に増悪し、PM療法を施行した症例について、その効果を評価した。評価項目は、奏効率、病勢コントロール率 (奏効+SD) 、PFS (progression-free survival) 、OS (overall survival) 、毒性とした。
CBR療法後に増悪し、PM療法を施行した106例が対象となった。原発巣の部位は結腸が62%、直腸が35%、両部位が3%であり、切除不能進行・再発大腸癌に対する治療を1〜9サイクル連続して施行した。
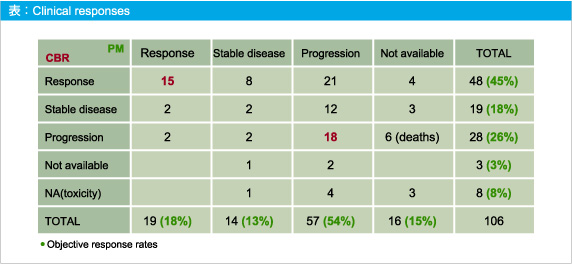
CBR療法による奏効率は45%、SDは18%であった。CBR療法後のPM療法による奏効率は18%、SDは13%であった。CBR療法で奏効した48例のうち、増悪後のPM療法により31% (15例) が奏効し、16% (8例) はSDであり、病勢コントロール率は47%であった。なお、Cetuximab抵抗性を示した28例については、PM療法による病勢コントロール率は14% [奏効7% (2例)、SD7% (2例)] であった (表) 。
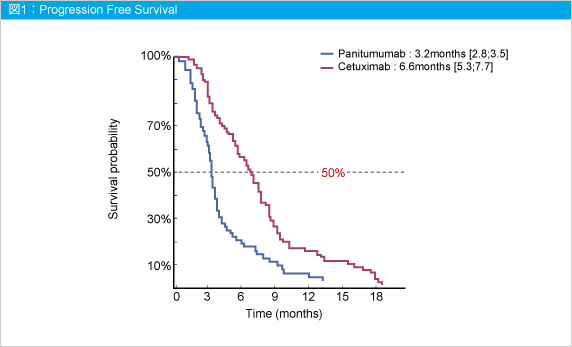
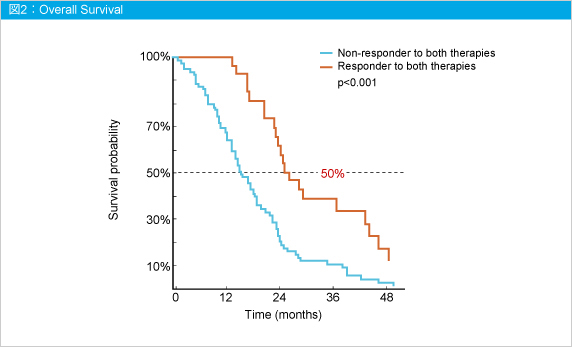
PFS中央値はCBR療法では6.6ヵ月、増悪後のPM療法では3.2ヵ月であった (図1) 。OS中央値は、CetuximabとPanitumumabともに奏効に至った症例では25.4ヵ月、ともに奏効に至らなかった症例では15.0ヵ月であり、有意差が認められた (p<0.001) (図2) 。
なお、grade 3/4の副作用はCBR療法で31%、増悪後のPM療法で14%にみられた。
今回の報告により、CBR療法で奏効後に増悪した症例に対してPM療法を用いることで、病勢コントロール率47%という優れたベネフィットを得られる可能性が示された。また、抗EGFR抗体薬のresponderに両分子標的薬を引き続き使用することにより、OSが延長する可能性がある。
