2011年9月23日〜27日にスウェーデン・ストックホルムにて開催されたThe European Multidisciplinary Cancer Congress 2011 - ESMOより、大腸癌や胃癌などの注目演題のレポートをお届けします。演題レポートの冒頭には、臨床研究の第一線で活躍する監修ドクターのコメントを掲載しています。

切除不能局所進行または転移を有する胃・胃食道接合部腺癌患者に対する1st-line治療としてのEpirubicin + Cisplatin + Capecitabine (ECX) + Rilotumumab併用療法の有効性および安全性の検討
Safety and Efficacy of Epirubicin, Cisplatin, and Capecitabine (ECX) Plus Rilotumumab (R) as First-line Treatment for Unresectable Locally Advanced (LA) or Metastatic (M) Gastric or Esophagogastric Junction (EGJ) Adenocarcinoma
Timothy Iveson, et al.

切除不能・再発胃癌に対するHGF/c-MET経路を標的とする治療戦略: 今後、c-MET陽性胃癌という分野が確立されるか?

c-MET受容体のリガンドであるHGFに対するRilotumumabに関しては、大腸癌のサルベージラインにおける比較第II相試験の結果が2011年の消化器癌シンポジウム1)、米国臨床腫瘍学会年次集会2)で報告されている。Panitumumab単独と比較してRilotumumabのresponse rate (RR) に対する有意な上乗せ効果が示されたが、c-MET発現は効果予測のバイオマーカーにはならないとの結果であった。
今回の胃癌1st-lineにおける検討では、主要解析の主要評価項目であるPFSでHR 0.64とpromisingな生存の上乗せ効果が示された。さらに、少数例の検討ではあるもののサブ解析においてPFSに加え、OS、RRでもc-METの高発現例においてより明らかに良好な成績が示されている。
今後の第III相試験においては、c-MET発現がRilotumumab投与における有効な症例を絞り込めるバイオマーカーになるかを十分に検証できる試験デザインで行われ、HER2陽性に続き、c-MET陽性胃癌という分野が確立されることが期待される。
Rilotumumab (AMG 102) はc-Met受容体のリガンドであるhepatocyte growth factor (HGF) に対する完全ヒト型モノクローナル抗体であり、c-Metの下流シグナルを抑制する。前臨床モデルでは腫瘍増殖をHGF/c-Met依存的に阻害し、早期臨床試験で忍容性が確認されている。
胃癌におけるc-Metの高発現は40-60%の患者に認められ、またc-Metは胃腺癌で活動性が高いことが報告されている。今回、プラセボを対照とした3群の多施設共同二重盲検無作為化比較第II相試験を実施した。
胃癌におけるc-Metの高発現は40-60%の患者に認められ、またc-Metは胃腺癌で活動性が高いことが報告されている。今回、プラセボを対照とした3群の多施設共同二重盲検無作為化比較第II相試験を実施した。
切除不能局所進行または転移を有する胃・胃食道接合部 (GEJ) および下部食道 (GEJから5cm以内) の腺癌で、当該疾患に対する全身化学療法歴がなく、ECOG PS 0-1の患者を対象とした。また、術前・術後補助療法から6ヵ月以上経過していること、アントラサイクリン系抗癌剤の投与歴がある症例では総投与量がEpirubicin換算で900mg/m2以下であること (本試験の予定投与量を含む)、左室駆出率50%以上の心機能を有することを条件とした。
対象はPSおよび転移の有無で層別化され、Arm A: Rilotumumab (15mg/kg) + Epirubicin + Cisplatin + Capecitabine (ECX) 療法、Arm B: Rilotumumab (7.5mg/kg) + ECX療法、Arm C: placebo + ECX療法の3群に無作為に割り付けられた (図1)。
対象はPSおよび転移の有無で層別化され、Arm A: Rilotumumab (15mg/kg) + Epirubicin + Cisplatin + Capecitabine (ECX) 療法、Arm B: Rilotumumab (7.5mg/kg) + ECX療法、Arm C: placebo + ECX療法の3群に無作為に割り付けられた (図1)。
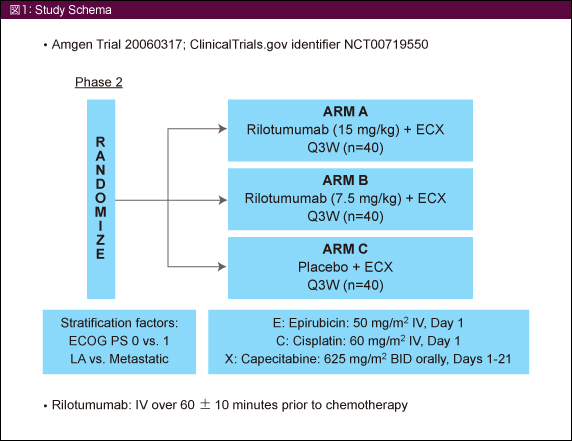
主要評価項目はPFS、副次的評価項目はOS、objective response rate (ORR)、安全性、バイオマーカー解析である。
2009年10月から2010年6月に欧州、北米、アジア、オーストラリアの13ヵ国42施設から121例が登録され、Arm A (40例)、Arm B (42例)、Arm C (39例) の3群に無作為に割り付けられた。
主要評価項目であるPFSの中央値はArm Aで5.3ヵ月、Arm Bで6.8ヵ月、Arm Cでは4.2ヵ月であり、Rilotumumab併用群全体 (Arm A + B) では5.6ヵ月 (HR=0.64, 80% CI: 0.48-0.85) であった (図2)。
主要評価項目であるPFSの中央値はArm Aで5.3ヵ月、Arm Bで6.8ヵ月、Arm Cでは4.2ヵ月であり、Rilotumumab併用群全体 (Arm A + B) では5.6ヵ月 (HR=0.64, 80% CI: 0.48-0.85) であった (図2)。
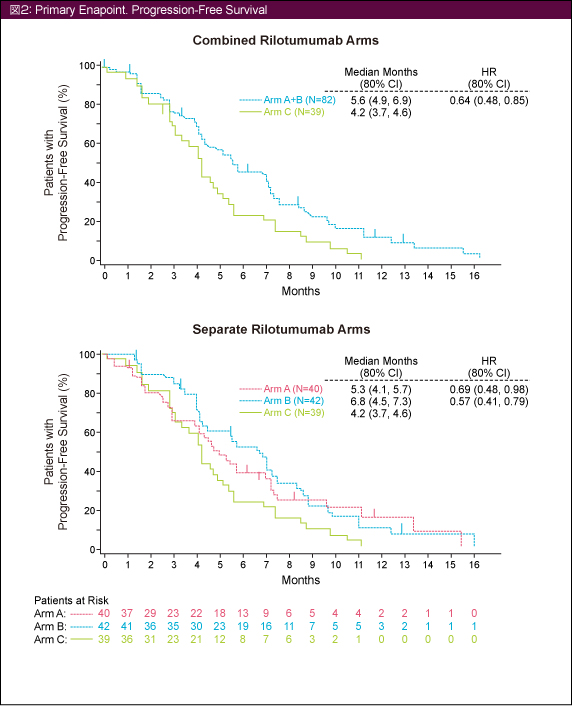
副次的評価項目であるOSの中央値はArm A、B、Cがそれぞれ11.1ヵ月 (HR=0.80, 80% CI: 0.54-1.17)、11.1ヵ月 (HR=0.68, 80% CI: 0.47-0.99)、8.9ヵ月であり、Rilotumumab併用群全体では11.1ヵ月 (HR=0.73, 80%CI: 0.53-1.01) であった。ORRはそれぞれ28%、48%、21%であった。
全Gradeの有害事象の発現頻度はRilotumumab併用群全体で99%、Arm Cでは100%であった。Rilotumumab併用群で高頻度 (Arm Cに比べ10%以上) にみられた有害事象は好中球数減少、末梢性浮腫、脱毛、食欲不振、貧血、血小板数減少、悪心であった。Grade 3以上の有害事象では、好中球数減少および深部静脈血栓症、血小板数減少はRilotumumab群で多く、胸痛および高ビリルビン血症、新生物進行はArm Cで多かった。
免疫組織化学染色 (Immunohistochemistry: IHC) によるc-Met発現についてのバイオマーカー解析は90/118例 (76%) で可能であり、そのうちc-Met高発現例は38例 (42%)、c-Met低発現例は52例 (58%) であった。
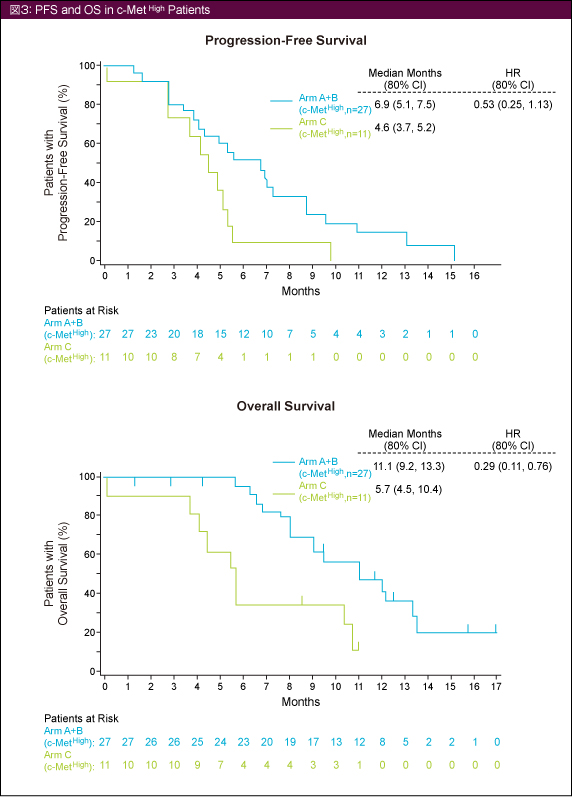
c-Met高発現例におけるPFSの中央値はRilotumumab併用群全体で6.9ヵ月、Arm Cでは4.6ヵ月 (HR=0.53, 80% CI: 0.25-1.13)、OS中央値はそれぞれ11.1ヵ月、5.7ヵ月 (HR=0.29, 80% CI: 0.11-0.76) であった (図3)。
全Gradeの有害事象の発現頻度はRilotumumab併用群全体で99%、Arm Cでは100%であった。Rilotumumab併用群で高頻度 (Arm Cに比べ10%以上) にみられた有害事象は好中球数減少、末梢性浮腫、脱毛、食欲不振、貧血、血小板数減少、悪心であった。Grade 3以上の有害事象では、好中球数減少および深部静脈血栓症、血小板数減少はRilotumumab群で多く、胸痛および高ビリルビン血症、新生物進行はArm Cで多かった。
免疫組織化学染色 (Immunohistochemistry: IHC) によるc-Met発現についてのバイオマーカー解析は90/118例 (76%) で可能であり、そのうちc-Met高発現例は38例 (42%)、c-Met低発現例は52例 (58%) であった。
c-Met高発現例におけるPFSの中央値はRilotumumab併用群全体で6.9ヵ月、Arm Cでは4.6ヵ月 (HR=0.53, 80% CI: 0.25-1.13)、OS中央値はそれぞれ11.1ヵ月、5.7ヵ月 (HR=0.29, 80% CI: 0.11-0.76) であった (図3)。
本第II相試験において示された進行胃癌1st-line治療としてのRilotumumabのECX療法への上乗せ効果は、期待できるものであった。末梢性浮腫および血液毒性の発現頻度はRilotumumab併用群で高いことが確認された。また、バイオマーカー解析の結果から、c-Met高発現例ではRilotumumab併用により高いベネフィットが得られる可能性が示唆された。
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。

