Abstract #3500
KRAS 野生型の切除不能進行・再発大腸癌に対するPanitumumab + Rilotumumab療法またはPanitumumab + Ganitumab療法とPanitumumab単独治療との無作為化比較第Ib/II 相試験
A randomized, phase Ib/II trial of rilotumumab (AMG 102; ril) or ganitumab (AMG 479; gan) with panitumumab (pmab) versus pmab alone in patients (pts) with wild-type (WT) KRAS metastatic colorectal cancer (mCRC): Primary and biomarker analysis
Cathy Eng, et al.

Panitumumabは、KRAS 野生型の切除不能進行・再発大腸癌に対する治療効果を有するEGFRに対する完全ヒト化モノクローナル抗体である。
Rilotumumab (AMG 102) は、c-Met受容体に対するリガンドであるhepatocyte growth factor (HGF) に対する完全ヒト化モノクローナル抗体であり、c-Metの下流シグナルを抑制する。Ganitumab (AMG 479) は、insulin-like growth 1 receptor (IGF-1R) に対する完全ヒト化モノクローナル抗体で、PI3K/AKTとMAPK pathwaysの下流シグナルを抑制する。Panitumumabへのこれらの受容体に対する抗体薬の併用が、相加的あるいは相乗的な抗腫瘍効果を認めるかは明らかではない。
Rilotumumab (AMG 102) は、c-Met受容体に対するリガンドであるhepatocyte growth factor (HGF) に対する完全ヒト化モノクローナル抗体であり、c-Metの下流シグナルを抑制する。Ganitumab (AMG 479) は、insulin-like growth 1 receptor (IGF-1R) に対する完全ヒト化モノクローナル抗体で、PI3K/AKTとMAPK pathwaysの下流シグナルを抑制する。Panitumumabへのこれらの受容体に対する抗体薬の併用が、相加的あるいは相乗的な抗腫瘍効果を認めるかは明らかではない。
Panitumumab (6mg/kg) + placebo群、Panitumumab (6mg/kg) + Rilotumumab (10mg/kg) 群、 Panitumumab (6mg/kg) + Ganitumab (12mg/kg) 群の3群におけるplacebo対照二重盲検無作為化比較試験(第II相試験 Part II)である。
主な適格基準は、KRAS 野生型の切除不能進行・再発大腸癌、PS 0-1、CPT-11 (Irinotecan) 併用かつ/またはL-OHP (Oxaliplatin) 併用化学療法に不応、HbA1c<8%、EGFR、c-MetあるいはIGF-1R抗体薬による治療歴なしである。
主な適格基準は、KRAS 野生型の切除不能進行・再発大腸癌、PS 0-1、CPT-11 (Irinotecan) 併用かつ/またはL-OHP (Oxaliplatin) 併用化学療法に不応、HbA1c<8%、EGFR、c-MetあるいはIGF-1R抗体薬による治療歴なしである。
| ・ | 主要評価項目: ORR (objective response rate) |
| ・ | 副次評価項目: PFS (progression-free survival)、OS (overall survival)、安全性、薬物動態、バイオマーカー解析 |
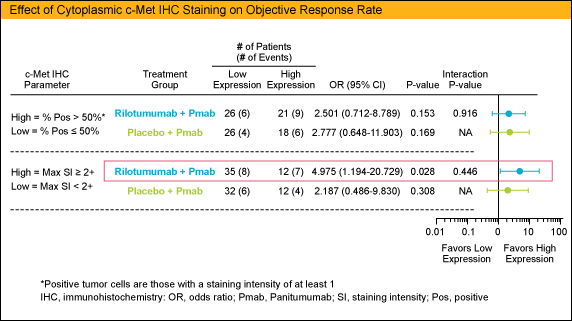
| ・ | c-Metの免疫組織染色による評価 強度(SI)を0-3に分類し、SIが1以上の癌細胞 (positive tumor cells) の癌全体における割合による分類 (High c-Met expression; positive tumor cells > 50%, Low c-Met expression; positive tumor cells ≦ 50%) およびSIの最高強度による分類 (High c-Met expression; SI≧2+, Low c-Met expression; SI<2+) で評価した。 |
2009年6月から2010年2月まで142症例が登録された。追跡期間中央値は6.9ヵ月であり、現在も追跡中である。
ORRは、Panitumumab単独群21%、Rilotumumab併用群31%、Ganitumab併用群22%であった。DCR (disease control rate) は、各56%、71%、61%で、奏効期間中央値は3.7ヵ月、5.1ヵ月、3.7ヵ月であり、Rilotumumab併用群で良好な傾向を認めた。PFS中央値は3.7ヵ月、5.2ヵ月、5.3ヵ月で、Panitumumab単独群に対するハザード比は、Rilotumumab併用群は0.96 (95%CI: 0.61-1.51)、Ganitumab併用群は0.89 (95%CI: 0.56-1.41)であった。
免疫組織染色によるc-MetとORRとの関係において、Rilotumumab併用群で最高強度で評価したHigh群(SI≧2+)はLow群に比べ、オッズ比が4.975 (95%CI: 1.194-20.729、p=0.028)と治療効果が良好であった。
ORRは、Panitumumab単独群21%、Rilotumumab併用群31%、Ganitumab併用群22%であった。DCR (disease control rate) は、各56%、71%、61%で、奏効期間中央値は3.7ヵ月、5.1ヵ月、3.7ヵ月であり、Rilotumumab併用群で良好な傾向を認めた。PFS中央値は3.7ヵ月、5.2ヵ月、5.3ヵ月で、Panitumumab単独群に対するハザード比は、Rilotumumab併用群は0.96 (95%CI: 0.61-1.51)、Ganitumab併用群は0.89 (95%CI: 0.56-1.41)であった。
免疫組織染色によるc-MetとORRとの関係において、Rilotumumab併用群で最高強度で評価したHigh群(SI≧2+)はLow群に比べ、オッズ比が4.975 (95%CI: 1.194-20.729、p=0.028)と治療効果が良好であった。
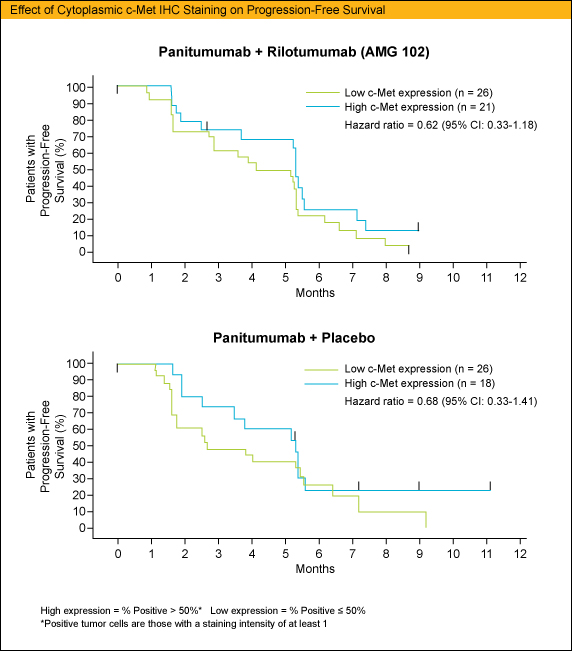
c-Metの染色度とPFSとは無関係であった。
KRAS 野生型の切除不能進行・再発大腸癌に対して、Panitumumab + Rilotumumab療法は、Panitumumab 単独療法に比べ、治療効果の上乗せが認められた。有害事象では、grade 3/4の皮膚障害は高頻度に認められるが、Panitumumab単独群と比べほぼ変わりはなかった。免疫組織染色によるc-Metは、Rilotumumab併用の有効な効果予測因子とは確定できなかった。
ここ数年、大腸癌領域における新薬の開発は滞っているのが現状である(最近、2nd-lineにおけるVEGF trapのpositive dataのプレスリリースがあったが、現時点における詳細は不明)。今回の発表は、2011年 消化器癌シンポジウムで報告されたデータ1)に、バイオマーカー研究が加えられた報告である。本試験は前治療として、CPT-11併用かつ/またはL-OHP併用化学療法に不応となった患者を対象とした試験である。前治療にどの程度の割合でBevacizumabを含んだレジメンが投与されていたのかは不明である。我が国においてconversion therapyやpalliative chemotherapyで腫瘍随伴症状を有する症例など、early tumor shrinkageが必要な患者以外のいわゆる“soft progression”が期待される症例には、1st-lineでBevacizumabを含んだ治療が行われることが多い。それら症例の1st PD後の治療選択を考える上で、M.D. Anderson Cancer CenterのKopez先生のbevacizumab beyond progression (BBP) を否定した探索的な研究報告結果が興味深い。この研究において、画像で増悪が認められる前にVEGF以外のangiogenic factor、HGF、bFGF、PlGFなどのgrowth factorが増加していたことが報告されている2)。そのことからこれらサイトカインを阻害することが必要で、今回の報告で完全ヒト化抗HGF抗体であるRilotumumabではPanitumumabに対する奏効率の上乗せが認められたことは興味深いところである。しかしながらその上乗せ効果が、PFSを含めて素晴らしいものでもなかったことから、患者の絞り込みのできるバイオマーカーが必要である。残念ながら今回取り上げられたc-Metの発現はRilotumumab併用の治療効果予測因子とはならなかったが、今後Rilotumumabの開発を進めていく上で、さらなるバイオマーカー研究が必要であろう。
(レポート: 松阪 諭 監修・コメント: 瀧内 比呂也)

このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。
