 |
 |
| はじめに / テーラーメイド医療
/ HLA抗原 / 日本人の特徴とHLA Typeの頻度 / HLA-oriented
therapyの試み |
| はじめに |
| |
2003年4月、世界ゲノム研究者の国際協力チームおよびセレラ・ジェノミクスはヒトゲノムの全配列の解読が完了したと発表した。約31億個といわれるヒトゲノムの配列決定が終わってもその情報は単なる“情報”に過ぎず、研究者が一番知りたい遺伝子の機能、すなわち、個々の生体反応をつかさどるタンパク質の設計図としての機能やその役割に関してはいまだ完全には解明されていない。
タイミング良く、2002年度のノーベル化学賞は、タンパク質の構造解析に新しい道を切り拓いたジョン・B・フェン博士と田中耕一氏(質量分析〔MS〕法の業績)、およびクルト・ビュートリッヒ博士(核磁気共鳴〔NMR〕法の業績)に贈られたことは記憶に新しい。
ヒトゲノム研究の成果は医療を大きく変化させるのではないかと期待されている。すなわち、万人に同じ医療、例えば白血病には白血病の治療など病名による治療を行った時代から、その患者の遺伝的体質に合った“テーラーメイド医療”、例えばc-kit遺伝子を持った慢性骨髄性白血病や胃GIST(gastrointestinal
stromal tumor)にはメシル酸イマチニブのような分子標的治療を行うことが可能になるだろうと期待されている。 |
| |
▲このページのトップへ |
| テーラーメイド医療 |
| |
テーラーメイド(tailor-made)医療とは、英語でぴったり合った医療(自分が気に入った医療)を意味する。日本語には、テーラーメイド医療に近い言葉として、“オーダーメイド医療”がある。オーダーメイド医療は“レディーメイド医療”に対する言葉として使われてきたが、本来は和製英語であり、レディーメイド(既成)ではない医療、つまり医者が患者の注文に応じて行う医療を意味し、日本においてはテーラーメイド医療とほぼ同じ意味合いで使われている。一方、英語にはテーラーメイド医療と“カスタムメイド(custom-made)医療”という言葉があり、後者は医者または患者が注文した医療を意味する。昨今、医学界で言われているのは、遺伝的体質に合ったテーラーメイド医療のことであり、“治療の個別化”とも言われる。また、最近では、先に述べたメシル酸イマチニブに代表されるような癌細胞の異常分子に特異的に働く薬剤を用いる“分子標的治療”も同様な概念として使われている。しかし、将来的には“カスタム・テーラーメイド医療”、すなわち治療法または治療薬剤のメニューが示され、自分にぴったり合った、気に入った医療が行われることが理想ではないかと考えられる1)。
著者が行っているHLA分子(phenotype)を用いた“癌治療の個性化”の試みを以下に紹介する。 |
| |
▲このページのトップへ |
| HLA抗原 |
| |
ヒトの主要組織適合遺伝子複合体(MHC:major histocompatibility complex)はHLA抗原(human
leukocyte antigen)と呼ばれ、第6染色体の短腕(6p21.3)上に存在する。HLA抗原は、高度な遺伝的多型性を示す細胞膜糖蛋白質、いわゆる受容体であり、すべての細胞表面上にはその人に特有なHLA分子があり、この分子によって自己と非自己を区別し、病気の感受性や免疫応答調節などをコントロールすると考えられている。
最近では、遺伝子のSNPs(single nucleotide polymorphisms)が疾患および薬剤感受性などに関与すると注目されているが、HLA遺伝子はヒト遺伝子群の中では遺伝子多型(polymorphism)を示す最も代表的な遺伝子である。これまでに、HLA領域は遺伝子の多様性だけでなく、タンパク質の立体構造や機能が詳しく研究されていることもあり、HLAに合わせた腫瘍抗原に対するパーソナルワクチンはテーラーメイド医療の1つの具体例として臨床的にも行われている。しかし、臨床ではその有効性はいまだ確認されていない。
|
| |
▲このページのトップへ |
| 日本人の特徴とHLA Typeの頻度 |
| |
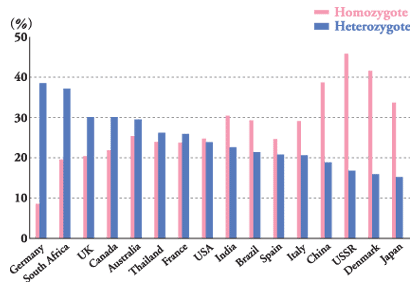
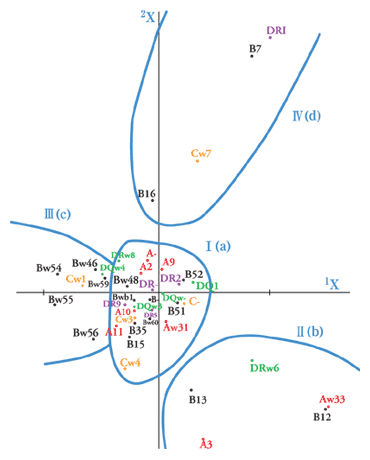
親から同じ対立遺伝子をもらった人(homozygote:ホモ接合体)、異なった対立遺伝子をもらった人(heterozygote:ヘテロ接合体)の頻度を検討した結果、日本人は世界で最もheterozygoteを示す頻度が少なく、遺伝子的に似通っていることがわかる(図1)2)。よって、遺伝子的には日本人はみな家族であり、同じような遺伝子を持つ人を見つけやすいことがわかるが、一方でhomozygoteの人は、癌になりやすいこともわかってきた3)。しかし、そのことが日本人には幸いし、質的事象を分類する多変量分析の一つである数量化III類を用いると、日本人のHLA遺伝子情報を4つのTypeに分類することができる(図2)4)。 |
| 図1:HLA抗原の多様性の頻度(n=7,979) |
| |
 |
| |
|
| 図2:数量化III類による胃癌症例のHLAの分類(胃癌626例) |
| |
 |
| |
|
| |
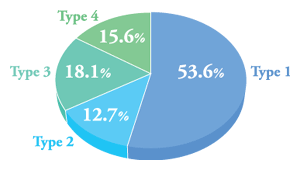
また、著者らの検討によると、胃癌患者1,926例では、HLA Typeの頻度はType1、2、4はそれぞれ約54%、13%、16%で、Type
3は18%であった(図3)。さらに約10〜15年間にわたり治療を行い、予後が確認された胃癌患者1,559例では、HLA TypeごとにCox-multivariate
analysisの推定生存曲線をみると、Type1、2、4の患者はPSKを用いた免疫化学療法が、Type 3の患者は化学療法が良好である結果が示された(図4)。注目すべき点は、同じ治療薬剤を使用しても、HLA
Typeによって、予後を悪くしていることもあるということである。欧米で中心に行われている化学療法はType 3の患者のみに効果が見られる。Type 3の患者の頻度に注目すると化学療法の効果は多くて15〜30%になることが理解できる。
現在、著者らは術前にHLA抗原を測定し、その患者と同じHLA Typeの過去の患者データを解析することにより、有効な治療法が存在すれば、その治療法を推薦し施行するという“HLA-oriented
therapy”を行っている。有効な治療法とその患者グループの同定を行い、新しい患者ごとに適した治療を行う方法であり、日本人のHLA遺伝子の特徴を利用し、患者同士のお見合い(pair-matching)を遺伝子情報で行っているのである。つまり、この治療は癌治療の“個別化”ではなく“個性化”であると考えている。現在ではType
1、2、4の患者にはPSKおよびフッ化ピリミジン剤を併用した免疫化学療法を推薦し、Type 3の患者にのみフッ化ピリミジン剤を使用した化学療法を推薦している。 |
| 図3:HLA Type の頻度(n=1,926) |
| |
 |
| |
|
| 図4:推定生存曲線(胃癌n=1,559) |
| |
| |
▲このページのトップへ |
| HLA-oriented therapyの試み |
| |
現在、著者らが行っているHLA-oriented therapyは“カスタム・テーラーメイド医療”であるが、その結果を一部紹介する。インフォームドコンセントを行い同意が得られた胃癌患者(pTNM
stage 1B-4、n=76)に対して術前にHLA抗原を測定し、胃切除術後にType 1、2、4の患者はPSKを用いた免疫化学療法を、Type 3の患者にはフッ化ピリミジン剤を用いた化学療法を行った。一方、HLA抗原の測定を希望しなかった同時期の胃癌患者(pTNM
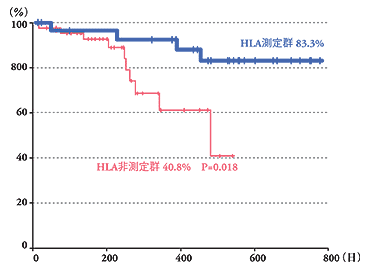
stage 1B-4、n=101)には胃切除術後、PSKを用いた免疫化学療法と化学療法を交互に施行した。その結果、HLA抗原を測定した患者すべてにHLA-oriented
therapyが施行されてはいないが、HLA抗原を測定した患者群は非測定群に比べ統計学的な有意差をもって生存率が良好であることが示された(図5)5)。今後、症例を増やすべく検討中である。 |
図5:生存曲線 |
| |
 |
| |
|
| ■文献 |
| |
| 1) |
生越喬二:癌のテーラーメード治療の現況
日本医事新報4106:138-139,2003 |
| 2) |
Ogoshi K,et al.Incidence of heterozygotes and homozygotes of
major histocompatibility complex in Japanese compared to non-Japanese.
Ann Cancer Res Ther 9:87-98,2001 |
| 3) |
Ogoshi K,et al.Heterozygote advantage at major histocompatibility
complex(MHC)molecules and cancer risk.
Ann Cancer Res Ther 9:73-86,2001 |
| 4) |
Hayashi F,et al.Classification of gastric cancer patients based
on HLA antigen expression using quantification method III. Ann Cancer Res Ther
3:117-120,1994 |
| 5) |
Ogoshi K,et al.A prospective study of HLA-oriented therapy:
An attempt to predictive the response to anti-cancer therapy in gastric cancer.
Ann Cancer Res Ther 8(1&2):155-167,2001 |
|
| |
2003年6月発行 |

