|
���̃T�C�g�͈�ÊW�҂̕��X��Ώۂɍ쐬���Ă��܂��B�K�������p�K���ɓ��ӂ̏�A�����p���������B�L�����e�Ŏ��グ����܂̌��\�E���ʂ���їp�@�E�p�ʂɂ́A���{���� �ŏ��F����Ă�����e�ƈقȂ���̂��A�����Ɋ܂܂�Ă��܂��̂ł����ӂ��������B
|

�؏��s�\�i�s�E�Ĕ��咰����1st-line���Âɂ�����FOLFOXIRI + Bevacizumab vs. FOLFIRI + Bevacizumab�̑�III�������̌��� (TRIBE����)
FOLFOXIRI plus Bevacizumab (Bev) vs FOLFIRI plus Bev as 1st-line Treatment of Metastatic Colorectal Cancer: Results of the Phase III Randomized TRIBE trial.
Fotios Loupakis, et al.

�זE�Ő���܂�3�ܕ��p���W���� + Bevacizumab�́A2�ܕ��p���W�����ɑ��Đ����ɗD�z�����o���邩�H

�@�Ő����������Ƃ��番�q�W�I��̃v���b�g�t�H�[���Ƃ��Ă̗L�p���͌��O����Ă������A����̕��������Bevacizumab���p�̔E�e���͂���Ƃ����悤�BGONO�O���[�v�̑�III�������ł�FOLFIRI vs. FOLFOXIRI��PFS (progression-free survival) ��6.9���� vs. 9.8�����A�t������41% vs. 66% (central review�ł�34% vs. 60%) �ł���APFS�ɂ�����Bevacizumab���p�̈Ӌ`�͂��肻�������A���̃��W�����̖��͂ł������t�����͌��サ�Ă��Ȃ��B�Ȃ��A���O���ꂽ�Ő��͑傫�ȈႢ�͂Ȃ������ł���B
�@���Տ��̑�����FOLFIRI/FOLFOX�̒������^����b�Ƃ��A����ɕ��q�W�I��p������헪���Ƃ��Ă���B���̃��W�����ɈӋ`�����邩�͐����̐��т�����Ă���c�_���ׂ��ł��낤�B
�@Doublet (2�ܕ��p) + Bevacizumab (Bev) ���W�����́A�؏��s�\�i�s�E�Ĕ��咰����1st-line�ɂ�����W�����Âł���2, 3) �B����AGONO�O���[�v�̑�III�������ł́Adoublet��FOLFIRI�ɑ�triplet (3�ܕ��p) ��FOLFOXIRI���t�����APFS �AOS (overall survival) �ŗD��Ă��邱�Ƃ�������Ă���4) �AFOLFOXIRI + Bev�̗L�����E���S��������������II������ (n=57) �ł́APFS�����l13.1�����A�t����77%�ƁA�����L�����ƈ��S�����F�߂�ꂽ5)�B
�@�{�����́A�؏��s�\�i�s�E�Ĕ��咰����1st-line�ł�Bev���p���ɂ�����AFOLFIRI �ɑ���FOLFOXIRI�̗D�z���������邱�Ƃ�ړI�Ƃ��Ď��{���ꂽ�B
�@�{�����́A�؏��s�\�i�s�E�Ĕ��咰����1st-line�ł�Bev���p���ɂ�����AFOLFIRI �ɑ���FOLFOXIRI�̗D�z���������邱�Ƃ�ړI�Ƃ��Ď��{���ꂽ�B
�@�؏��s�\�i�s�E�Ĕ��咰�����҂��A�{�݁APS 0/1-2�A�p��⏕���w�Ö@��w�ʈ��q�Ƃ��āAFOLFIRI + Bev�Q ��FOLFOXIRI + Bev�Q�Ƃ� 1:1�̊����Ŗ���ׂɊ���t���� (�}1) �B�Ȃ��A���Q�Ƃ���2�T�Ԃ�1�T�C�N���Ƃ���12�T�C�N���܂œ��^���A���̌�͈ێ��Ö@�Ƃ���5-FU + Bev��PD�ƂȂ�܂Ŏ��{�����B
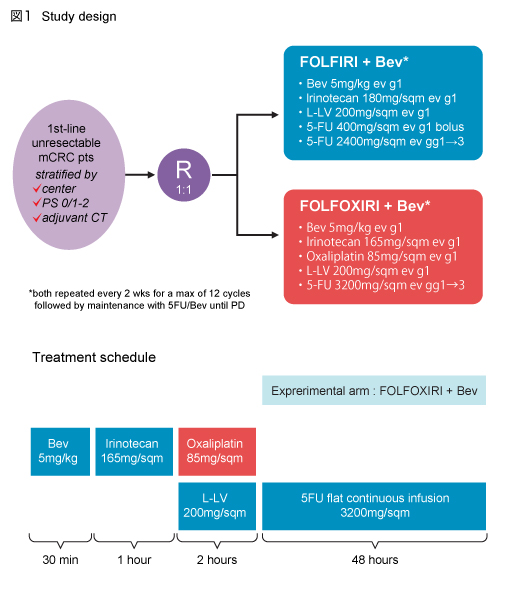
�@��ȓK�i��́A�g�D�w�I�ɑB���Ɛf�f����ARECIST 1.0�ɂ�葪��\��1�ȏ�̕a�ς�L���A�]�ڑ��ɑ��đO���Â��s���Ă��Ȃ��؏��s�\�i�s�E�Ĕ��咰�����҂ł���A�N��18�`75�AECOG PS 2�ȉ� (71�`75�̏ꍇ��PS 0) �A�����E�́E�t�@�\������Ȋ��҂Ƃ����B�Ȃ��AL-OHP���܂ޏp��⏕���w�Ö@�����{�������҂ɂ����ẮA���ÏI���ォ�珉��Ĕ��܂ł̊��Ԃ�12�����ȏ�ł�����e�����B
�@��v�]�����ڂ�PFS�ł���A�����]�����ڂ͑t�����AR0�؏����AOS�A���S���A�o�C�I�}�[�J�[�ɂ��]���Ƃ����B�Ȃ��AFOLFIRI + Bev��PFS�����l��11�����Ɖ��肵��6) �AFOLFOXIRI + Bev��HR=0.75�ŗD�z���������Ɛݒ肵���ꍇ (�L�Ӑ�������5%�A���o��80%) �A�K�v�Ǘᐔ��379��ł������B
�@��v�]�����ڂ�PFS�ł���A�����]�����ڂ͑t�����AR0�؏����AOS�A���S���A�o�C�I�}�[�J�[�ɂ��]���Ƃ����B�Ȃ��AFOLFIRI + Bev��PFS�����l��11�����Ɖ��肵��6) �AFOLFOXIRI + Bev��HR=0.75�ŗD�z���������Ɛݒ肵���ꍇ (�L�Ӑ�������5%�A���o��80%) �A�K�v�Ǘᐔ��379��ł������B
�@508�Ⴊ�o�^����AFOLFIRI + Bev�Q��256��AFOLFOXIRI + Bev�Q��252�Ⴊ����t����ꂽ�B�Ȃ��A���Q�Ԃ̊��Ҕw�i�ɑ傫�ȈႢ�݂͂��Ȃ������B
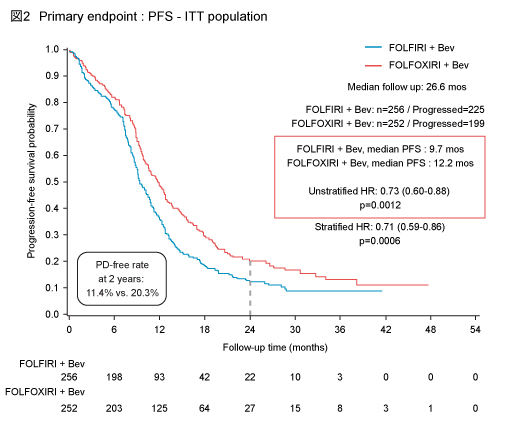
�@��v�]�����ڂ�PFS�����l�́AFOLFIRI + Bev�Q9.7�����ɑ���FOLFOXIRI + Bev�Q12.2�����ł���AFOLFOXIRI + Bev�Q�ŗL�ӂȉ������F�߂�ꂽ (HR=0.73, 95% CI: 0.60-0.88, p=0.0012) (�}2) �B�܂��A2�NPFS��FOLFIRI + Bev�Q11.4%�AFOLFOXIRI + Bev�Q20.3%�ł������B
�@��v�]�����ڂ�PFS�����l�́AFOLFIRI + Bev�Q9.7�����ɑ���FOLFOXIRI + Bev�Q12.2�����ł���AFOLFOXIRI + Bev�Q�ŗL�ӂȉ������F�߂�ꂽ (HR=0.73, 95% CI: 0.60-0.88, p=0.0012) (�}2) �B�܂��A2�NPFS��FOLFIRI + Bev�Q11.4%�AFOLFOXIRI + Bev�Q20.3%�ł������B
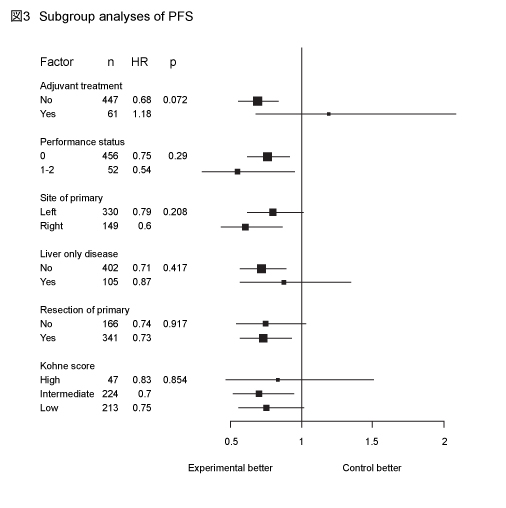
�@�T�u�O���[�v��͂ł́A�p��⏕���w�Ö@�����Ǘ�̂�FOLFOXIRI + Bev�Q�����X���ɂ��������̂́A�p��⏕���w�Ö@�̗L���ɂ����đ��݊W�݂͂��Ȃ����� (p=0.072) (�}3) �B
�@�t�����́AFOLFIRI + Bev�Q53%�ɑ���FOLFOXIRI + Bev�Q65%�ł���AFOLFOXIRI + Bev�Q�ŗL�ӂɍ������� (p=0.006) �B
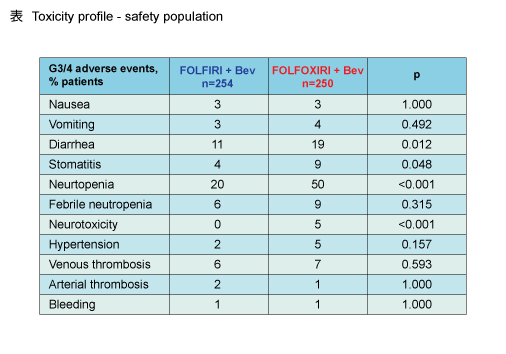
�@���S���Ɋւ��āA�d�ĂȗL�Q���ہA�v���I�ȗL�Q���ہA���Ê֘A���A�������S�́A���Q�Ԃłقړ����ł������BGrade 3/4�̗L�Q���ۂł́A���� (p=0.012) �A������ (p=0.048) �A�D�������� (p<0.001) ���AFOLFOXIRI + Bev�Q�ɂ����ėL�ӂɍ������� (�\) �B�Ȃ��A���M���D���������ǂ�FOLFOXIRI + Bev�Q�ő����X�����݂�ꂽ���̂́A�L�Ӎ��͔F�߂��Ȃ����� (p=0.315) �B
�@���S���Ɋւ��āA�d�ĂȗL�Q���ہA�v���I�ȗL�Q���ہA���Ê֘A���A�������S�́A���Q�Ԃłقړ����ł������BGrade 3/4�̗L�Q���ۂł́A���� (p=0.012) �A������ (p=0.048) �A�D�������� (p<0.001) ���AFOLFOXIRI + Bev�Q�ɂ����ėL�ӂɍ������� (�\) �B�Ȃ��A���M���D���������ǂ�FOLFOXIRI + Bev�Q�ő����X�����݂�ꂽ���̂́A�L�Ӎ��͔F�߂��Ȃ����� (p=0.315) �B
�@�܂��A���w�Ö@�̃T�C�N������FOLFOXIRI + Bev�Q11�AFOLFIRI + Bev�Q12�Ɨ��Q�Ԃɍ��͂Ȃ��������̂́A�זE�Ő��R���܂̑����^�ʂ͂��ꂼ��73�`75%�A83�`84%�ƁAFOLFOXIRI + Bev�Q�ŒႢ�X�����݂�ꂽ�B
�@FOLFOXIRI��FOLFIRI�ɑ��ABev���p�ɂ����Ă�PFS�ŗD�z�����������B�L�Q���ۂ́AFOLFOXIRI + Bev�ő����݂�ꂽ���A���e�ł�����̂ł������B�{�����őΏۂƂȂ������ҌQ�ɂ����ẮAFOLFOXIRI + Bev���p�Ö@���A�V���Ȏ��ÃI�v�V�����ƂȂ邱�Ƃ������ꂽ�B�Ȃ��A�Đ؏��APD��̎��ÁAOS�A�o�C�I�[�}�[�Ɋւ����͂͌��ݐi�s���ł���B
Reference
1) Sunakawa Y, et al.: Oncology. 82(4): 242-248, 2012�@�mPubMed�n
2) Hurwitz H, et al.: N Engl J Med. 350(23): 2335-2342, 2004�@�mPubMed�n�m�_���Љ��n
3) Saltz LB, et al.: J Clin Oncol. 26(12): 2013-2019, 2008�@�mPubMed�n
4) Falcone A, et al.: J Clin Oncol. 25(13): 1670-1676, 2007�@�mPubMed�n�m�_���Љ��n
5) Masi G, et al.: Lancet Oncol. 11(9): 845-852, 2010�@�mPubMed�n
6) Sobrero A, et al.: Oncology. 77(2): 113-119, 2009�@�mPubMed�n
1) Sunakawa Y, et al.: Oncology. 82(4): 242-248, 2012�@�mPubMed�n
2) Hurwitz H, et al.: N Engl J Med. 350(23): 2335-2342, 2004�@�mPubMed�n�m�_���Љ��n
3) Saltz LB, et al.: J Clin Oncol. 26(12): 2013-2019, 2008�@�mPubMed�n
4) Falcone A, et al.: J Clin Oncol. 25(13): 1670-1676, 2007�@�mPubMed�n�m�_���Љ��n
5) Masi G, et al.: Lancet Oncol. 11(9): 845-852, 2010�@�mPubMed�n
6) Sobrero A, et al.: Oncology. 77(2): 113-119, 2009�@�mPubMed�n
