|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。
|

Abstract #LBA385
標準化学療法不応の切除不能進行・再発大腸癌患者に対するRegorafenibの有用性を検討した多施設共同プラセボ対照二重盲検無作為化比較第III相試験 (CORRECT試験)
Results of a phase III randomized, double-blind, placebo-controlled, multicenter trial (CORRECT) of Regorafenib plus best supportive care (BSC) versus placebo plus BSC in patients with metastatic colorectal cancer (mCRC) who have progressed after standard therapies
Axel Grothey, et al.

切除不能進行・再発大腸癌サルベージライン化学療法における新たな標準治療の確立

Regorafenibは腫瘍の血管新生にかかわるVEGFR、TIE-2を標的にするほか、腫瘍増殖にかかわるRAFなどにも阻害作用をもつとされ、第I相試験の大腸癌症例における結果ではKRAS 変異の有無に依存せず効果を発揮することが報告され1)、期待された薬剤であった。大腸癌で初めて有効性を示した低分子化合物となったが、単剤でのサルベージラインでの開発が成功に結びついた主因であると考えられる。
今後、本邦でも承認申請がなされると思われるが、同効薬のSorafenibと同様に手足症候群、倦怠感、高血圧、下痢、皮疹のgrade 3以上のものが少なからず認められ、日本では肝不全死亡例も1例認められることより、慎重な対応が必要であると考えられる。本試験においては100例の日本人症例が登録されており、有効性や安全性のサブ解析結果が待たれるところである。
現在、同様の対象に対して第II相比較試験で有効性の示されたAkt阻害剤Perifosineや代謝拮抗剤TAS-102の後期開発がなされており2-4)、今後サルベージラインでの治療戦略が大きく変わってくるものと思われる。
Regorafenibは経口マルチキナーゼ阻害剤であり、血管新生に関わる受容体型チロシンキナーゼ (VEGFR 1-3, TIE2) および間質系に関わる受容体型チロシンキナーゼ (PDGFR-β, FGFR)、発癌に関与する受容体型チロシンキナーゼ (KIT, PDGFR, RET) に対する阻害作用を有する5)。
CORRECT試験は、標準化学療法に不応の切除不能進行・再発大腸癌患者に対するRegorafenibの有用性を評価する多施設共同プラセボ対照二重盲検無作為化比較第III相試験である。
CORRECT試験は、標準化学療法に不応の切除不能進行・再発大腸癌患者に対するRegorafenibの有用性を評価する多施設共同プラセボ対照二重盲検無作為化比較第III相試験である。
◆対象
標準化学療法 (Fluoropyrimidine、Irinotecan、Oxaliplatin、Bevacizumab、抗EGFR抗体薬 [KRAS 野生型の場合]) 6) を2レジメン以上施行された切除不能進行・再発大腸癌患者。年齢18歳以上、ECOG PS 0/1、期待余命3ヵ月以上。
◆方法
対象をRegorafenib + BSC群(以下Regorafenib群) とplacebo + BSC群 (以下placebo群) に2:1の割合で無作為に割り付けた (図1)。Regorafenib (160mg/日、経口) を3週投与1週休薬の4週1サイクルとして、病勢進行、死亡、副作用により投与が継続できない状態のいずれかが認められるまで継続した。
主要評価項目はoverall survival (OS)、副次評価項目はprogression-free survival (PFS)、奏効率、disease control rate (DCR) とした。
標準化学療法 (Fluoropyrimidine、Irinotecan、Oxaliplatin、Bevacizumab、抗EGFR抗体薬 [KRAS 野生型の場合]) 6) を2レジメン以上施行された切除不能進行・再発大腸癌患者。年齢18歳以上、ECOG PS 0/1、期待余命3ヵ月以上。
◆方法
対象をRegorafenib + BSC群(以下Regorafenib群) とplacebo + BSC群 (以下placebo群) に2:1の割合で無作為に割り付けた (図1)。Regorafenib (160mg/日、経口) を3週投与1週休薬の4週1サイクルとして、病勢進行、死亡、副作用により投与が継続できない状態のいずれかが認められるまで継続した。
主要評価項目はoverall survival (OS)、副次評価項目はprogression-free survival (PFS)、奏効率、disease control rate (DCR) とした。
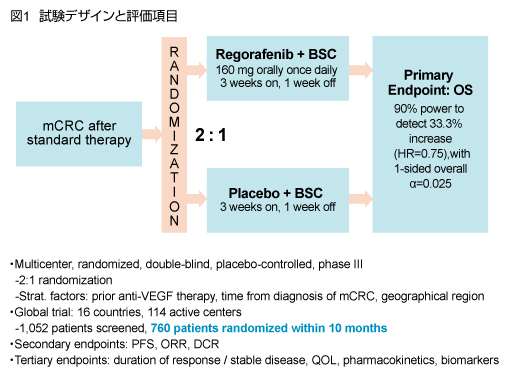
2010年5月-2011年3月の間に1,052例がスクリーニングされ、760例が登録された。Regorafenib群は505例、placebo群は255例であった。
両群の患者背景に有意な差はみられなかった。年齢中央値は両群とも61歳、男性はRegorafenib群61.6%、placebo群60.0%、白人は各々77.6%、78.8%、ECOG PS 0は52.5%、57.3%、KRAS 変異型は54.1%、61.6%であった。前治療は3レジメン以上が各々83.8%、84.3%であり、Bevacizumab投与歴は両群とも100%であった。
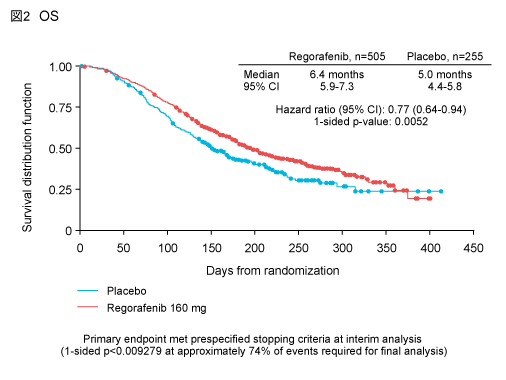
主要評価項目であるOSの中央値はRegorafenib群が6.4ヵ月、placebo群は5.0ヵ月であり (HR=0.77, 95% CI: 0.64-0.94, p=0.0052)、Regorafenib群でOSが有意に延長した (図2)。
両群の患者背景に有意な差はみられなかった。年齢中央値は両群とも61歳、男性はRegorafenib群61.6%、placebo群60.0%、白人は各々77.6%、78.8%、ECOG PS 0は52.5%、57.3%、KRAS 変異型は54.1%、61.6%であった。前治療は3レジメン以上が各々83.8%、84.3%であり、Bevacizumab投与歴は両群とも100%であった。
主要評価項目であるOSの中央値はRegorafenib群が6.4ヵ月、placebo群は5.0ヵ月であり (HR=0.77, 95% CI: 0.64-0.94, p=0.0052)、Regorafenib群でOSが有意に延長した (図2)。
副次評価項目であるPFSの中央値はRegorafenib群で1.9ヵ月、placebo群では1.7ヵ月 (HR=0.49, 95% CI: 0.42-0.58, p<0.000001)であった。DCRは各々44.8%、15.3% (p<0.000001)、奏効率は1.0%、0.4%であった。
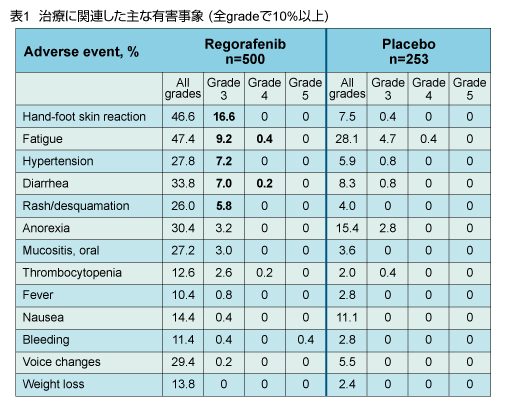
治療に関連した主な有害事象を表1に示す。治療中止につながる有害事象の発現頻度はRegorafenib群で8.2%、placebo群で1.2%であった。
治療に関連した主な有害事象を表1に示す。治療中止につながる有害事象の発現頻度はRegorafenib群で8.2%、placebo群で1.2%であった。
また、Regorafenib群ではplacebo群に比べ肝機能値の上昇が高頻度であったが (ALT: Regorafenib群 vs. placebo群 = 45.2% vs. 29.8%, AST: 65.0% vs. 45.6%, ビリルビン: 44.4% vs. 17.5%)、その多くはgrade 1/2であった。ただし、日本人でRegorafenibに関連すると思われる致死的な薬剤性肝障害が1例報告され、注意深いモニタリングが推奨された。
Regorafenibは標準化学療法6) に不応な切除不能進行・再発大腸癌患者において、OSを有意に改善した。Regorafenibは、大腸癌に対して有用性を示した初の低分子マルチキナーゼ阻害剤であり、標準化学療法に不応な切除不能進行・再発大腸癌患者における新たな標準薬になり得る。
Reference
1) Strumberg D, et al.: 2009 Annual Meeting of the American Society of Clinical Oncology®: abst #3560
2) Richard DA, et al.: 2010 Annual Meeting of the American Society of Clinical Oncology®: abst #3531
3) Clinical Trials.gov: Perifosine Plus Capecitabine Versus Placebo Plus Capecitabine in Patients With Refractory Advanced Colorectal Cancer (X-PECT)
4) Yamazaki K, et al.: 9th Annual Meeting of Japanese Society of Medical Oncology: PL-01, 2011
5) Wilhelm SM, et al.: Int J Cancer. 129(1): 245-255, 2011 [PubMed]
6) NCCN Clinical Practice Guideline in Oncology, Colon Cancer, 2012, version 2
1) Strumberg D, et al.: 2009 Annual Meeting of the American Society of Clinical Oncology®: abst #3560
2) Richard DA, et al.: 2010 Annual Meeting of the American Society of Clinical Oncology®: abst #3531
3) Clinical Trials.gov: Perifosine Plus Capecitabine Versus Placebo Plus Capecitabine in Patients With Refractory Advanced Colorectal Cancer (X-PECT)
4) Yamazaki K, et al.: 9th Annual Meeting of Japanese Society of Medical Oncology: PL-01, 2011
5) Wilhelm SM, et al.: Int J Cancer. 129(1): 245-255, 2011 [PubMed]
6) NCCN Clinical Practice Guideline in Oncology, Colon Cancer, 2012, version 2
