|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。
|

Abstract #LBA3
化学療法歴を有する進行胃癌患者におけるEverolimusの第III相試験:GRANITE-1試験
Phase 3 Trial of Everolimus in Previously Treated Patients with Advanced Gastric Cancer: GRANITE-1
Eric Van Cutsem, et al.

標的は何処へ

LBAということでpositiveな結果を期待していたが、発表された結果は非常に残念なものであった。主要評価項目のoverall survival (OS) ではEverolimus投与により約1ヵ月の延長が認められたものの有意な差は得られず、副次評価項目のprogression-free survival (PFS) では有意な差が認められているとはいえ、その差はわずかに8日であった。Waterfall plotを見るとEverolimus群では確かに腫瘍縮小は得られているが、生存の延長に結びつかなかったことになる。サブグループ解析においても大きな偏りは認められず、有効性が高そうな集団を抽出することは困難であった。今後はバイオマーカーの研究が予定されており、その結果が期待されるところである。しかし、単一のマーカーで効果を予測することはおそらく不可能であり、リン酸化プロテオーム解析のような手法により、分子の活性化の状態を含めた網羅的な検討が必要とされるものと思われる。
それにしても標的に届かないのか、標的が消えてしまったのか。分子標的治療薬の開発では継続的にproof of conceptを検証していく必要があるのかもしれない。
胃癌は進行が早く治療が困難であり2)、進行・転移した場合の5年生存率は5%未満である3,4)。進行胃癌に対する2nd-line以降の化学療法は未だ確立されていない。
Everolimusは経口のmTOR阻害薬であり、細胞増殖、代謝および血管新生の主要調節因子であるPI3K/Akt/mTOR経路を阻害する。同剤は前臨床試験および第I相試験5) で胃癌に対する効果を示し、日本での進行胃癌53例を対象とした第II相試験においても効果と安全性が認められたことから1)、その有用性が期待されている。
Everolimusは経口のmTOR阻害薬であり、細胞増殖、代謝および血管新生の主要調節因子であるPI3K/Akt/mTOR経路を阻害する。同剤は前臨床試験および第I相試験5) で胃癌に対する効果を示し、日本での進行胃癌53例を対象とした第II相試験においても効果と安全性が認められたことから1)、その有用性が期待されている。
本試験は国際共同プラセボ対照二重盲検無作為化比較第III相試験である。適格基準は18歳以上、胃および胃食道接合部 (腫瘍の大半が胃に位置する場合) 腺癌と確定診断されている、1st-lineまたは2nd-line治療で病勢進行の記録がある、ECOG PS 2以上、骨髄および腎・肝機能が十分に保たれている、とした。3ライン以上の化学療法歴がある患者は除外した。
対象をEverolimus群 (10mg/日 + best supportive care [BSC]) とplacebo群 (placebo + BSC) に2:1の割合で無作為に割り付けた (図1)。
対象をEverolimus群 (10mg/日 + best supportive care [BSC]) とplacebo群 (placebo + BSC) に2:1の割合で無作為に割り付けた (図1)。
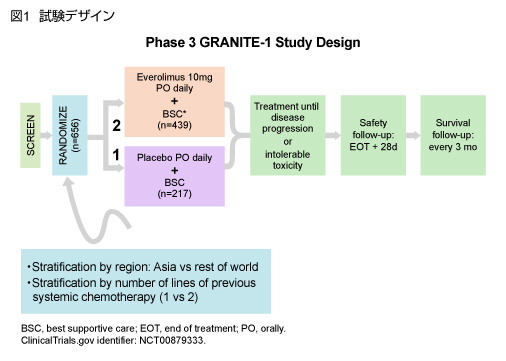
主要評価項目はOS、副次評価項目はPFS、奏効率、安全性、PS低下までの期間、QOL低下までの期間とした。探索的評価項目はバイオマーカーと臨床的評価項目との相関である。
90%の検出力で両群の死亡リスクに26%の差 (OS: placebo群4.0ヵ月 vs. Everolimus群5.4ヵ月に相当) を検出するための必要症例数は633例とし、最終解析は526例の死亡イベントが発生した時点で実施することとした。
90%の検出力で両群の死亡リスクに26%の差 (OS: placebo群4.0ヵ月 vs. Everolimus群5.4ヵ月に相当) を検出するための必要症例数は633例とし、最終解析は526例の死亡イベントが発生した時点で実施することとした。
2009年7月-2010年12月の間に23ヵ国から656例が登録された。Everolimus群439例、placebo群217例に無作為に割り付けられた。患者背景は男性73.6%、アジアからの登録55.3%、化学療法歴1ライン47.7%、胃切除術を受けた患者は50.2%であり、両群間に差はみられなかった。
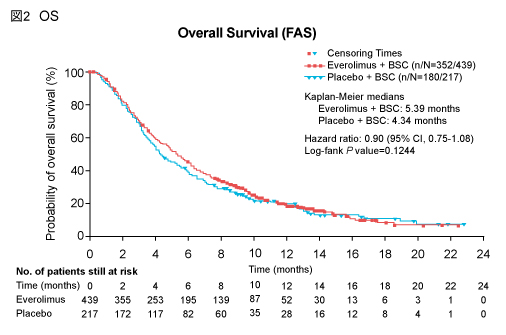
主要評価項目であるOSの中央値はEverolimus群で5.39 ヵ月、placebo群では4.34ヵ月であり、有意な延長は示されなかった (HR=0.90, 95% CI: 0.75-1.08, p=0.1244) (図2)。層別因子 (化学療法歴、地域) 別のOSでは、アジア以外の地域においてEverolimus群でやや良好な傾向がみられたが (HR=0.85, 95% CI: 0.65-1.10)、いずれも有意ではなかった。
主要評価項目であるOSの中央値はEverolimus群で5.39 ヵ月、placebo群では4.34ヵ月であり、有意な延長は示されなかった (HR=0.90, 95% CI: 0.75-1.08, p=0.1244) (図2)。層別因子 (化学療法歴、地域) 別のOSでは、アジア以外の地域においてEverolimus群でやや良好な傾向がみられたが (HR=0.85, 95% CI: 0.65-1.10)、いずれも有意ではなかった。
PFSの中央値はEverolimus群で1.68ヵ月、placebo群で1.41ヵ月であり、Everolimus群で有意な延長が認められた (HR=0.66, 95% CI: 0.56-0.78, p<0.0001)。奏効率は各々4.5%、2.1%であった。
全有害事象の発現頻度はEverolimus群で99.1%、placebo 群では96.7%、grade 3/4の有害事象は各々70.9%、53.5%、重篤な有害事象は47.4%、41.4%であった。主なGrade 3/4の有害事象は貧血 (各々16.0%、12.6%)、食欲不振 (11.0%、5.6%)、疲労 (7.8%、5.1%) などであった。
全有害事象の発現頻度はEverolimus群で99.1%、placebo 群では96.7%、grade 3/4の有害事象は各々70.9%、53.5%、重篤な有害事象は47.4%、41.4%であった。主なGrade 3/4の有害事象は貧血 (各々16.0%、12.6%)、食欲不振 (11.0%、5.6%)、疲労 (7.8%、5.1%) などであった。
1st-lineならびに2nd-line治療で病勢進行が認められた進行胃癌患者において、Everolimus単剤投与によるOSの有意な延長は示されなかった。一方、PFSはEverolimus単剤投与により、placebo群と比較して有意な延長が認められた。安全性プロファイルは他癌腫で報告されたものと同等であった。現在、バイオマーカーの解析が進行中である。
Reference
1) Doi T, et al.: J Clin Oncol. 28(11): 1904-1910, 2010 [PubMed]
2) Catalano V, et al.: Crit Rev Oncol Hematol. 71(2): 127-164, 2009 [PubMed]
3) American Cancer Society. Cancer Facts & Figures 2011
4) Matsuda T, et al.: Jpn J Clin Oncol. 41(1): 40-51, 2011 [PubMed]
5) Okamoto I, et al.: Jpn J Clin Oncol. 40(1): 17-23, 2010 [PubMed]
1) Doi T, et al.: J Clin Oncol. 28(11): 1904-1910, 2010 [PubMed]
2) Catalano V, et al.: Crit Rev Oncol Hematol. 71(2): 127-164, 2009 [PubMed]
3) American Cancer Society. Cancer Facts & Figures 2011
4) Matsuda T, et al.: Jpn J Clin Oncol. 41(1): 40-51, 2011 [PubMed]
5) Okamoto I, et al.: Jpn J Clin Oncol. 40(1): 17-23, 2010 [PubMed]
