The European Cancer Congress 2013 - ESMO
EXPERT-C試験は高リスク直腸癌における術前化学放射線療法としてCAPOXにCetuximabを併用することの意義を検証した第II相の臨床試験であり、CR率およびPFS (progression-free survival) においてCetuximab併用による有意な改善が認められなかったことが既に報告されている。しかし、追跡期間中央値37ヵ月時点においてKRAS /BRAF 野生型症例ではCetuximab併用によるOS (overall survival) 延長効果が確認されている。
今回は追跡期間を延長し、有効性を再度検討した報告 (#2168)、および効果予測因子としてのTP53 変異解析の報告 (#LBA7) が発表された。

EXPERT-C試験は、切除可能高リスク直腸癌に対する術前CAPOX → Capecitabine + 放射線療法 → 手術 → 術後CAPOXという一連の周術期治療における、CAPOXおよびCapecitabineへのCetuximabの上乗せ効果を検証した第II相試験である。全身化学療法により臓器転移を、化学放射線療法により局所再発を低下させることを目的としており、さらにCetuximabによる上乗せ効果が期待された。
主要評価項目であるpCR率は既に論文として報告されており、Cetuximabの上乗せ効果は認めなかった1)。しかし、奏効率 (OR=0.39, p=0.038) およびOS (HR=0.27, p=0.034) でCetuximab併用 (CAPOX-C) 群で有意に良好な可能性が示唆されていたため、今回観察期間を延長した結果が報告された (#2168)。結果は、5年OSにおいて両群間に有意差を認めず、周術期のCetuximabの上乗せ効果は全体として否定された形である。
注目すべきは、「Presidential Session」として発表された、効果予測因子としてのTP53 についての報告である (#LBA7)。TP53 は腫瘍抑制遺伝子であり、細胞増殖、DNA修復機能に関与していることが知られている。そして結果は、TP53 野生型においてPFS (HR=0.23, p=0.02)、OS (HR=0.16, p=0.02) と有意にCetuximabの上乗せ効果を認めた。驚くべきはforest plotであり、TP53 野生型ではKRAS /NRAS /BRAF /PIK3CA 変異型でもCetuximabの上乗せ効果を認めた。近年metastaticなsettingにおいて抗EGFR抗体薬の効果予測因子としてRAS 野生型が注目されているが、それと相反する結果と言える。
このような結果が出た背景として、本試験が術前術後というsettingであること、周術期に化学療法、分子標的薬、放射線療法と様々な治療が行われたこと、症例数が少ないこと、あくまで後ろ向きな解析であることなどが考えられるが、十分な症例数をもって前向きに検討したときに同様の結果が再現されるかは大変興味が持たれるところである。
DiscussantのVan Custem氏が述べていたように、直ちに臨床の現場が変わる結果ではないと考えられるが (因みにVan Custem氏のコメントは「Congratulation!!」であった)、Cetuximabの効果予測、症例選択、術前術後治療の開発という点で一石を投じる報告であることは間違いない。

EXPERT-C試験には、2005年10月〜2008年7月までに164例が登録され、Cetuximab併用の有無による有効性・安全性が検討された (図1)。主要評価項目はKRAS /BRAF 野生型におけるpCR率、副次評価項目をPFS、OSと設定した。併せて、全体解析においてもPFS、OSを評価している。
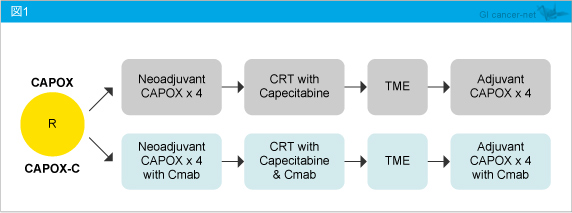
149例がKRAS およびBRAF 解析可能であり、そのうち90例がKRAS /BRAF 野生型で、CAPOX群44例、CAPOX-C群46例であった。追跡期間中央値は63.8ヵ月であり、45例は死亡し、4例は追跡不能で、54イベントがみられた。
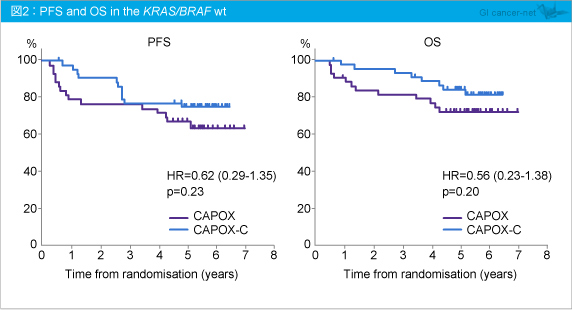
KRAS /BRAF 野生型において、5年PFSはCAPOX群67.8%、CAPOX-C群75.4%であり、両群間に有意差を認めなかった (HR=0.62, 95% CI: 0.29-1.35, p=0.23)。同様に、5年OSはそれぞれ72.3%、84.3%であり、有意差を認めなかった (HR=0.56, 95% CI: 0.23-1.38, p=0.20) (図2)。なお、KRAS /BRAF statusと有効性との間に相関は認められなかった。
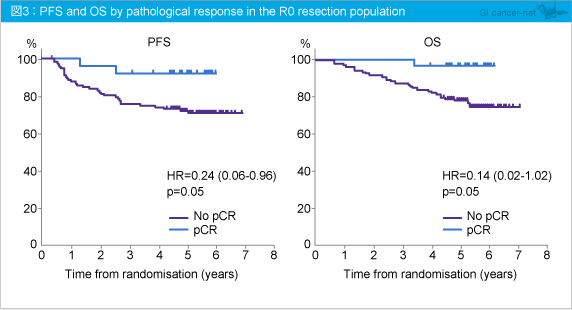
一方、R0切除が施行された140例を対象に、pCR群と No pCR群におけるPFS、OSを評価したところ、5年PFSは、pCR群92.3%、No pCR群72.0% (HR=0.24, 95% CI: 0.06-0.96, p=0.05)、5年OSはそれぞれ96.3%、77.3% (HR=0.14, 95% CI: 0.02-1.02, p=0.05) であり、pCR群で有意な予後延長効果が確認された (図3)。
高リスク直腸癌症例に対する術前化学療法は長期予後に寄与することが示された。一方、Cetuximab併用による予後改善効果は期待されるものの、有意差は認められなかった。また、pCRは高リスク直腸癌に対する術前化学療法をベースとした治療戦略を検討する臨床試験のサロゲートエンドポイントになる可能性がある。

TP53 は癌抑制遺伝子であり、細胞増殖やDNA損傷などに関与するとされている2, 3)。また、基礎実験において、p53の機能とEGFR阻害剤の効果が関連するという報告がある4-7)。そこで、EXPERT-C試験に登録された症例を対象に、TP53 変異の有無とCetuximabの有効性を検討した。
対象は、EXPERT-C試験に登録された164例のうち、組織標本の入手ができなかった症例、遺伝子増幅が十分でなかった症例を除いた144例であり、解析対象症例のTP53 変異の有無別、治療薬別におけるPFS、OSを比較検討した。
遺伝子変異に関しては、EXPERT-C試験に登録された症例の組織標本を用い、fluorescent PCR法によりゲノムDNAを抽出した。なお、TP53 exon 4-9の変異は、キャピラリー電気泳動法を用いた一本鎖DNA解析によりスクリーニングされ、双方向性のサンガー法によるDNAシークエンスにより変異の有無を評価した。
144例中75例 (52.1%) にTP53 変異が認められ、内訳はexon 4: 14例、exon 5: 25例、exon 6: 8例、exon 7: 23例、exon 8: 15例、exon 9: 0例であった。
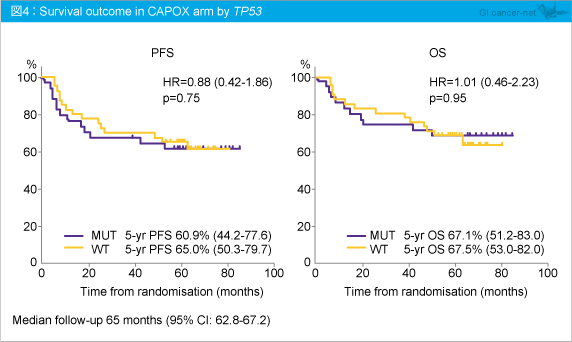
全体解析において、5年PFSはTP53 変異型群60.9%、 TP53 野生型群65.0% (HR=0.88, p=0.75)、5年OSはそれぞれ67.1%、67.5% (HR=1.01, p=0.95) であり、TP53 変異の有無はPFS、OSに影響を与えなかった (図4)。
CAPOX群、CAPOX-C群におけるTP53 変異の有無別における比較では、TP53 野生型において5年PFSはCAPOX群65.0%、CAPOX-C群89.3% (HR=0.23, p=0.02) (図5)、5年OSはそれぞれ67.5%、92.7%であり (HR=0.16, p=0.02) (図6)、PFS、OSともに有意に延長することが示された。なお、TP53 変異型では両群に差を認めなかった。
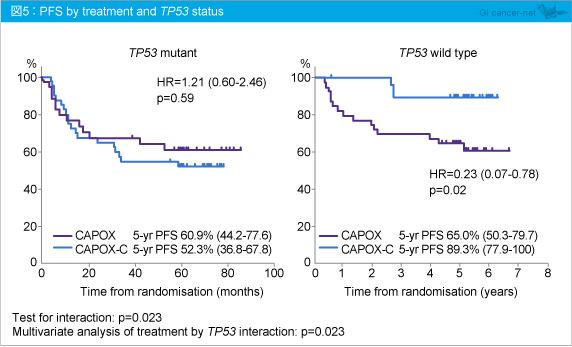
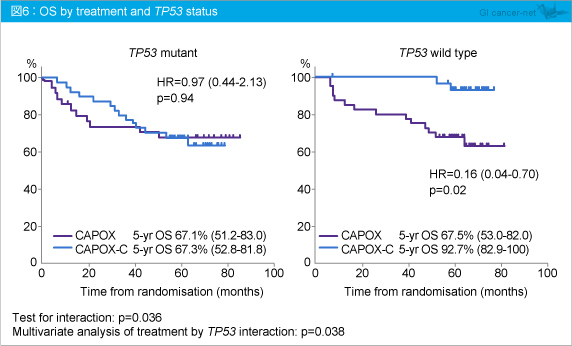
また、KRAS /NRAS /BRAF /PIK3CA 変異の有無別におけるOSへの影響を検討したところ、TP53 野生型においてはKRAS /NRAS /BRAF /PIK3CA 変異の有無にかかわらず、CAPOX-C群で良好であることが示された (図7)。
一方、奏効率ではTP53 野生型においても、Cetuximab併用による有意な上乗せ効果は認められなかった (表)。
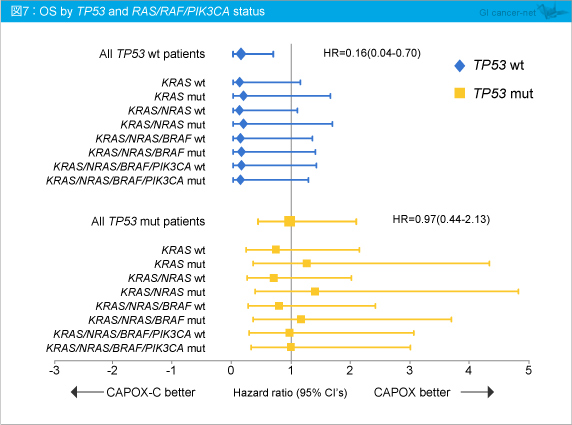
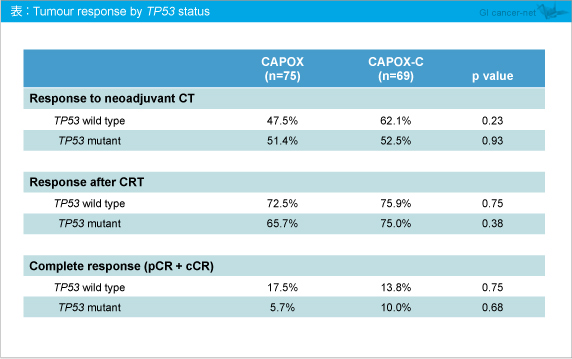
高リスク直腸癌に対して、CetuximabはTP53 野生型において有意な予後改善効果を認めた。TP53 変異は予後因子ではないものの、Cetuximabの効果予測因子になり得ることが示された。TP53 野生型におけるCetuximabのベネフィットは、RAS 変異の有無および放射線感受性との間に関連性はない。
1) Dewdney A, et al.: J Clin Oncol. 30(14): 1620-1627, 2012[PubMed]
2) Brown CJ, et al.: Nat Rev Cancer. 9(12): 862-873, 2009 [PubMed]
3) Kruse JP, et al.: Cell. 137(4): 609-622, 2009 [PubMed]
4) Huang S, et al.: Cancer Res. 71(22): 7071-7079, 2011 [PubMed]
5) Bouali S, et al.: Cancer Gene Ther. 16(6): 498-507, 2009 [PubMed]
6) Rho JK, et al.: Cancer Res. 67(3): 1163-1169, 2007 [PubMed]
7) Chang GC, et al.: Eur J Pharmacol. 600(1-3): 37-44, 2008 [PubMed]


