
The 35th ESMO Congress, Milan 2010
Abstract #713P/174PD |
バイオマーカー解析を含む最新報告
#713P
Randomized, double-blind, placebo-controlled, multicentre phase III study of Capecitabine/Cisplatin + Bevacizumab or placebo as 1st-line therapy in patients with advanced gastric cancer (AVAGAST update)
E. van Cutsem, et al.
#174PD
Tumour biomarker analyses in the AVAGAST phase III randomized study of first-line Bevacizumab + Capecitabine/Cisplatin in patients with advanced gastric cancer
M.A. Shah, et al.
|
胃癌に対するBevacizumab併用療法の有用性は示されず、 |
|
|
今回の報告は、2010年 米国臨床腫瘍学会年次集会で報告されたAVAGAST試験のUPDATEである。 |
AVAGAST試験は、進行胃癌におけるCapecitabine + Cisplatin療法(XP)へのBevacizumab 併用の有効性および安全性を検討した多施設共同無作為化比較第III相試験である。2010年 米国臨床腫瘍学会年次集会において、一次エンドポイントであるOSについてのBevacizumabの有意な上乗せ効果は示されなかったが、二次エンドポイントであるprogression-free survival (PFS) およびobjective response rate (ORR) については有意に良好であることが報告された1)。
今回は、サブグループ解析の最新データ (#713P) とともに、本試験の登録患者における予後および効果予測因子となるバイオマーカーについてのプロスペクティブな解析結果を報告する(#174PD)。
切除不能進行再発胃癌・胃食道接合部癌 (腺癌) の初回治療例を、XP + Bevacizumab群とXP + placebo群に無作為に割り付けた。Capecitabineが使用できない地域では5-FUを使用した。
一次エンドポイントはOS、二次エンドポイントはPFS、ORR、安全性、QOL、バイオマーカーなどとした。
バイオマーカー解析のための腫瘍サンプルとして、登録患者の腫瘍組織のパラフィン包埋ブロックあるいは未染色スライドを収集した。免疫組織化学染色 (IHC) により、VEGF-A、VEGFR-1/2、neuropilin-1/2、HER2、EGFRについて解析した。バイオマーカーと治療効果の関係については、Cox回帰モデルを用いて検討した。
2007年9月〜2008年12月に774例が登録された。登録患者の内訳は、約半数がアジア (376例) であり、次いで欧州 (249例)、汎アメリカ (149例) の順であった。アジアの大半は日本と韓国であった (188例、153例)。
有効性についてのサブグループ解析 (#713P)
患者背景において10%以上の地域差がみられたのは、「原発巣」「測定可能病変の有無」「肝転移の有無」であった(表1)。
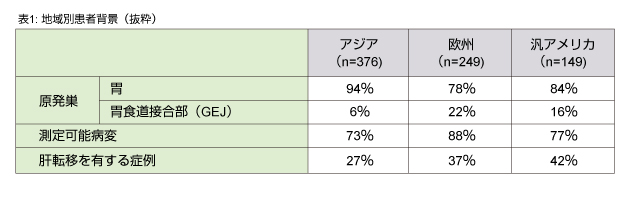
OSおよびPFSにおける地域差は既報の通りである1)。
二次エンドポイントであるORRは、XP + Bevacizumab群とXP + placebo群でそれぞれアジア: 47.9%、45.5% (OR=1.10、95%CI: 0.69-1.77)、欧州: 41.3%、28.2% (OR=1.79、95%CI: 1.02-3.15)、汎アメリカ: 50.0%、36.4% (OR=1.75、95%CI: 0.83-1.97) であり、ORRにおけるBevacizumabの上乗せ効果は、欧州および汎アメリカにおいて高い傾向がみられた。
アジアにおけるサブグループ解析の結果は表2に示す通りである。OS中央値は、XP + Bevacizumab群、XP + placebo群ともに日本が最長であった (15.4ヵ月、14.2ヵ月)。一方、韓国のOS中央値はそれぞれ13.8ヵ月、10.9ヵ月であり、両群の差は約3ヵ月と最大であった。PFS中央値のアジア地域内での差は認められなかった。
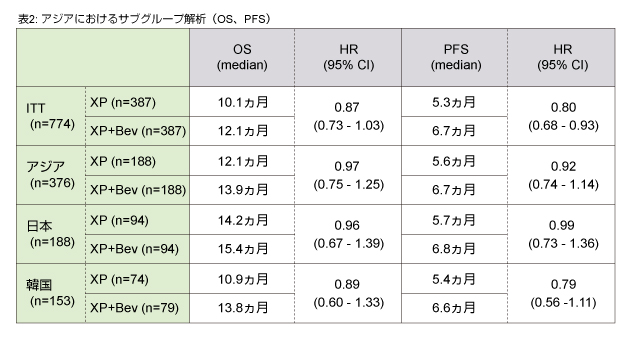
後治療については地域差が大きく、アジアでは66%の症例で2nd-line治療が行われたのに対し、欧州は31%、汎アメリカでは21%であった。
バイオマーカー解析 (#174PD)
本試験の登録患者774例のうち、629〜727例 (81〜94%) の腫瘍サンプルを用いて解析を行った。
XP + placebo群において、neuropilin*の発現レベルが中央値より低い群は、高発現群に比べてOSおよびPFSが低い傾向にあり、neuropilinの予後予測因子としての可能性が示唆された。一方、XP + Bevacizumab群では、neuropilin低発現群におけるBevacizumabの上乗せ効果が大きく、特にPFSにおいてその傾向が顕著であった。
Neuropilinの発現レベルは腫瘍のタイプおよびPSと相関があり、さらにはアジアとそれ以外の地域でも差が認められた (表3)。
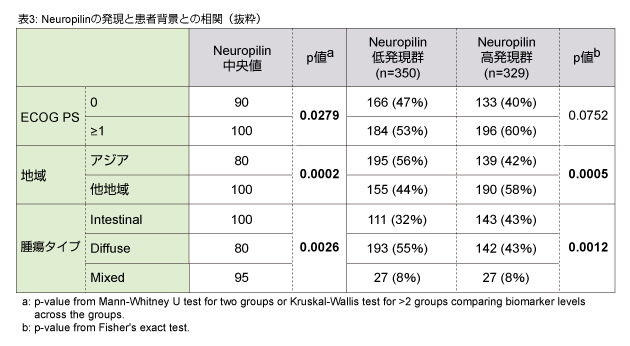
しかしながら、腫瘍サンプルの提出方法が各地域で異なり、現時点ではneuropilinの発現レベルの地域差について言及するには至らない。なお、HER2 statusによるOS中央値に差は認められなかった。
*neuropilin: VEGFR2のco-receptorとして強調してVEGFシグナルを伝える。
今回のサブグループ解析から、患者背景の違いなどにより、OS、ORRなどの臨床転帰に地域差があることが認められた。また、neuropilinが進行胃癌患者の予後およびBevacizumabの治療効果予測の有力なバイオマーカー候補であることが示唆された。現在、本試験における別のバイオマーカーに関する解析が進行中である。
Reference
1) Kang Y-K, et al.: 2010 Annual Meeting of the American Society of Clinical Oncology®, abst #LBA4007 [学会レポート]

