
The 35th ESMO Congress, Milan 2010
Abstract #583PD |
Efficacy and safety of second-line treatment with panitumumab plus irinotecan, both given every three weeks (Q3W), in patients (pts) with wild-type (WT) K-RAS metastatic colorectal cancer (mCRC): A study from the Spanish Cooperative Group for the Treatment of Digestive tumours (TTD)
A. Gomez, et al.
|
CPT-11 + Panitumumab併用療法 待望の第一報 |
|
|
Panitumumabは二次治療における有用性が大変期待されているが、今回はその最も有望なパートナーであるIrinotecan (CPT-11) との併用療法の報告である。 |
Panitumumabは完全ヒト抗EGFRモノクローナル抗体であり、KRAS遺伝子野生型の転移性大腸癌患者に対する単剤および併用療法 (1st-line、2nd-line) の有効性と安全性が示されている。化学療法との併用を検討した過去の報告では、Panitumumabは2週毎の投与であり、転移性大腸癌患者を対象とした2nd-lineとしてのPanitumumab + Irinotecan (CPT-11) ベース化学療法の3週毎投与の報告はない。
本試験は、転移性大腸癌患者に対する2nd-lineとしてのPanitumumab + CPT-11併用3週毎投与の有効性および安全性を検討した、多施設共同シングルアーム第II相試験 (NCT00475293) である。
対象は1st-lineとしてFUベースの化学療法を受けてPDが認められた転移性大腸癌患者 (18歳以上、ECOG PS 0-2) としたが、途中でKRAS遺伝子野生型患者のみに変更した。
Panitumumab 9 mg/kg + CPT-11 350 mg/m2 (>70歳およびPS 2の患者は300 mg/m2) をPDまたは毒性により投与不可となるまで3週毎に投与した。
腫瘍の評価はinvestigatorがmodified RECIST ver. 1.0にもとづき9週間毎に行った。有害事象の表記にはMedDRA ver. 12.1を用い、CTCAE ver. 3.0に従って評価した。
| 一次エンドポイント Objective response rate (ORR) |
||
| 二次エンドポイント Disease control rate (DCR)、progression-free survival (PFS)、overall survival (OS)、有害事象 |
KRAS遺伝子野生型患者53例が登録された (男性: 66.0%、年齢中央値: 67歳、ECOG PS < 1: 90.6%)。前治療として、1st-lineにOxaliplatinベース: 84.9% (45/53例)、CPT-11ベース: 7.5% (4/53例) が施行されており、90.6% (48/53例) が手術を受けていた。
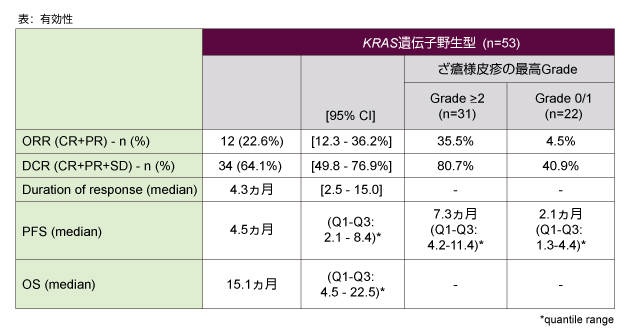
有効性を下表に示した。一次エンドポイントであるORRは22.6% (CR: 0/53例、PR: 12/53例)、二次エンドポイントであるDCRは64.1% (34/53例)、PFS中央値は4.5ヵ月 (Q1-Q3*: 2.1-8.4)、OS中央値は15.1ヵ月 (Q1-Q3: 4.5-22.5) であった。また、Panitumumab副作用であるざ瘡様皮疹の最高Grade別の有効性解析において、ORRおよびDCR、PFSのいずれもGrade 2以上の群で高値であった (表)。
*quantile range
Grade 3/4の有害事象としては、下痢 (35.9%)、ざ瘡様皮疹 (32.1%)、無力 (18.9%)、好中球減少 (13.2%) などが認められたが、皮膚症状および下痢は、対症療法や投与量の変更により対処可能であった。
本報告は、KRAS遺伝子野生型の転移性大腸癌患者に対する2nd-lineとしてのPanitumumab + CPT-11併用3週毎投与の有効性と安全性を示した初めての報告である。

