背景と目的
導入化学療法 (induction CT) によって病勢がコントロールされた局所進行膵癌に対する化学放射線療法 (CRT) は、化学療法 (CT) の継続よりも予後が良好である可能性が示唆されている1)。今回、4ヵ月間の導入化学療法後の局所進行膵癌に対するCRTの生存への影響を評価した国際第III相試験 (LAP 07試験) の結果について報告する。
対象と方法
対象は未治療の局所進行膵癌 (stage III) で、まず4ヵ月間の導入化学療法としてGemcitabine単独療法群とGemcitabine + Erlotinib療法群に無作為に割り付けられた。導入化学療法で病勢のコントロールが可能であった症例は、さらに2ヵ月間の治療を行うCT群またはCRT群に無作為に割り付けられ、導入化学療法でErlotinibが投与された患者はプロトコール治療終了後も維持療法として投与を継続した (図1)。
図1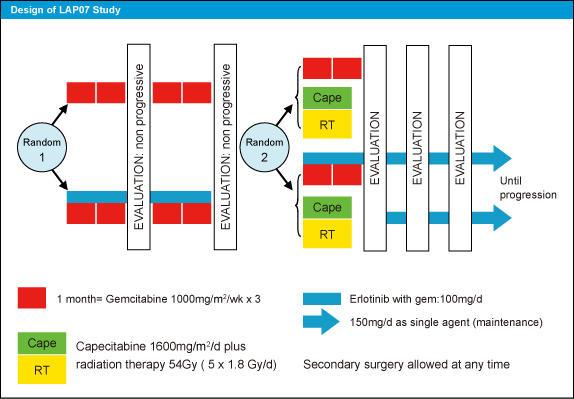
主要評価項目はCRTもしくはCTに割り付けられた患者のOS (overall survival)、副次評価項目はErlotinibの効果、放射線療法の質評価 (RTQA)、忍容性などであった。
統計学的考察では、試験期間を通じて病勢増悪30%、追跡不能5%、CRT群でのOS延長が9~12ヵ月 (HR=0.75、両側α=5%、β=20%) と設定したところ、必要症例数は722例 (392イベント) であった。なお、あらかじめ設定されていた中間解析 (2012年1月、最初の患者割付けから22ヵ月後) において仮説検証が行われ、必要症例数は420例 (196イベント) に修正された。
結果
導入化学療法には442例が登録され、Gemcitabine群223例、Gemcitabine + Erlotinib群219例に割り付けられた。Gemcitabine群とGemcitabine + Erlotinib群の患者背景に有意な差は認められなかった。続くCRTとCTには269例が登録され、CRT群133例、CT群136に割り付けられた。
追跡期間中央値が36ヵ月の時点 (2013年3月、死亡221例) で2回目の中間解析が行われ、主要評価項目のCRTとCT開始からのOS中央値はCRT群15.2ヵ月、CT群16.4ヵ月と有意差は認められなかった (HR=1.03, 95% CI: 0.79-1.34, p=0.8295) (図2)。また、PFS (progression-free survival) 中央値についてもそれぞれ12.5ヵ月、11.8ヵ月であり、有意差は認められなかった (HR=0.9, 95% CI: 0.7-1.1, p=0.2161)。この段階で、本試験におけるCRTの優越性を確認できないと判断されたことから、本解析をもって最終結果とした。
図2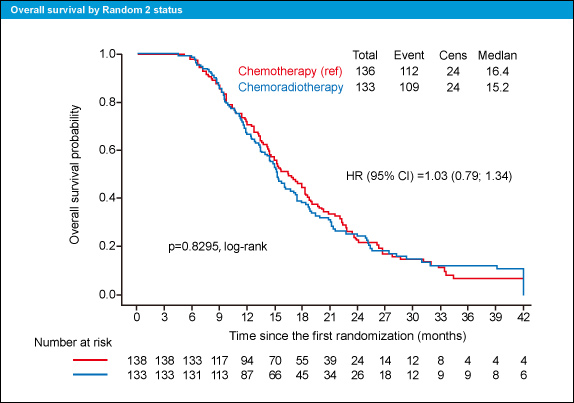
CRT群におけるRTQAはプロトコールどおり (PP) が37例 (31.6%)、小さな逸脱 (MID) 59例、大きな逸脱 (MAD) 21例、評価なし4例、治療なし12例であったが、これらのプロトコール逸脱は転帰に有意な影響を与えていなかった。
CRTとCTにおけるgrade 3以上の有害事象はCT群に比べCRT群で悪心が有意に多く認められたが (0% vs. 5.9%, p=0.009)、その他に差は認められなかった。なお、CRT群では放射線療法とは関連のない治療関連死が1例認められた。
また、導入化学療法開始からのOS中央値はGemcitabine群13.6ヵ月、Gemcitabine + Erlotinib群11.9ヵ月と有意差は認められなかった (HR=1.19, 95% CI: 0.97-1.45, p=0.0930) (図3)。またPFS中央値も、それぞれ10.7ヵ月、9.3ヵ月と差はなかった (HR=1.20, 95% CI: 0.9-1.4, p=0.1526)。
図3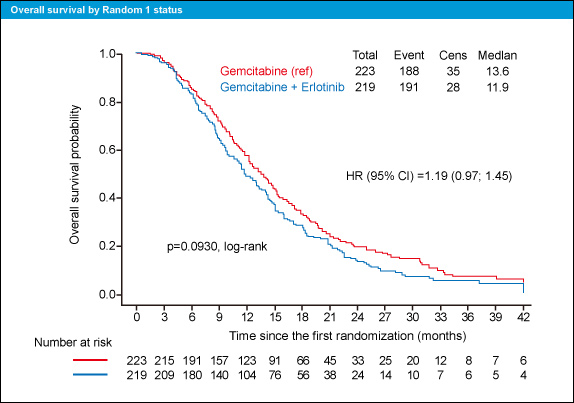
導入化学療法におけるgrade 3以上の有害事象は、Gemcitabine群に比べGemcitabine + Erlotinib群でヘモグロビン減少 (2.3% vs. 6.2%, p=0.04)、発熱性好中球減少症 (0% vs. 2.4%, p=0.03)、下痢 (1.4% vs. 6.6%, p=0.005)、ざ瘡様皮疹 (0.5% vs. 5.7%, p=0.007) が有意に多く認められた。
結論
導入化学療法によって病勢がコントロールされた局所進行膵癌に対するCRTは、CTの継続の効果を上回らないことが示された。また、導入療法におけるErlotinib併用による上乗せ効果は認められず、Erlotinibによる有害事象の頻度が高まると考えられた。
コメント
局所進行膵癌は、転移巣を形成した膵癌と比較して生存期間は長いが、極めて予後不良な疾患単位である。これまでに、Gemcitabine + 放射線療法 (RT) がGemcitabine単独療法と比較して全生存期間を延長すること2)、化学療法による導入後にRTを施行するとRT単独と比較して全生存期間が延長することが示された1)。今回の試験は、局所進行膵癌に対する導入化学療法後のRTの効果と導入化学療法におけるErlotinibの併用の意義を検証するものである。結果はいずれもnegativeで、RTを追加してもOSの延長は認められなかった。また、Erlotinibの併用によりHRは1を上回った。今後は、より有効な化学療法とRTとの併用効果を検証する必要がある。この演題を含むセッションでは、転移を有する膵癌に対するnab-PaclitaxelのGemcitabine単独療法への上乗せ効果が示された。またJASPAC試験の成績から、S-1には微小な膵癌集団を排除する効果があると考えられる。これらが、RTとの併用効果を検証すべき候補と考えられる。
(レポート:岩本 慈能 監修・コメント:大村 健二)
- Reference



