背景と目的
切除不能GISTにおいてImatinib、Sunitinib療法の施行後に増悪した場合、治療を中止すると急速な腫瘍増大をしばしば経験する。その際、日常臨床ではImatinibを再投与されることがあるが、Imatinib再導入の有効性については前向き比較試験で検証されていない。
対象と方法
対象は1st-line治療のImatinib (400mg/日) で効果が認められた後 (6ヵ月以上のCR、PR、SD)、Imatinib、Sunitinibを含むチロシンキナーゼ阻害剤 (TKI) に不応となったECOG PS 0-3の切除不能GIST患者であり、Imatinib群(400mg/日)とプラセボ群に1 : 1で無作為に割り付けられた。プラセボ群では増悪後にImatinib投与が、Imatinib群では増悪後に治療中止あるいはImatinib継続が許容された (図1)。
図1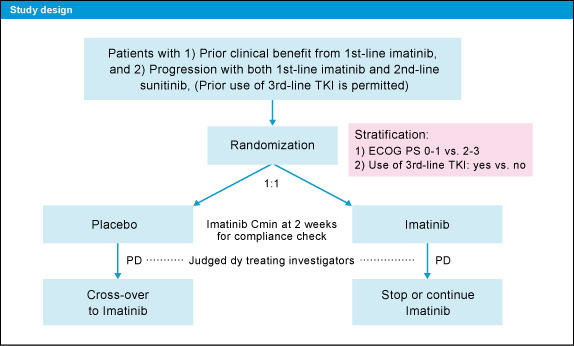
主要評価項目はRECIST ver. 1.0を用いた外部評価によるPFS (progression-free survival) であり、副次評価項目は12週時点での病勢コントロール率 (DCR)、OS (overall survival) などであった。腫瘍評価は、治療開始4ヵ月間は4週毎、以後PDまで8週毎に撮像されたCT画像が用いられた。Imatinib群で治療開始12週時点の増悪リスクが50%低下することを見込み、片側α=0.025、検出力85%として必要症例数は各群40例と計算された。
結果
2010年7月から2013年1月までに81例が登録された。患者背景には両群に大きな差を認めなかった (図2、3)。
図2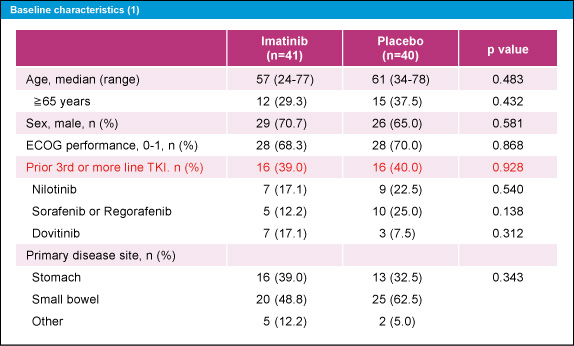
図3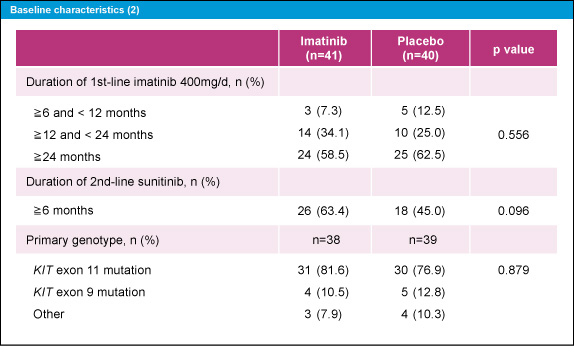
主要評価項目の外部評価によるPFSは、Imatinib群で中央値1.8ヵ月、プラセボ群0.9ヵ月とImatinib群で有意に良好であった (HR=0.45, 95% CI: 0.27-0.76, p=0.00075) (図4)。年齢、性別、PS、1st-lineのImatinib治療期間、KIT exon11変異の有無などでPFSに対するサブグループ解析を行ったが、いずれのグループにおいても Imatinib群で良好な傾向であった。
図4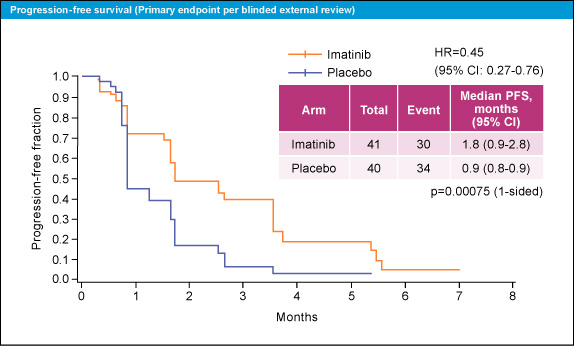
12週時点でのDCRも Imatinib群31.7%、プラセボ群5.0%とImatinib群が良好であった (p=0.003)。プラセボ群の92.5%に増悪後Imatinib投与が行われた。OSは、Imatinib群で中央値8.2ヵ月、プラセボ群7.5ヵ月と両群に明らかな差を認めなかった (HR=0.99, 95% CI: 0.57-1.72, p=0.4912) (図5)。
図5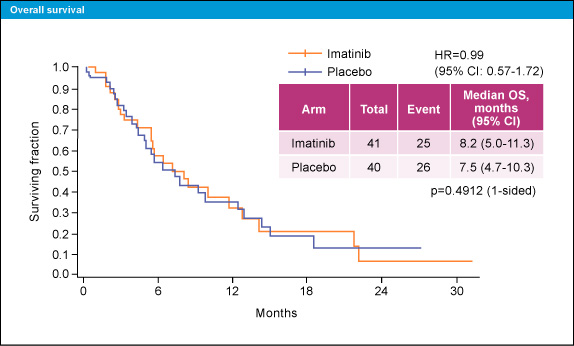
Imatinib群におけるgrade 3以上の有害事象は貧血 (29%)、倦怠感 (10%)、高ビリルビン血症 (7%) であり、既報と同程度であった。
結論
Imatinib、Sunitinib不応後の切除不能GISTに対するImatinib再導入は、PFSならびにDCRを改善した。
コメント
あらゆる抗癌剤、放射線などに耐性であるGIST治療において、唯一効果のある経口TKIのImatinibおよびSunitinibに耐性となれば、現時点では他に治療法がないため、Imatinibの再投与が計画されたものと思われる。本研究の結果は、本邦からほぼ同様な形で2010年の米国臨床腫瘍学会において発表された後ろ向き研究1)の解析結果と同じであり、2ヵ月あまりのPFSが得られていた。機序は、他の分子標的薬で治療中にGIST細胞内で二次耐性が生じ、再度Imatinibに感受性が生じるなどの仮説はあるが証明されていない。会場でも質問があったが、本年秋には、第三の経口分子標的薬となるRegorafenibが世に出るため、Imatinibのrechallengeの使い所は、通常はlast-lineであると思われるが、今後の検討が必要となる。
(レポート:谷口 浩也 監修・コメント:小松 嘉人)
- Reference
-
- 1) Sawaki, Komatsu, et al.: 2010 Annual Meeting of the American Society of Clinical Oncology®


