背景と目的
Gemcitabineは治癒切除後膵癌に対する術後補助化学療法として、現時点で最も推奨される標準治療である1,2)。これまで進行再発膵癌に対しては、GEST試験において、S-1はOS (overall survival) でGemcitabineに比して非劣性であることが証明されている3)。本試験の目的は、治癒切除後膵癌に対する術後補助化学療法としてのGemcitabineに対するS-1の非劣性を検証することである。主要評価項目はOSであり、副次評価項目は無再発生存期間 (RFS)、毒性、health-related QOLと設定した。
対象と方法
本試験は無作為化、非盲験、多施設共同の第III相試験である。病理学的に治癒切除された膵癌患者でUICC ver.6のstage I-IIIの症例を対象に、ECOG PSが0-1、十分な臓器機能が保たれた症例をS-1 (80/100/120mg/day、d1-28、6週毎、4コース) とGemcitabine (1,000mg/m2 iv、d1、8、15、4週毎、6コース) に無作為に割り付け、施設、切除断端、リンパ節転移の状況を調整因子とした (図1)。Gemcitabine群の3年OSを36%、非劣性マージンを1.25として、両群で360例となった。中間解析はイベント数180の時点と計画された。
図1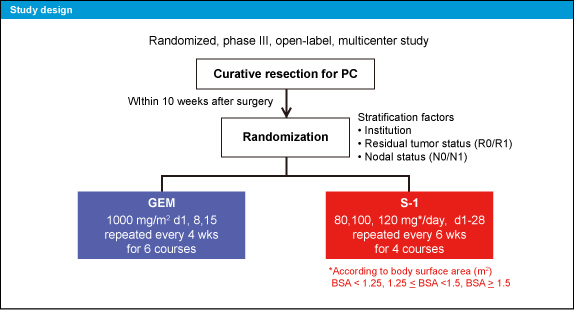
結果
2007年4月から2010年6月までの3年3ヵ月の間に、日本の33施設より385症例が登録された。2012年8月に中間解析が行われ、独立評価委員会より試験の中止と速やかな結果報告が推奨された。最終的な解析は2012年12月 (219イベント) に行われた。385例中378例がfull analysis setとして解析された。患者背景は両群で差を認めず、両群ともにT3、N1の症例およびstage IIが最も多く登録された。
主要評価項目であるOSの解析では、2年OSがS-1群70%、Gemcitabine群53%であり、HRは0.54、非劣性検定および優越性検定ともにp<0.0001と、S-1群で有意に優れた結果であった (図2)。サブセット解析からも、S-1群が大部分のサブセットでまさる結果であった。
図2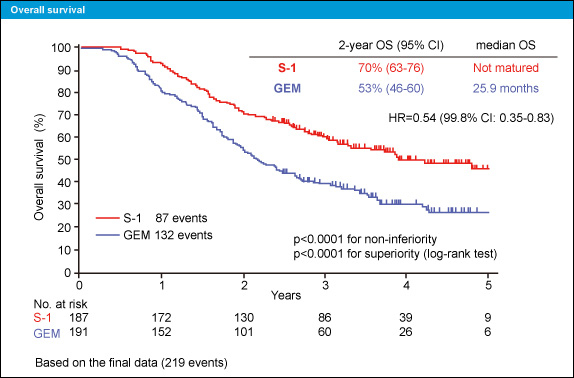
副次評価項目のRFSも、2年RFSはS-1群49%、Gemcitabine群29%であり、HRは0.57、優越性検定p<0.0001とS-1群が有意に優れていた。RFS中央値はそれぞれ23.2ヵ月、11.2ヵ月であった (図3)。サブセット解析もS-1群が大部分のサブセットで優れていた。
図3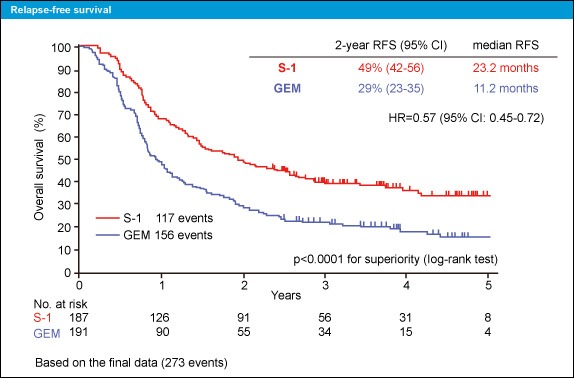
治療完遂率はGemcitabine群58%、S-1群72%であり、再発で中止となった症例はGemcitabine群14%、S-1群5%であった。Relative dose intensityはGemcitabine群84%、S-1群98%であった。
Grade 3/4の有害事象は、白血球減少、好中球減少、血小板減少などの頻度はGemcitabine群で、口内炎および下痢の頻度はS-1群で有意に高値であった。
再発部位は、肝、局所、リンパ節、腹膜、肺が主なものであるが、群間で大きな差を認めなかった。再発後の治療はGemcitabine群では、S-1ベースの化学療法が55%と最も多く、逆にS-1群ではGemcitabineベースの化学療法が57%と最も行われていた。
生存者のQOL (EQ-5D index) は、S-1群では全データおよび再発前データともに、治療開始12~24ヵ月時点で有意に良好であった。
結論
切除膵癌患者におけるS-1の術後補助化学療法はOS、RFSともにGemcitabineより優れており、有害事象は術後補助化学療法で用いた場合においても忍容可能であった。S-1は良好なQOLに寄与する可能性がある。S-1は切除後膵癌の新しい標準治療と考えられる。
コメント
今年のGastrointestinal Cancers Symposiumで発表されたJASPAC試験4)について、サブセット解析とQOL解析の結果が追加されて報告された。改めてみても、S-1のGemcitabine (GEM) に対する優越性は大きなものがあり、ほとんど全てのサブセットでS-1の効果が示されていた。ディスカッサントは、これまでの試験と比較して膵尾側切除が多いことや、サンプルサイズが小さいことを指摘していたが、どれもGEMに対するS-1の優越性を覆すものではない。唯一、GEST試験との成績の差は、論点になるところであるが、微小転移巣においてこそDPDが高発現し、S-1の効果がより顕著に現れるのではないだろうか。今後のTS、DPDなどのフッ化ピリミジン代謝関連酵素や、最近注目されているhENT1や核酸代謝関連酵素などを含めたバイオマーカー解析の結果に期待したい。
それにしても、これだけの効果が示されているにもかかわらず、S-1に対する米国の評価は厳しく、完全にAsian drugの扱いである。とりわけ司会のSyma氏の退屈そうな表情が印象に残ってしまった。近い将来にglobal drugとして再評価されることに期待したい。
(レポート:坂東 英明 監修・コメント:寺島 雅典)
- Reference
-
- 1) Oettle H, et al.: JAMA. 297(3), 267-277, 2007
- 2) Neuhaus P, et al.: 2008 Annual Meeting of the American Society of Oncology®: abst #LBA4504
- 3) Ueno H, et al.: J Clin Oncol. 2013 May 1; 31(13): 1640-1648. doi: 10.1200/JCO.2012.43.3680.
- 4) Katsuhiko Uesaka, et al.: 2013 Gastrointestinal Cancers Symposium: abst #145



