背景と目的
BRAF V600変異は、切除不能進行・再発大腸癌の5~10%に認められ、強い予後不良因子であることが知られている。BRAF 変異陽性メラノーマに対するBRAF阻害薬単独療法の奏効率は60~80%と高い有効性を認めるが1)、BRAF 変異陽性大腸癌に対しては奏効率が5%と期待されたような有効性は示されなかった2)。
一方、基礎研究ではBRAF阻害薬であるDabrafenib (GSK436) とMEK阻害薬であるTrametinib (GSK212) の併用療法の有効性が報告されていることから、この併用療法が臨床的に有効であるか否かを検討するため、本試験が行われた。
対象と方法
ECOG PS 0-1の臓器機能が保たれているBRAF V600変異陽性の切除不能進行・再発大腸癌患者42例 [Original efficacy cohort 26例、その後day 15の組織検体採取を必須とするPharmacodynamic (PD) expansion cohort 16例] に対し、Dabrafenib (150mg, 1日2回) とTrametinib (2mg, 1日1回) の併用療法が行われた。
結果
有効性と安全性の評価が可能であったのは40例であった。患者背景は女性が80%、PS 1が45%、前治療レジメン数3以上が53%、EGFR阻害薬の投与歴のある症例は45%であった。
腫瘍縮小割合はCRが1例、PRが3例で、奏効率は11%であった (図1)。また、minor responseを8例 (22%) に認めた。PFS中央値は3.5ヵ月 (95% CI: 1.8-4.9ヵ月) であった。
図1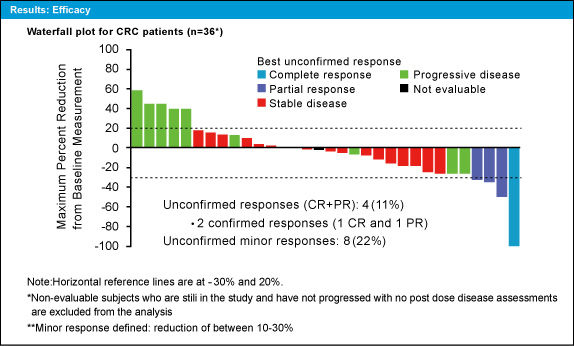
主な有害事象 (any grade) は、発熱63%、悪心60%、倦怠感53%、悪寒48%、嘔吐43%、頭痛30%などで、grade 3以上の有害事象の頻度は低かった (表1)。左室駆出率 (LVEF) 低下を18%に認めたが、扁平上皮癌の発生は認めなかった。
表1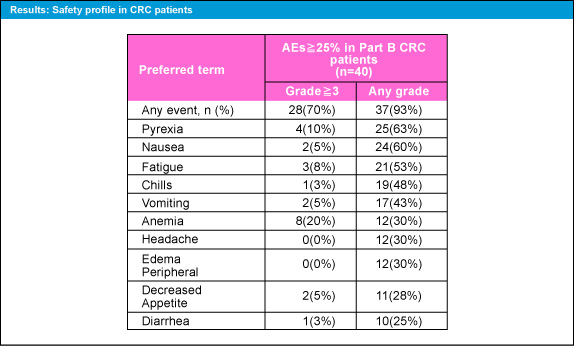
6例において、治療前と治療開始後day 15の組織検体を用いて免疫組織化学染色によりリン酸化ERK (pERK) 発現量を評価したところ、全例で治療後にpERK発現量の低下を認めた。
バイオマーカー解析では、いずれも少数例の検討であるが、Microsatellite Stability (MSS) 群に比較してMicrosatellite Instability (MSI) 群で (図2)、また、EGFR 高発現群に比較して低発現群で (図3)、治療効果が高い傾向が認められた。
図2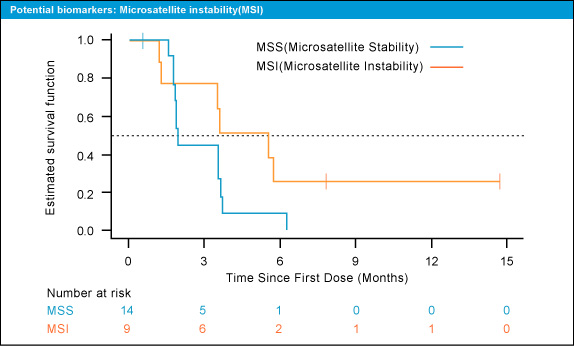
図3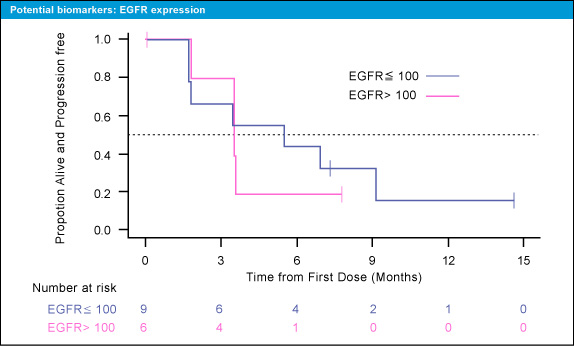
結論
DabrafenibとTrametinibの併用療法は忍容可能であり、BRAF 変異型大腸癌患者の一部に抗腫瘍効果が認められた。
コメント
大腸癌の薬物療法も、従来の腫瘍細胞に対する直接で網羅的な抗癌剤による治療から、特定の分子をターゲットにした分子標的薬の開発が可能な時代になってきている。現在、大腸癌においては抗EGFR抗体薬、抗VEGF抗体薬、および最近薬価収載されたマルチターゲットの経口TKIであるRegorafenibが実臨床で処方可能となっている。
BRAF V600変異は切除不能進行・再発大腸癌において、強い予後不良因子であることが知られており、また、BRAF 変異陽性メラノーマに対するBRAF阻害薬単独療法は奏効率60~80%と高い有効性を認めるため、大腸癌においてRas/Raf/ERKシグナル経路をダブルで阻害する目的で、BRAF阻害薬であるDabrafenibとMEK阻害薬のTrametinibの併用療法の臨床試験が行われた。結果は上述の如くで、約11%の症例に奏効が認められた。現在、大腸癌領域において実用レベルで使用できるバイオマーカーはKRASだけであり、今回のBRAFのように、新しいバイオマーカーの探索により、さらなる個別化医療の実践を図るべく、臨床試験をすすめ、有効な治療法の開発を進めていく必要があるものと思われる。
(レポート:谷口 浩也 監修・コメント:小松 嘉人)
- Reference
-
- 1) Flaherty KT, et al.: N Engl J Med. 363(9): 809-819, 2010[PubMed]
- 2) Kopetz S, et al.: 2010 Annual Meeting of the American Society of Oncology®: abst #3534



