|
 |
|
 |
ToGA試験は、HER2陽性の進行胃癌患者に対する1st-line治療にtrastuzumabを追加することのベネフィットを検討した試験である。Eric Van Cutsem氏(University Hospital Gasthuisberg, Leuven, Belgium)は口演(late-breaking)において、ToGA試験の有効性に関する成績を発表した。また、別のポスター発表ではYung-Jue Bang氏(Seoul National University Hospital, Seoul, Republic of Korea)が、ToGA試験の国際的スクリーニング・プログラムの解析に基づいて、進行胃癌の病理学的特徴とHER2陽性の関係について報告した。
確立されているHER2検査プロトコル(Hofmann et al,2006 Gastrointestinal Cancers Symposium)を用いて、ToGAの被験者のHER2状態を調べた。24ヵ国の3,807例から集められた腫瘍標本をホルマリン固定パラフィン包埋し、免疫組織化学染色法(IHC法)と蛍光in situハイブリダイゼーション法(FISH法)でHER2状態を検査した。IHC 3+および/またはFISH陽性の場合をHER2-陽性と定義した。
スクリーニングされた3,807例の標本のうち、3,667例の標本が評価可能であり、810例(22.1%)がHER2陽性であった。そのうち試験の適格基準を満たした584例を5-FUまたはcapecitabine+CDDP(FC群:290例)、5-FUまたはcapecitabine+CDDP+trastuzumab(FC+T群:294例)に無作為割り付けした。
これらの患者を進行癌と転移性癌、胃癌と胃食道接合部癌、測定可能病変の有無、ECOG のPS 0-1とPS 2、capecitabineと5-FUで層別化した。一次エンドポイントはOS、二次エンドポイントはPFS、TTP、ORR、臨床的ベネフィット比、奏効期間(DoR)、QOL、安全性、疼痛の強さ、鎮痛薬消費量、体重変化、薬物動態とした。
両群の患者背景に偏りはなく、男性が約75%であり、年齢中央値は約60歳であった。大部分の患者はアジア、中南米、ヨーロッパの出身であった。
HER2のスクリーニング検査の結果、IHC 0の4.9%、IHC 1+の15.7%がFISH陽性であった。
IHC 0/IHC 1+/FISH陽性の頻度は IHC 2+/FISH陽性とほぼ同等であったが、これは大部分のIHC 0/IHC 1+がFISH陰性である乳癌とは対照的であった。IHC 3+の5%はFISH陰性であった。
HER2陽性率はヨーロッパ(23.6%)とアジア(23.5%)では同等であったが、その他の国では異なっていた。
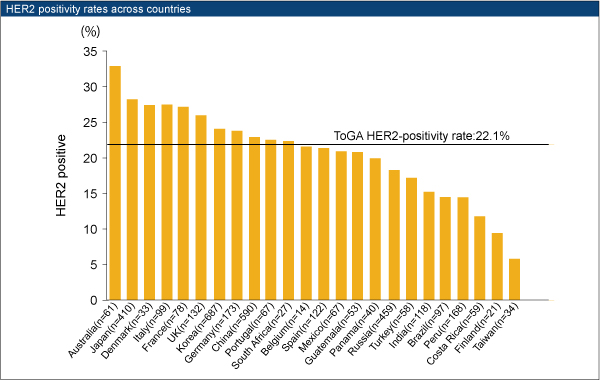
胃癌のHER2陽性率は20.9%であったのに対し、胃食道接合部癌では33.2%であった(p<0.001)。
組織型分類によってもHER2陽性率は異なり、intestinal typeは32.2%、diffuse typeは6.1%、混合型は20.4%であった(p<0.001)。
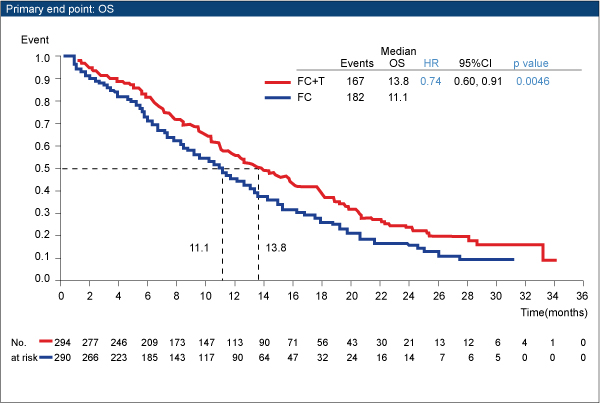
OS中央値はFC群(11.1ヵ月)に比べ、FC+T群(13.8ヵ月)で有意に長かった(p=0.0046)。
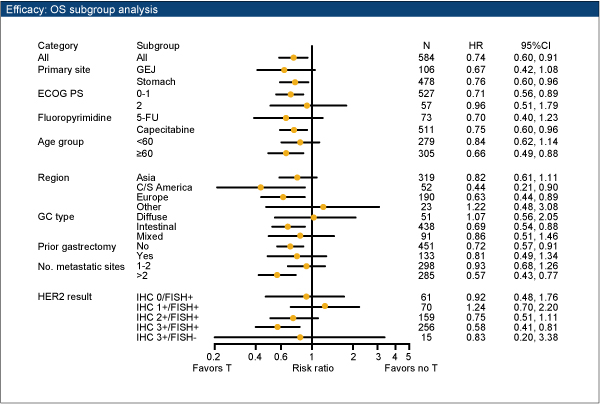
OSのサブグループ解析では、その他の国の患者とdiffuse typeの患者を除いて、大部分の患者ではtrastuzumabの追加によるベネフィットが認められた。
探索的解析ではあるが、IHC2+/FISH+またはIHC3+群では、OS中央値はFC+T群が16.0ヵ月、FC群が11.8ヵ月(HR 0.65、95%CI; 0.51-0.83)と更にOSの延長が認められた。
PFS中央値は、FC+T群が6.7ヵ月であったのに対し、FC群は5.5ヵ月であり(p=0.0002、HR 0.71、 95%CI; 0.59-0.85)、ORRはそれぞれ47.3%と34.5%であった(p=0.0017)。その他の二次エンドポイントもtrastuzumabの追加によって有意に改善した。
死亡率は、FC+T群が57%であったのに対し、FC群では63%であった。癌の進行による死亡はそれぞれ50%と57%、治療関連死は3%と1%であった。心毒性を含めた全体の安全性プロファイルにおいても両群間に差を認めなかった。
ToGA試験は、進行胃癌患者のHER2陽性に関する情報を得るために行われた初めてのプロスペクティブな第III相試験である 。HER2陽性の進行胃癌患者に対し、標準的化学療法にtrastuzumabを追加することで死亡リスクが26%低下し、生存期間中央値が約3ヵ月延長した。
また、この治療は忍容性も高かった。よって、化学療法とtrastuzumabの併用療法は、HER2陽性の進行胃腺癌患者のための新しい治療選択肢になり得ると考えられる。
一方、本試験のHER2陽性率は22.1%と、乳癌でみられた陽性率と同等であった。国によってHER2陽性率が異なるのは、組織型や腫瘍部位の違いによるものと考えられる。胃癌は乳癌よりも不均一で複雑な病態であるため、乳癌で用いられているHER2のスコアリングと評価をそのまま胃癌に適用することはできない。一次検査としてIHCを使用し、その次にFISH検査を行うべきである。現在、臨床効果とFISH比、多染色体性、腫瘍異質性などの関係を解析する研究が進行中である。
日本が参加したGlobal studyであること、及び分子標的薬剤の胃癌に対する有用性が初めて示された試験であることから、最も注目すべき報告の一つである。経口フッ化ピリミジン系抗癌剤が選択肢の一つ(日本はcapecitabine+CDDPの選択のみであった)にされている点も臨床に導入しやすいと考える。
HER2過剰発現は予後不良を意味する予後因子である。この集団に対するtrastuzumabの有用性が示されたことにより、胃癌も乳癌と同様に、個別化した治療戦略が立てられる時代に突入していくと思われる。今後は、trastuzumab単剤での効果、2nd-line治療における併用効果、さらには乳癌で話題となったBeyond progression、補助化学療法への導入等が検討されていくことなるだろう。いずれにせよ早い承認が望まれる。
(コメント・監修:佐藤 温)