 |
|||
|
 |
||
進行結腸・直腸癌に対するVEGF抗体であるbevacizumab + フッ化ピリミジンベースの化学療法は現在、標準的な一次治療と考えられている。また、EGFRに対するキメラモノクローナル抗体であるcetuximabは、単剤もしくは化学療法との併用により進行結腸・直腸癌に対し有効である。CAIRO2試験は、進行結腸・直腸癌においてcapecitabine + oxaliplatin + bevacizumab(CapeOX/Bev)にcetuximabを加える有用性を検討するためにデザインされた無作為化第III相試験である。
<対象>
進行再発結腸・直腸癌
測定可能病変を有する症例
転移に対し前治療が施行されていない症例
過去6ヵ月以内に補助化学療法を施行されていない症例
18歳以上
WHO PS 1以下の症例
十分な臓器・骨髄機能が保たれている症例
抗凝固療法を施行されていない症例
<方法>
| ・A群: | (CapeOX/Bev) | capecitabine | 1,000mg/m2 | 1日2回経口投与 | day1-14 |
| oxaliplatin | 130mg/m2 | day1 | |||
| bevacizumab | 7.5mg/kg | day1 | |||
| 3週毎に繰り返す。 7コース以降はoxaliplatinを中止し、capecitabineを1,250mg/m2を1日2回に増量した。 |
|||||
| ・B群: | CapeOX/Bev + cetuximab 400mg/m2を1コース目の1週目に静注、2週目以降は、250mg/m2を毎週静注した。 | ||||
一次エンドポイントはPFS、二次エンドポイントはOS、RR、毒性、トランスレーショナルリサーチである。3コース毎にRECISTにて効果判定し、コース毎にNCI-CTCにより毒性の評価を行った。
2005年6月より2006年12月までに、755例が本試験に登録され(適格症例736例)、A群368例、B群368例に無作為割り付けされた。年齢中央値(範囲)は62歳(27-83歳)であり、施行コース数中央値はA群10コース(1-39コース)、B群:9コース(1-40コース)であった。
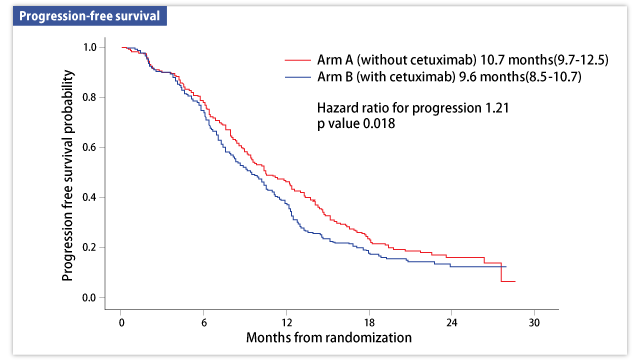
PFS中央値は、A群10.7ヵ月、B群9.6ヵ月であり(HR:1.21、95%CI:1.03-1.45)、有意な差が認められた(p=0.018:図1、表1)。
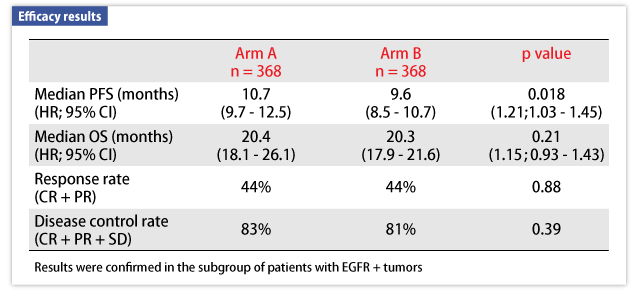
grade 3以上の有害事象(A群/B群)は、全体(72%/82%、p=0.0013)、皮膚毒性を除いた有害事象(72%/75%、p=0.37)、下痢(19%/26%、p=0.026)などで認められた(表2)。
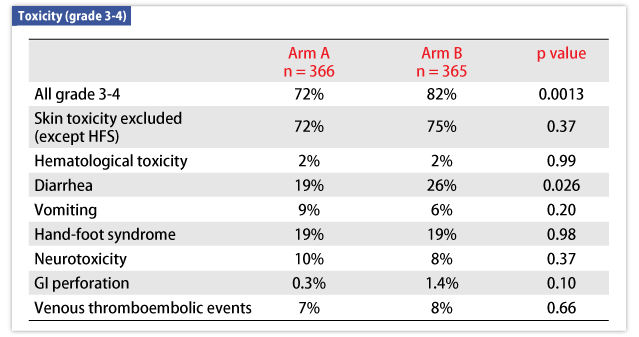
cetuximabに関連した皮膚毒性ではA群、B群においてそれぞれ全gradeのアクネ様皮膚反応(4%、84%)、grade 3のアクネ様皮膚反応(0.5%、25%)、全gradeの爪の変化(13%、32%)、grade 3の爪の変化(0.3%、4%)であり、B群で有意に高値であった(p<0.001)。
B群について皮膚反応のgrade毎にPFSを比較すると、皮膚反応が高度になるほど、PFSは有意に延長していた(p<0.01)。また、A群全例と、皮膚反応がgrade 0-1であったB群を比較すると、A群のPFSが有意に延長していた(p<0.0001)。
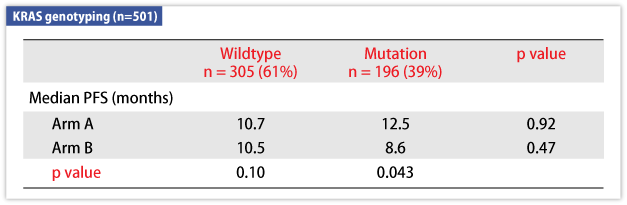
K-RASのwild type、mutation別にPFSを比較すると、wild typeではA群・B群間に差は認めなかったが、mutationではA群がB群に比して有意にPFSが延長していた(A群12.5ヵ月、B群8.6ヵ月 p=0.043)。OSでは有意差を認めなかった(A群24.9ヵ月、B群19.1ヵ月 p=0.35)。
CapeOX/Bevにcetuximabを加えることにより、有意なPFSの短縮を認めたが、OSに差はなかった。一方、皮膚毒性、下痢は有意に増加したが、その毒性は認容される範囲内であった。cetuximab関連の皮膚毒性のgradeは有意にPFSと相関していた。
K-RAS変異を伴う症例に対し、CapeOX/Bevにcetuximabを加えることにより有意なPFSの短縮を認めた。
CapeOX/Bevに対するcetuximabの上乗せ効果を検証した試験であるが、予想に反して、cetuximabの上乗せ効果は全く認められなかった。それどころか、K-RASのmutationを有する症例では、むしろ有意に劣る治療成績を示していた。以前に報告されたFOLFOX or FOLFIRI + bevacizumabに対して、cetuximabと同様の抗EGFR抗体であるpanitumumabの併用効果を検証したPACCE試験においてもpanitumumabの上乗せ効果が証明されなかったことから、詳細な機序は不明ではあるものの、抗VEGF抗体と抗EGFR抗体の併用は行うべきではないものと思われる。今後報告されるであろう小分子化合物との併用療法に期待したい。
(レポーター:佐瀬 善一郎 監修:寺島 雅典)