ESMO 2014 Congress
大腸癌
Abstract #549P
切除不能進行・再発大腸癌患者に対する1st-lineとしてのFOLFIRI + PanitumumabにおけるRAS /BRAF statusが有効性に及ぼす影響
Impact of Tumour RAS /BRAF Status on Efficacy of First-line Panitumumab + FOLFIRI in Patients with Metastatic Colorectal Cancer
Meinolf Karthaus, et al.

Expert's view

岩本 慈能 先生
関西医科大学附属
枚方病院
消化管外科
本報告ではRAS、BRAF ともに野生型の症例 (RAS およびBRAF 野生型) とRAS、BRAF いずれかが変異の症例 (RAS もしくはBRAF 変異型) と比較しているが、切除率は変わらないものの奏効率、PFSでは、RAS およびBRAF 野生型の方が、RAS もしくはBRAF 変異型より大きく上回っているとしている。
Panitumumabなどの抗EGFR抗体薬の使用において、今後はRAS 野生型の症例に限定すべきであると考えられるが、BRAF 変異型に関してはそれ自身が予後不良因子であると考えられ、あらたなストラテジーの開発が必要であると思われた。
切除不能進行・再発大腸癌に対する1st-lineにおけるFOLFOX4 ± Panitumumabを検討したPRIME試験1)、および2nd-lineにおけるFOLFIRI ± Panitumumabを検討した20050181試験2)において、KRAS exon 2以外のRAS 変異がPanitumumabの有効性に影響を与えることが示された。また、いずれにおいてもBRAF 変異が予後不良因子であることも報告されている1, 2)。
本報告は、切除不能進行・再発大腸癌に対する1st-lineとしてのFOLFIRI + Panitumumabを検討した第II相試験3)における、後ろ向きなRAS /BRAF 解析である。
本報告は、切除不能進行・再発大腸癌に対する1st-lineとしてのFOLFIRI + Panitumumabを検討した第II相試験3)における、後ろ向きなRAS /BRAF 解析である。
対象は、ECOG PS 0-2で、組織学的/細胞学的に診断され放射線学的に評価可能な未治療の切除不能進行・再発大腸癌患者で、主要評価項目は奏効率、副次評価項目は病勢コントロール率、奏効期間、PFS、TTP (time to progression)、安全性であった。なお、KRAS exon 2にはScorpion ARMS法 (DxS社)、その他のKRAS exon 3, 4、NRAS exon 2, 3, 4、BRAF exon 15には、双方向性のサンガー法によるDNAシークエンスが用いられ、変異の有無が評価された。
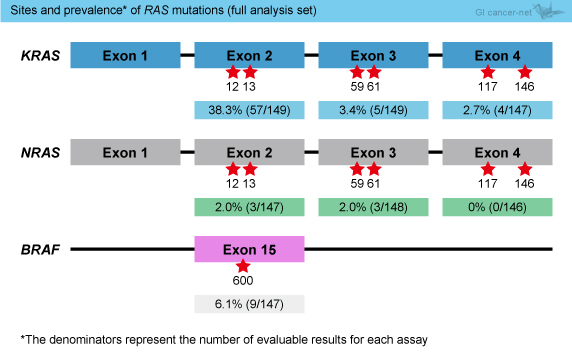
154例中150例においてRAS /BRAF 検査が行われ、150例中15例 (10%) でKRAS exon 2以外のRAS 変異が認められた (図1)。RAS データが得られた143例中69例 (48%) がRAS 野生型であり、74例 (52%) が何らかのRAS 変異を有していた。また、BRAF 変異はRAS 野生型に9例認められた。
 対象の年齢中央値は63歳で、RAS 野生型 (69例)、RAS 変異型 (74例)、RAS およびBRAF 野生型 (60例)、RAS もしくはBRAF 変異型 (83例) の患者背景は同様であった。
対象の年齢中央値は63歳で、RAS 野生型 (69例)、RAS 変異型 (74例)、RAS およびBRAF 野生型 (60例)、RAS もしくはBRAF 変異型 (83例) の患者背景は同様であった。
抗腫瘍効果は141例が評価可能であり、奏効率はRAS 野生型59%、RAS 変異型41%、RAS およびBRAF 野生型68%、RAS もしくはBRAF 変異型37%と、RAS 野生型、BRAF 野生型で良好であった (表)。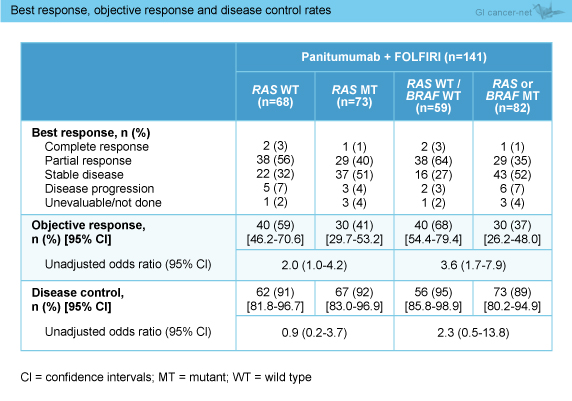 奏効期間中央値は、RAS 野生型13.0ヵ月、RAS 変異型5.8ヵ月であり、RAS 野生型で有意に良好であった (HR=0.16, 95% CI: 0.07-0.37)。
奏効期間中央値は、RAS 野生型13.0ヵ月、RAS 変異型5.8ヵ月であり、RAS 野生型で有意に良好であった (HR=0.16, 95% CI: 0.07-0.37)。
PFS中央値は、RAS 野生型11.2ヵ月、RAS 変異型7.3ヵ月、RAS およびBRAF 野生型13.2ヵ月、RAS もしくはBRAF 変異型6.9ヵ月であり、RAS 野生型、BRAF 野生型で良好であった (図2)。
TTP中央値はそれぞれ13.2ヵ月、7.3ヵ月、13.3ヵ月、7.2ヵ月、切除率はそれぞれ13%、9%、15%、8%であり、いずれもRAS 野生型、BRAF 野生型で良好であった。
なお、本解析において新たに問題となる有害事象は認められなかった。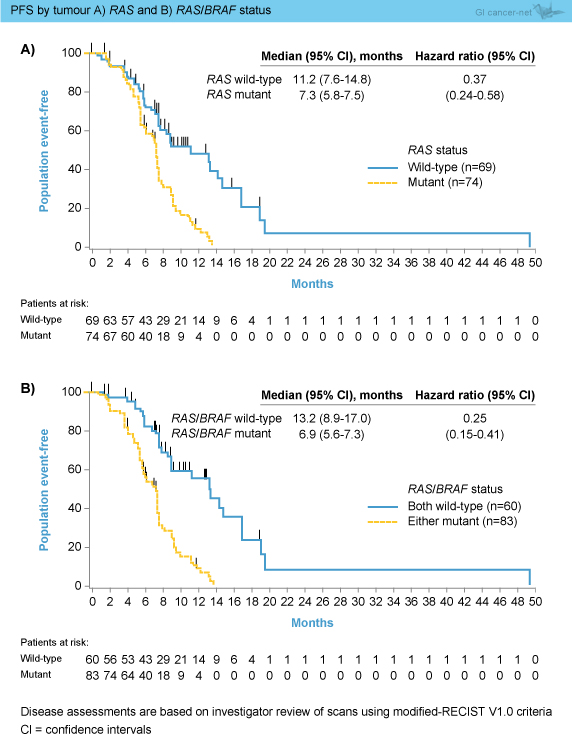
図1

抗腫瘍効果は141例が評価可能であり、奏効率はRAS 野生型59%、RAS 変異型41%、RAS およびBRAF 野生型68%、RAS もしくはBRAF 変異型37%と、RAS 野生型、BRAF 野生型で良好であった (表)。
表

PFS中央値は、RAS 野生型11.2ヵ月、RAS 変異型7.3ヵ月、RAS およびBRAF 野生型13.2ヵ月、RAS もしくはBRAF 変異型6.9ヵ月であり、RAS 野生型、BRAF 野生型で良好であった (図2)。
TTP中央値はそれぞれ13.2ヵ月、7.3ヵ月、13.3ヵ月、7.2ヵ月、切除率はそれぞれ13%、9%、15%、8%であり、いずれもRAS 野生型、BRAF 野生型で良好であった。
なお、本解析において新たに問題となる有害事象は認められなかった。
図2

既報と同様に、切除不能進行・再発大腸癌に対する1st-lineとしてのFOLFIRI + Panitumumabは、RAS 野生型で良好な成績が得られた。また、BRAF 変異は1st-line治療にかかわらず予後不良であると考えられる。FOLFIRI + Panitumumabは、RAS 野生型の1st-lineにおける他のFOLFIRI/FOLFOXと抗EGFR抗体薬の併用療法の報告と比較し、一貫した有効性を示した。
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。

