
(幨恀偼嫟摨尋媶幰偺D. Marino巵)


丂娞尷嬊揮堏偱偼愗彍屻偵巆娞婡擻偑曐偨傟傟偽愗彍偺揔墳偲峫偊傜傟傞丅屄乆偺揮堏偑戝偒偔悢偑尷傜傟偰偄傞応崌偼丄揮堏偑弅彫偡傞偙偲偱愗彍壜擻偲側傞壜擻惈偑崅偄偺偱丄弅彫傪慱偭偨弍慜壔妛椕朄偑桳岠偲峫偊傜傟傞丅杮帋尡 (METAPAN) 偺億僀儞僩偼2揰丄懳徾偲側傞娞揮堏偺婯掱偲丄壔妛椕朄儗僕儊儞偺慖戰偱偁傞丅
丂杮帋尡偺懳徾偲側傞娞揮堏偼丄3屄傛傝懡偔偰庮釃愯嫆棪50%埲忋丄懳懁偺灦忬愗彍傪敽偆娞梩愗彍傪梫偡傞娞揮堏丄傑偨偼愗彍偡傞偲椬愙偡傞2嬫堟傪巆偣側偄丄廫暘側寣棳傗抇娗僪儗僫乕僕傪堐帩偱偒側偄娞揮堏偱偁傝丄娞愗彍傪擮摢偵偍偄偰丄懡悢偺彫偝側揮堏偱偼側偔愗彍偺懳徾偵側傝傗偡偄戝偒側揮堏偑懡偔娷傑傟傞傛偆偵愝掕偝傟偰偄傞丅壔妛椕朄儗僕儊儞偼3廡偵1夞偺捠堾偱傛偄Panitumumab + XELOX偱偁傝丄Panitumumab傕9mg/kg傪3廡娫偵1夞搳梌偱偁傞丅
丂杮帋尡偱KRAS 栰惗宆偼35椺偱偁傝丄偐側傝恑峴偟偨娞揮堏偱偁傝側偑傜丄昡壙壜擻32椺拞憈岠棪65.7%丄15椺偑愗彍壜擻偲側傝 (10椺偼1夞栚偺昡壙)丄EW (-) 庤弍偼10椺丄OS (overall survival) 拞墰抣偼30.1儠寧偱偁偭偨丅偙偺傛偆偵Panitumumab偺弍慜壔妛椕朄傊偺婜懸偑朿傜傓寢壥偩偑丄桳奞帠徾偲偟偰壓棢偑25椺偵偁傝丄偦偺偆偪10椺偑grade 3埲忋偩偭偨偲偄偆栤戣揰傕巆偭偰偄傞丅XELOX偲Panitumumab (9mg/kg) 傪3廡娫偵1夞搳梌偲偟偨偙偲偑尨場側偺偐偼晄柧偩偑丄崱屻娞揮堏弍慜壔妛椕朄傪峫偊傞嵺偺婎弨傗丄傛傝桳奞帠徾偺彮側偄梡朄梡検傗慻傒崌傢偣傪峫偊傞昁梫惈側偳丄師偵偮側偑傞帋尡偲偟偰昡壙偟偨偄丅
丂昗弨壔妛椕朄 + 峈EGFR峈懱栻偵傛傞弍慜壔妛椕朄偼丄愗彍壜擻傑偨偼愽嵼揑偵愗彍壜擻側娞揮堏傪桳偡傞戝挵娻偵偍偄偰丄梊屻夵慞偵宷偑傞偙偲偑曬崘偝傟偰偄傞1, 2)丅偦偙偱丄愗彍晄擻恑峴丒嵞敪戝挵娻偺娞尷嬊揮堏姵幰偵偍偗傞弍慜壔妛椕朄偲偟偰偺Panitumumab + XELOX椕朄偺桳梡惈傪専摙偟偨丅
丂懳徾偼愗彍晄擻側娞揮堏偑偁傝丄懠憻婍偵揮堏傪擣傔側偄壔妛椕朄枹巤峴偺戝挵娻姵幰 (ECOG PS 0-2) 偲偟丄弍慜壔妛椕朄偲偟偰Panitumumab + XELOX椕朄 [Panitumumab (9mg/kg丄day1) 3廡枅 + L-OHP (130mg/m2丄day1) + Capecitabine (1,000mg/m2丄1擔2夞丄day1-14) 3廡枅] 傪巤峴偟偰丄4僒僀僋儖枅偵庮釃弅彫岠壥偍傛傃愗彍偺壜擻惈傪嵞昡壙偟偨丅
丂側偍丄乽愗彍晄擻側娞揮堏乿偺掕媊偼埲壓偵帵偡丅
| 丒 | 娞揮堏悢>3屄丄庮釃愯嫆棪>50%丄懳懁偺灦忬愗彍傪敽偆娞梩愗彍傪梫偡傞娞揮堏 |
| 丒 | 愗彍偡傞偲椬愙偡傞2嬫堟傪巆偣側偄丄傑偨偼廫暘側柆娗寣棳傗抇娗僪儗僫乕僕傪堐帩偱偒側偄娞揮堏 |
丂2007擭11寧偐傜2011擭1寧傑偱偵僀僞儕傾偺堛椕婡娭6巤愝偐傜49椺偑搊榐偝傟偨丅側偍丄2008擭11寧偐傜偼搊榐偵KRAS status偑昁梫偵側偭偨丅KRAS status偼栰惗宆35椺丄曄堎宆5椺丄晄柧9椺偱偁偭偨丅偦偺懠偺姵幰攚宨偼丄ECOG丂PS 0偑34椺 (69.4%)丄PS 1偑15椺 (30.6%) 偱偁傝丄暯嬒擭楊偼60.4嵨丄尨敪憙愗彍徢椺偼28椺 (57.1%)丄捛愓婜娫拞墰抣偼16.6儠寧偱偁偭偨丅
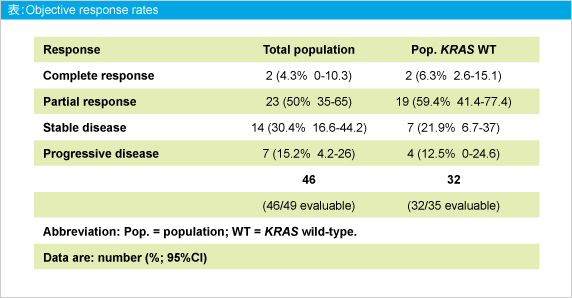
丂昡壙壜擻46椺偺偆偪CR偼4.3% (2椺)丄PR偼50% (23椺)丄SD偼30.4% (14椺) 偱偁傝丄憈岠棪偼54.3%偱偁偭偨 (昞)丅KRAS 栰惗宆姵幰32椺偵偍偗傞憈岠棪偼65.7% (CR 6.3%丄PR 59.4%丄SD 21.9%) 偱偁偭偨丅
丂傑偨丄帯椕奐巒屻偵乽娞揮堏愗彍壜擻乿偲恌抐傪偝傟偨姵幰悢偼丄嵞昡壙1夞栚10椺丄嵞昡壙2夞栚5椺偱偁傝丄愗彍椺偼慡偰KRAS 栰惗宆偱偁偭偨丅
丂慡懳徾偵偍偗傞OS拞墰抣偼23.9儠寧偱丄PFS拞墰抣偼11.5儠寧偱偁偭偨丅
丂僒僽僌儖乕僾夝愅偱偼丄娞揮堏愗彍椺偺OS拞墰抣偼36.6儠寧偲丄屍懅揑壔妛椕朄椺偺18.6儠寧偲斾傋偰桳堄偵墑挿偟偨 (p<0.001)丅傑偨丄KRAS status 偵傛傞夝愅偱偼丄KRAS 栰惗宆椺偺OS拞墰抣偼30.1儠寧偲丄KRAS 曄堎椺偍傛傃晄柧椺偺15.3儠寧偲斾傋偰桳堄偵墑挿偟偨 (p<0.001) (恾)丅

丂側偍丄昿搙偺崅偄桳奞帠徾偼徚壔婍撆惈丄旂晢忈奞丄慡恎徢忬偍傛傃恄宱撆惈偱偁傝丄摿偵壓棢偼25椺偵擣傔偨 (grade 3埲忋丗10椺)丅
丂崱夞偺専摙偵傛傝丄愗彍晄擻恑峴丒嵞敪戝挵娻偺娞尷嬊揮堏椺偵偍偗傞frontline偲偟偰偺Panitumumab + XELOX暪梡椕朄偺桳梡惈偑妋擣偝傟偨丅偙偺暪梡椕朄偵傛傝丄崅偄庮釃弅彫岠壥偑摼傜傟傞偲偲傕偵丄搊榐徢椺偺1/3偺徢椺偑愗彍壜擻偲昡壙偝傟偨丅
丂拲栚偡傋偒揰偲偟偰偼丄崱夞搊榐偝傟偨戝晹暘偺徢椺偱偼丄夠忬偺娞揮堏傪桳偟偰偄偨偵傕偐偐傢傜偢丄2椺偵CR傪擣傔丄OS拞墰抣偼婛曬偲斾妑偟偰傕懟怓側偐偭偨丅
