


治療開始8週目の効果判定の重要性は同じ抗EGFR抗体薬であるCetuximabを用いたOPUS試験やCRYSTAL試験1) でもすでに報告されているが、20%以上の早期腫瘍縮小症例 (ETS) ではその他の症例と比較して生存期間が延長される。
今回の報告はPRIME試験における8週目のETSを20%以上と30%以上で検討し、いずれの検討においてもETS群がPFSおよびOSにおいて生存期間が延長されるとの報告であった。このETS症例において生存期間が延長される傾向はPanitumumab + FOLFOX群においてもFOLFOX単独群においても同様に認められる。
一方OPUS試験とCRYSTAL試験では、化学療法 + Cetuximab群でのみETS症例において生存期間の延長を認めるが、化学療法単独ではこの傾向は認めておらず、結果が異なった理由は不明である。ただし、いずれにしても治療開始8週目における効果判定の重要性が示唆され、治療方針決定の参考になると思われる。
RECIST (固形がんの治療効果判定のための新ガイドライン) では、30%以上の腫瘍縮小に臨床的意義があると考えられている2)。また、抗EGFR抗体薬による治療を受けたKRAS 野生型切除不能進行・再発大腸癌症例では、8週時点でのRECIST奏効および20%以上の早期腫瘍縮小 (ETS) は、PFS (progression-free survival)、OS (overall survival) の改善を予測することが報告されている3, 4)。
今回、KRAS 野生型切除不能進行・再発大腸癌の1st-line治療としてPFSおよびOSの改善が示されたPRIME試験における8週時点での腫瘍縮小と、6ヵ月PFSおよび2年OSとの関連性を検証した。
PRIME試験の最終結果を用い、以下の基準で群別化してOSおよびPFS中央値を算出した。
−8週時点のRECIST奏効 (腫瘍縮小≧30%)
−8週時点のETS (腫瘍縮小≧20%)
さらに、上記の基準を満たす腫瘍縮小と、6ヵ月PFSと2年OSとの関連性について、相関係数 (φ) を用いて検証した。
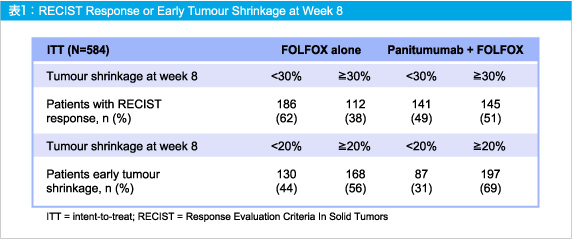
8週時点における腫瘍計測の可能な症例は582例であり (FOLFOX群298例、Panitumumab + FOLFOX群284例)、FOLFOX群のRECIST奏効38%、ETS 56%と比べ、Panitumumab + FOLFOX群ではそれぞれ51%、69%と高値であり、既報の抗EGFR抗体薬の結果と一致していた (表1)。
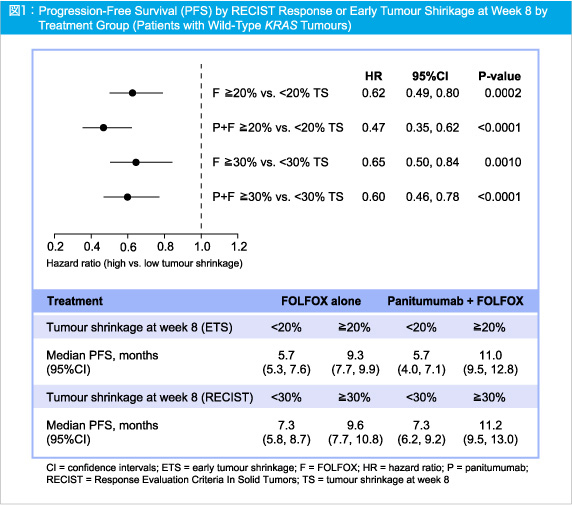
腫瘍縮小とPFSとの関連性について解析対象は491例 (腫瘍計測の可能例からcensored case 91例を除く) であり、8週時点のRECIST奏効またはETSを達成した症例は、治療内容にかかわらず、PFSの有意な延長を示した (図1上)。
また、PFS中央値は、FOLFOX群のRECIST奏効9.6ヵ月、ETS 9.3ヵ月と比べ、Panitumumab + FOLFOX群ではそれぞれ11.2ヵ月、11.0ヵ月と延長を示した (図1下)。
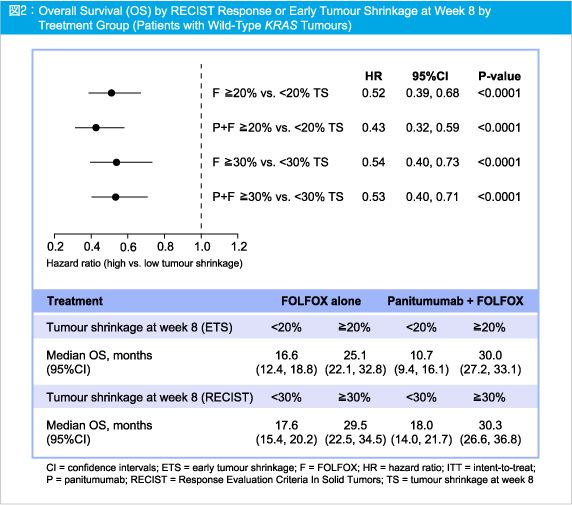
OSの解析対象は391例 (腫瘍計測の可能例からcensored case 191例を除く) であり、8週時点のETS達成例におけるOS中央値は、FOLFOX群25.1ヵ月と比べ、Panitumumab + FOLFOX群では30.0ヵ月と延長がみられたが、RECIST奏効例ではそれぞれ29.5ヵ月、30.3ヵ月と、両群ともに同程度の改善であった (図2)。
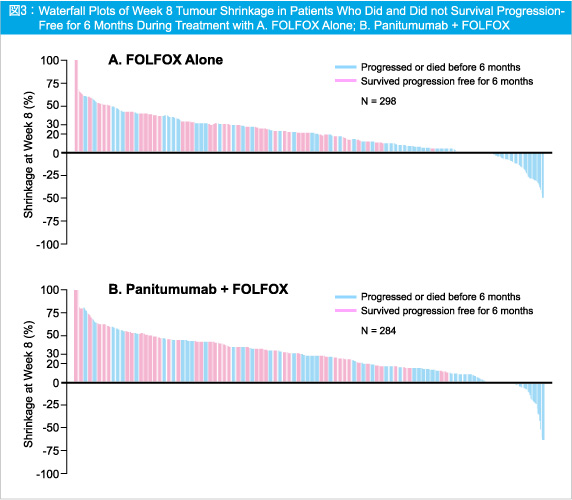
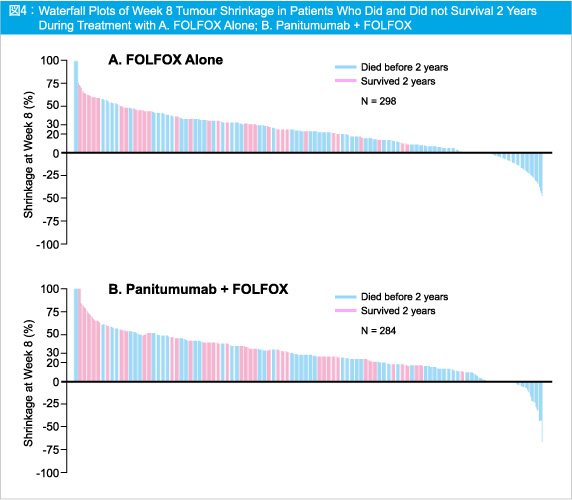
8週時点の腫瘍縮小率と6ヵ月PFSのwaterfall plot (図3) および2年OSのwaterfall plot (図4) より、腫瘍縮小率の高い症例では、低い症例に比べて、生存期間が延長する傾向がみられた。
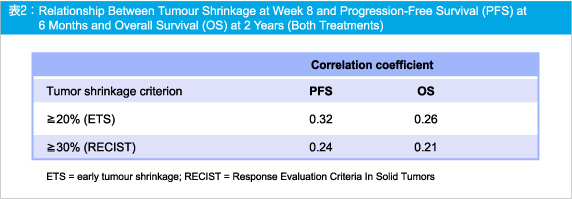
なお、8週時点における腫瘍縮小と、6ヵ月PFSおよび2年OSとの相関係数 (φ) は、ETSではPFS 0.32、OS 0.26であり、RECIST奏効ではPFS 0.24、OS 0.21であった (表2)。
PRIME試験において、8週時点での腫瘍縮小 (20%以上あるいは30%以上) の達成は、Panitumumab + FOLFOX療法を行った症例でより多くみられた。また、腫瘍縮小を達成した症例では、治療レジメンにかかわらず、PFSおよびOSの延長が示された。しかし、個々の患者レベルにおいては、早期腫瘍縮小は長期予後の予測因子になり得なかった。
早期腫瘍縮小の達成は、治療の重要なゴールの1つであるが、8週以内で腫瘍縮小を達成しなかった場合でも、治療の中断にはつながらないと考えられる。
1) Griebsch I, et al.: 2011 Gastrointestinal Cancers Symposium: abst #476
2) Therasse P, et al.: J Natl Cancer Inst. 92(3): 205-216, 2000 [PubMed]
3) Piessevaux H, et al.: ESMO 2010: abst #4777
4) Mansmann U, et al.: 2012 Gastrointestinal Cancers Symposium: abst #580
