


ヌクレオチド除去修復遺伝子であるERCC1の発現は、切除不能進行・再発大腸癌においてL-OHPの感受性に関連するとの報告を複数認める。今回の報告はstage III結腸癌におけるERCC1およびMMRの発現と補助化学療法との関連性を評価した。
その結果、L-OHP投与症例において、ERCC1が陰性であればDFS (disease-free survival)、OS (overall survival) ともに予後が良好であった。一方、MMRの発現や、L-OHPが投与されていない症例でのERCC1の発現は、予後とは関与しなかったと報告している。本邦では、stage III結腸癌に対する補助化学療法としてL-OHPを加えたFOLFOXやXELOXが標準療法のひとつとなっているが、欧米と比較して手術の治療成績が良好であることから、全例にL-OHPを投与することに対して賛否がある。今回の結果から、L-OHPを投与する症例の絞り込みにERCC1の測定結果が参考となる可能性が示唆された。
ERCC1 (excision repair cross-complementation group 1) の発現状況が、切除不能進行・再発大腸癌に対するL-OHPベース化学療法の効果予測因子としてのバイオマーカー候補であることが、いくつかの試験で示されてきた。また、術後補助化学療法については、5-FUによる治療を実施したstage II大腸癌におけるMMR (mismatch repair) の発現が、良好な術後生存に関連することが確認されている。しかしながら、L-OHPベースの化学療法を実施したstage IIIB結腸癌患者においては、ERCC1およびMMR発現との関連性は明確ではない。
対象は根治手術後のstage III結腸癌患者255例であり、95例にfull-courseの5-FU + LV (Mayo regimen) を、160例にmFOLFOX6またはXELOXを施行した。MMRおよびERCC1発現については、免疫組織化学的解析を実施した。
なお、5年DFSおよび5年OSによる予測モデルは、Kaplan-Meier解析、ロジスティックおよびCox回帰モデルを用いて解析した。
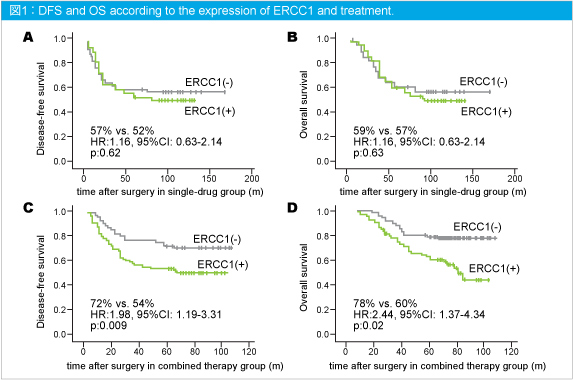
L-OHP併用例における5年DFSはERCC1陽性群では54%、陰性群では72%と、陰性群で有意に高かった (HR=1.98, 95%CI: 1.19-3.31, p=0.009) (図1C) 。5年OSにおいても陽性群60%、陰性群78%と、陰性群で有意に高かった (HR=2.44, 95%CI: 1.37-4.34, p=0.02) (図1D) 。また、多変量解析の結果、ERCC1発現はDFSとOSにおける有意に独立した予測因子であった (DFS:HR=2.33, 95%CI: 1.37-3.93, p<0.001) 、 (OS:HR=2.87, 95%CI: 1.59-5.16, p<0.001) 。
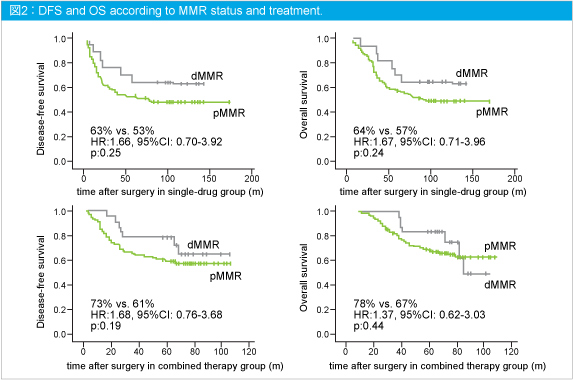
なお、5-FU + LV例においてERCC1発現はDFSおよびOSに有意な影響を及ぼさなかった (図1A・B) 。また、MMR発現はL-OHP併用例、5-FU+LV例ともにDFSおよびOSに有意な影響を与えなかった (図2) 。
ERCC1発現は、stage IIIB結腸癌治療において、5-FUにL-OHPを追加する際の効果予測因子となることが示された。なお、MMR発現は予測因子とならなかった。
